Hibridização - Orbitais
-
Upload
isabella-silva -
Category
Documents
-
view
27.655 -
download
2
description
Transcript of Hibridização - Orbitais

Orbitais Hibridização ou Hibridação

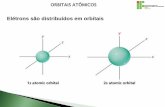
Orbitais
Região do espaço onde há maior probabilidade de se encontrar elétrons
Orbitais

Orbitais
Entretanto, os orbitais não representam a posição exata do elétron no espaço, que não pode ser determinada devido a sua natureza ondulatória; apenas delimitam uma região do espaço na qual a probabilidade de encontrar o elétron é elevada
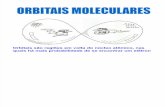
Na formação de pares eletrônicos, ocorre a fusão dos orbitais atômicos, originando o orbital molecular.
Carbono tetraédrico (Le Bel e Van´t Hoff, 1874): “O átomo de Carbono ocupa o centro de um tetraedro regular imaginágio e dirige suas valências para os quatro vértices do tetraedro.”
Orbitais

Orbital s
O orbital s tem simetria esférica ao redor do núcleo. São mostradas duas alternativas de representar a
nuvem eletrônica de um orbital s: 1. 2.
Em 1, a probabilidade de encontrar o elétron (representada pela densidade de pontos) diminui à medida que nos afastamos do núcleo.
Em 2, representa o volume esférico no qual o elétron passa a maior parte do tempo.
Orbitais

Orbital s
Orbitais
x
y
z

Orbital p
A forma geométrica dos orbitais p é a de duas esferas achatadas até o ponto de contato ( o núcleo atômico ) e orientadas segundo os eixos de coordenadas.
Orbitais

Orbital p
pz orbital py orbital px orbital
z
x
y
Orbitais

Orbital d
Os orbitais d tem uma forma mais diversificada: quatro deles têm forma de 4 lóbulos de sinais alternados ( dois planos nodais, em diferentes orientações espaciais ), e o último é um duplo lóbulo rodeado por um anel ( um duplo cone nodal ).
Orbitais

Orbital f
Os orbitais f apresentam formas ainda mais exóticas, que podem ser derivadas da adição de um plano nodal às formas dos orbitais d.
Orbitais

Ligações Covalentes
Resultam da sobreposição dos orbitais atômicos dos átomos que participam da ligação.
Os átomos compartilham o par eletrônico existente na ligação.
A ligação covalente pode ser polar ou apolar, que será visto posteriormente.
Podem ser do tipo sigma ou pi.
Orbitais

Carbono tetraédrico
Orbitais

Ligações simples
1. Tetraedros ligados por um vértice
Ex: etano H3C CH3
Orbitais

Ligações duplas
2. Tetraedros ligados por uma aresta
Ex: eteno H2C CH2
Orbitais

Ligações triplas
3. Tetraedros ligados por uma face
Ex: etino HC CH
Orbitais
H C C H

Hibridação/Orbitais
Orbitais/Hibridação

Hibridação ou Hibridização
Consiste na mistura de orbitais atômicos puros. São 3 tipos: sp3, sp2, sp.
hibridização "sp" é um orbital híbrido construído de um orbital "s" e um orbital "p".
Orbitais/Hibridação

Ligação sp
É a mistura de um orbital s com 1 orbital p, produzindo dois novos orbitais denominados híbridos sp.
Os orbitais híbridos sp formam um ângulo de 180 entre si.
A geometria molecular será linear. Surge em C com duas duplas ou C com uma
tripla ligação. Numa tripla ligação teremos uma ligação
sigma e duas pi (porção inferior da molécula)
Orbitais/Hibridação

Hibridização sp
Ex: Etino (Acetileno) C2H2
Etino (acetileno) Em torno dos átomos de C existem dois orbitais
híbridos sp e dois orbitais p “puros”. Os dois orbitais híbridos se ligarão através de
ligações sigma s-sp (H-C) e sigma sp-sp(C-C). Os dois orbitais p de cada carbono se ligarão
produzindo duas ligações pi entre os carbonos (resultando numa tripla ligação entre os dois carbonos).
Liga tripla uma ligação e duas ligações p
Orbitais/Hibridação

Hibridização sp
Ex: Etino (Acetileno) C2H2
• Fórmula estrutural do acetileno
Cada átomo de carbono é um híbrido sp.
Os hidrogênios possuem orbitais 1s, não
hibridizados.
Observe que a tripla ligação consiste de uma e 2p
As duas ligações p provem dos orbitais p, não
hibridizados.
C C H H
2p
2s
hibridação
2p
sp
Orbitais/Hibridação

Hibridização sp Ex: Etino (Acetileno) C2H2
C C H H
C C HH
Orbitais/Hibridação

Molécula de C2H2
Orbitais/Hibridação

Hibridação sp Etino (Acetileno)
C2H2
Orbitais/Hibridação

Tipos de ligações no C2H2
No acetileno existem 3 tipos de ligações: ligações sigma s-sp; ligação sigma sp-sp; ligações pi
[sp (C 1 ) – 1s (H) ] x 2 tipo
[sp (C 1 ) – sp (C 2 ) ] tipo
[2py (C 1 ) – 2py
(C 2 ) ] tipo p
[2pz (C 1 ) – 2pz
(C 2 ) ] tipo p
Orbitais/Hibridação

Hibridização sp2
É a mistura de um orbital s com dois orbitais p (pertencentes a um mesmo átomo), resultando em 3 novos orbitais denominados híbridos sp2.
Os três orbitais híbridos sp2 situam-se num mesmo plano formando ângulos de 120° entre si (geometria plana triangular).
Acontece com C que possua uma dupla ligação.
Num C do tipo sp2 existirá um orbital p “puro” que será responsável pela ligação covalente do tipo pi. Orbitais/Hibridação

Exemplo de hibridação sp2 H2C=CH2
Molécula de eteno (etileno).
Os dois átomos de C encontram-se ligados por uma dupla ligação Uma ligação sigma sp2-sp2 e uma ligação pi).
Cada átomo de C encontra-se ligado a dois átomos de H (duas ligações sigma s-sp2).
Orbitais/Hibridação

Hibridização sp2
Eteno H2C CH2
C C
H
H
H
H
C C
H
H
H
H
Orbitais/Hibridação

Hibridização sp2
Observe que a dupla ligação consiste numa
ligação do tipo e outra do tipo p.
C C
Orbitais/Hibridação

HIBRIDIZAÇÃO DO CARBONO sp2
Etileno C C H
H
H
H
Cada carbono é hibrido sp2 . O hidrogênio é 1s.
Uma ligação da dupla é sp2 - sp2. A outra é p - p.
2p
2s
hibridação
p
sp2 Orbitais/Hibridação

Os ângulos de ligações no C2H4
Como os átomos centrais são dois carbonos de hibridação sp2 o ângulo entre as ligações sigma será de 120. observe que a ligação p é perpendicular ao plano que contém a molécula.
C com uma dupla ligação hibridação sp2
Numa dupla ligação uma ligação e uma ligação p
Orbitais/Hibridação

A Molécula de C2H4 Hibridização sp 2
Orbitais/Hibridação

Hibridização sp3
É a mistura de 3 orbitais p “puros” com um orbital s “puro”, formando 4 novos orbitais “híbridos” denominados sp3.
A geometria dos 4 orbitais sp3 é tetraédrica (os 4 orbitais partem do centro do tetraédro e dirigem-se, cada um, para um dos vértices do tetraédro).
O ângulo entre os orbitais sp3 será de aprox.109°
Acontece no C que se liga através de 4 ligações simples ( o C é tetravalente).
Orbitais/Hibridação

Orbitais Híbridos sp3
Orbitais/Hibridação

Hibridização sp3
Orbitais/Hibridação

Carbono
O carbono possui 4 elétrons de valência 2s2p2
• O carbono pode formar ligações simples, duplas e triplas.
• O carbono pode apresentar orbitais híbridos do tipo sp, sp2 e sp3
O carbono é tetravalente.
Orbitais/Hibridação

Exemplo de ligação sp3 -> CH4
No CH4, os 4 orbitais híbridos sp3 do C se ligam com os orbitais s de 4 átomos de H, formando 4 ligações sigma C-H
[sp3 (C) – 1s (H) ] x 4 ligação
Orbitais/Hibridação

Metano
Fórmula molecular do metano: CH4
- Lembrando, 4 ligações simples sp3 ( 4 orbitais
híbridos). Hidrogênio possui 1s orbital não
hibridizado.
Fórmula estrutural do metano: C
H
H
H
H
Orbitais/Hibridação

Carbono Hibridizando
hibridação sp3

CH4 - metano
H
H
H
H
Orbitais/Hibridação

CH4 - metano
Orbitais/Hibridação
















![LISTÃO [Q.O.] - Introdução à química orgânica: Hibridização](https://static.fdocumentos.tips/doc/165x107/5899b6641a28aba11e8b5d85/listao-qo-introducao-a-quimica-organica-hibridizacao-58b170a791e35.jpg)
