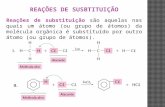
Reações de Substituição Eletrofílica Aromática_parte 1
-
Upload
wadson-leite-barbosa -
Category
Documents
-
view
245 -
download
5
description
Transcript of Reações de Substituição Eletrofílica Aromática_parte 1

Reações de substituiçãoeletrofílica aromática
CaioCaio Lima Lima FirmeFirme

Substituição eletrofílica aromática –
reações representativas
Benzeno ácido nítrico nitrobenzeno água
Benzeno ácido sulfúrico ácido benzenosulfônico água
Benzeno bromo bromobenzeno ácido bromídrico
Benzeno cloreto de t-butila t-butilbenzeno ácido clorídrico
Benzeno cloreto de propanoíla 1-fenil- ácido clorídrico
1-propanona

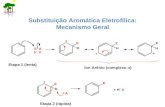
Reações eletrofílicas aromáticas: mecanismo Geral
+
Complexo sigma
EH
Complexo sigma
EH
Complexo sigma = cátion ciclohexadienila
Benzeno e o eletrófilo complexo sigma

Mecanismo geral de reações eletrofílicas aromáticas
Coordenada da reação
En
ergia
+ EY
EH
+
Y-
E
+ HY
EHδδδδ++++ δδδδ++++
Y-
EHδδδδ++++
δδδδ++++
Y-
+
EHE
++EY
Y-
HY
ETCVR
Estado detransição Estado de
transição
Intermediário

Complexo σσσσ
EH
+δ
1+
δ3
+
δ2
+
δ1
+ = δ3
+
δ1
−
δ3
−δ
2−
δ2
− = δ3
−
E= NO2
� O complexo σσσσ é eletronicamente equivalente ao cátion pentadienila (quatro elétrons ππππ deslocalizados)� As cargas positivas são distribuídas nas posições orto e para em relação ao sítio de substituição� A remoção do próton no sítio da substituição não ocorre simultaneamente com a inserção do eletrófilo.
F
H
H
+
SbF6- Determinado
por RMN

Nitração do benzeno� O HNO3 é um ácido e agente oxidante em altas temperaturas.� Como a reação do HNO3 com o benzeno é muito lenta, é necessário aquecer a
reação, o que pode fazer o HNO3 oxidar o benzeno.� Para resolver isso, usa-se H2SO4 que reage com HNO3 para formar o eletrófilo mais
forte – o íon nitrônio NO2+
� Síntese do nitrobenzeno: Adicionar 74g de H2SO4 em 50g de HNO3 em banho de gelo e depois acrescentar 26g de benzeno de 3 em 3mL. A temperatura não pode ultrapassar 55oC durante a adição. Depois, refluxar por 45 minutos.
Benzeno ácido nítrico nitrobenzeno (95%) água
H2SO4
30-40oC
HNO3 2 H2SO4 NO2+ H3O+
2 HSO4-
N
O
HO
O
-
H
H+
N
2 HSO4-
H
H2SO4
H3O+ N
H2SO4
HSO4-
HSO4-
O
O
N
O
HO
O
O-
HO
O
-
HNO3 2 H2SO4 NO2+ H3O+
2 HSO4-
N
O
HO
O
-
H
H+
N
2 HSO4-
H
H2SO4
H3O+ N
H2SO4
HSO4-
HSO4-
O
O
N
O
HO
O
O-
HO
O
-

Halogenação do benzeno� O bromo e o cloro não conseguem reagir diretamente com o benzeno porque o
benzeno não é um nucleófilo tão forte quanto os alcenos. É necessário o uso de ácido de Lewis para viabilizar a reação entre benzeno e halogênios.
� Ferro e bromo reagem formando FeBr3 que, em seguida, reage com bromo para formar o complexo de ácido-base de Lewis.
� A função do ácido de Lewis é enfraquecer a ligação halogênio-halogênio e diminuir a energia de ativação para a formação do complexo σσσσ.
� A anilina, com um grupo ativado amino, reage com bromo sem uso de catalisador.� A reatividade dos halogênios em substituição eletrofílica aromática: I2<Br2<Cl2<F2
� A iodação de tolueno e benzeno é feita com HNO3 que oxida o I2 a I+, que é mais reativo.
NH2
NH2
Br
Br
Br
+ Br2
Anilina
CH3 CH
3
I
I2
HNO3
+
Tolueno
Benzeno bromo bromobenzeno ácido
(65-75%) bromídrico
Fe
∆

Mecanismo da halogenção do benzeno
� Síntese do bromobenzeno: colocar 50g de benzeno seco, 0,5 mL de piridina e 125g de bromo em banho de gelo. Aumentar a temperatura para 70oC e deixar por 45 minutos até o vapor vermelho desaparecer.
� A cloração e a brominação do benzeno, usando AlCl3 como catalisador, é uma reação com cinética de terceira ordem. Isto é consistente com a formação do complexo Br2/Cl2-AlCl3 que age como agente halogenador ativo.
]].[AlClClou .[Braromático] ok.[compost reação da velocidade 322=

Sulfonação do benzeno
� A reação do trióxido de enxofre (SO3) com benzeno, catalisado por H2SO4, é muito mais reativa do que a reação do benzeno com ácido sulfúrico.
� O SO3 não é necessário na sulfonação do tolueno, pois o grupo metila é um moderado ativador da reação de substituição eletrofílica aromática.
H2SO4
120oC
H2SO4
120oCBenzeno trióxido ácido benzenosulfônico
de enxofre
H2SO4

Alquilação Friedel-Crafts do benzeno
� Os carbocátions são os eletrófilos mais importantes na substituição eletrofílicaaromática por causa da formação da ligação carbono-carbono (ligação muito forte).
� Uma das formas de se obter carbocátion é a partir da reação de haletos de alquila secundário e terciário ácido de Lewis. Dessa reação, forma-se o complexo ácido-base de Lewis que, em seguida, libera o carbocátion para reagir com o benzeno.
� No caso dos haletos de alquila primário, é o complexo ácido-base de Lewis que reage com o benzeno e não o carbocátion primário isolado porque este é muito instável para existir isoladamente.
Benzeno cloreto de t-butila t-butilbenzeno (60%) ácido clorídrico
Cloreto de t-butila
Cloreto de t-butila - cloreto de alumínio
Cloreto de alumínio
Complexo decloreto de t-butilacloreto de alumínio
t-butila Tetracloroaluminato
AlCl3
0oC

Alquilação Friedel-Crafts do benzeno
� Mecanismo da alquilação do benzeno a partir de haletos de alquila terciário e ácidode Lewis.

Alquilação Friedel-Crafts do benzeno
� Mecanismo da alquilação do benzeno a partir de haletos de alquila primário e ácidode Lewis.
Cl AlCl3
Cl AlCl3
CH3CH3Cl+AlCl3
+ HCl
CH3CH3Cl AlCl3+ CH3CH2
δ+
δ-
+ CH3CH2
δ+ -
+ HCl

Alquilação Friedel-Crafts do benzeno
� Rearranjos podem ocorrer quando haletos de alquila primários são usados para reagir com ácido de Lewis.
AlCl30oC

Alquilação do benzeno via outros agentes
alquilantes� Rotas alternativas para se formar carbocátions existem. Uma das formas
alternativas para se obter carbocátions é a partir da reação de álcoois ou alcenoscom ácidos fortes.
� A reação de compostos aromáticos com alcenos na presença de ácidos de Lewis é a base para a produção industrial de muitos compostos aromáticos alquilados. O estireno, por exemplo, é preparado pela desidrogenação do etilbenzeno, que é feito de benzeno e etileno.
Etil-benzeno
Ciclohexeno
Estireno Benzeno
Benzeno
Etileno
Ciclohexilbenzeno (65-68%)
HCl, AlCl3
H2SO4
ZnO
630oC

Limitações da alquilação Friedel-Crafts
� As reações de Friedel-Crafts somente funcionam com benzenos, halobenzenos e derivados de benzeno com substituintes doadores de elétrons. Elas falham com derivados de benzeno com substituintes retiradores (ou atratores) de elétrons, como NO2 e SO3H.
� A reação é sensível à umidade e ao ar por causa da formação do carbocátion. Por isso, para se fazer a reação de Friedel-Crafts deve-se usar atmosfera inerte, geralmente sob nitrogênio seco (técnica do balãozinho ou técnica de Schlenk).
� Haletos de alquila primário são suscetíveis a sofrerem rearranjo para formar um carbocátion mais estável, antes de reagirem com o benzeno.
� Como os grupos alquila são substituintes ativadores da reação de substituição eletrofílica aromática, o produto de alquilação de Friedel-Crafts é mais reativo que o reagente de partida (o benzeno). Por conta disso, é difícil parar a reação na monoalquilação do benzeno. A reação de alquilação de Friedel-Crafts tende a formar um produto dialquilado.
– Para se evitar a dialquilação da reação de Friedel-Crafts, usa-se grande quantidade em excesso do benzeno, na proporção de aproximadamente 50:1 (benzeno/haleto de alquila). Após a reação, é feita uma destilação que separa o excesso de benzeno do produto monoalquilado.

Acilação de Friedel-Crafts do benzeno
� A acilação de Friedel-Crafts é analoga à alquilação de Friedel-Crafts, exceto pelo reagente que é o cloreto de acila ao invés do cloreto de alquila.
� Para compostos aromáticos mais reativos (com substituintes doadores de elétrons), o eletrófilo ativo é provavelmente o complexo formado entre o haleto de acila e ácido de Lewis.
� Para compostos aromáticos menos reativos como benzeno (ou derivados com substituintes retiradores de elétrons), o eletrófilo ativo é provavelmente o íon acílio.
� O grupo acila não rearranja como acontece com os carbocátions derivados de haleto de alquila primários.
� O produto da reação de acilação de Friedel-Crafts é uma cetona aromática.
AlCl3
CS2, 40º C
Benzeno Cloreto de propanoíla 1-fenil-1-propanona (88%)
Íon acílio

Acilação de Friedel-Crafts e redução de Clemmensen
� É possível obter alquilbenzenos a partir da acilação de Friedel-Crafts.� O produto formado a partir da acilação de Friedel-Crafts, um acilbenzeno ou cetona
aromática, é reduzido a alquilbenzeno a partir da redução de Clemmensen.� Através da redução de Clemmensen, é possível alquilar benzenos que são
impossíveis via alquilação de Friedel-Crafts. Por exemplo, a obtenção de n-propilbenzeno a partir da alquilação de Friedel-Crafts, pois forma-se isopropilbenzeno por conta do rearranjo do carbocátion primário em carbocátionsecundário.
� A redução de Clemmensen consiste de um tratamento do acilbenzeno ou cetona aromática com HCl em agua e amálgama de zinco.
Benzeno cloreto de butanoíla 1-fenil-1-butanona (86%) Butilbenzeno (73%)
AlCl3
AlCl3HCl
Zn(Hg)
redução RC(O)Cl