qaula 59 e 60 - Your Company Name ano/aulas/aula 59_60_61_62_63... · Efeito do aumento de carga...
Transcript of qaula 59 e 60 - Your Company Name ano/aulas/aula 59_60_61_62_63... · Efeito do aumento de carga...
1830 – Johann Döbereiner
� Lei das tríadas
Grupos constituídos por três elementos
K 39
Na 23
Li 7
I 127
Br 80
Cl 35,5
1865 – John Newlands
� Lei das oitavas
Sete grupos constituídos por sete elementos
Ro, Ru
Di, Mo
Zr
Ce, La
Sr
Rb
Br
ThAuSeFeSO
BiNbAsMnPN
PbWInTiSiC
TlTaYCrAlBo(B)
HgBa, VZnCaMgG(Be)
OsCsCuKNaLi
Pt, IrICo, NiClFH
1869 – Dimitri Mendeleiev� Elementos ordenados por ordem
crescente de número de massa.
� Elementos com propriedades semelhantes no mesmo grupo.
1913 – Henry Moseley
� Identificou o número atómico com a carga positiva do núcleo de cada elemento;
� Verificou que o número atómico coincidia com o número de ordem do elemento.
Tabela Periódica
s1
s2 s2p1
s2
s2p2 s2p3 s2p4 s2p5 s2p6
Bloco s Bloco d Bloco p
Bloco f
Subnível 4f
Subnível 5f
Grupo 18 – Família dos gases nobres
� Configuração electrónica de valência ns2np6 ou ns2;
� Possuem oito ou dois electrões de valência;
� Elevada estabilidade;
� Reactividade muito baixa;
� Gases inertes;
� Forma monoatómica.
Grupo 1 – Família dos metais alcalinos
� Configuração electrónica de valência ns1;
� Possuem um electrão de valência;
� Originam iões monopositivos;
� Iões mais estáveis que os átomos correspondentes;
� Reactividade aumenta com o aumento do número atómico;
Hidrogénio – Situação especial
Semelhante aos metais alcalinos porque:
� Configuração electrónica ns1;
� Possuem um electrão de valência;
� Pode originar um ião monopositivo (H+).
Semelhante aos halogéneos porque:
� Pode originar um ião mononegativo (H-);
� O ião hidreto é muito reactivo;
� Halogéneos formam iões mononegativos.
Grupo 2 – Família dos metaisalcalino-terrosos
� Configuração electrónica de valência ns2;
� Possuem dois electrões de valência;
� Originam iões bipositivos;
� Iões mais estáveis que os átomos correspondentes;
� Reactividade aumenta com o aumento do número atómico;
Grupo 17 – Família dos Halogéneos
� Configuração electrónica de valência ns2np5;
� Possuem sete electrões de valência;
� Originam iões mononegativos (halogenetos ou haletos);
� Iões mais estáveis que os átomos correspondentes;
� Reactividade diminui com o aumento do número atómico;
Causas da variação periódica das propriedades
� Efeito do número quântico principal das orbitais de valência
Electrões mais afastados do núcleo
Menor atracção
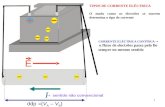
� Efeito do aumento de carga nuclear
Electrões mais atraídos ao núcleo
Contracção da nuvem electrónica
� Efeito do aumento do número de electrões
Maior repulsão entre os electrões
Expansão da nuvem electrónica
Raio Atómico
d
� Raio atómico: é metade da distância entre dois núcleos de átomos (iguais) adjacentes.
Variação do raio atómico
� Ao longo do grupo o raio atómico aumenta, pois há um aumento do número de níveis de energia.
Aumento do raio atómico
� Ao longo do período o raio atómico diminui, pois os electrões encontram-se mais atraídos ao núcleo devido ao aumento da carga nuclear.
Raio iónico
Na Na+
Átomo
Ião positivo Átomo
Ião negativo
F F -
� O raio do catião é menor que o raio do átomo correspondente.
� O raio do anião é maior que o raio do átomo correspondente.
Espécies isoelectrónicas
� Espécies isoelectrónicas são espécies que possuem o mesmo número de electrões.
� O raio de espécies isoelectrónicas aumentacom a diminuição da carga nuclear.
12Mg2+11Na+9F
-8O2 -
r 8O2- > r 9F
- > r 10Ne > r 11Na+ > 12Mg
2+
10Ne
Variação da energia de ionização
Aumento da energia de ionização
� Ao longo do grupo a energia de ionização diminui, pois há um aumento do número de níveis de energia, o raio atómico aumenta.
� Ao longo do período a energia de ionização aumenta, pois os electrões encontram-se mais atraídos ao núcleo devido ao aumento da carga nuclear, o raio atómico diminui.