Proteínas
-
Upload
tulio-goncalves -
Category
Documents
-
view
612 -
download
4
Transcript of Proteínas

UNIVERSIDADE FEDERAL DO PARÁ
INSTITUTO DE CIÊNCIAS DA SAÚDE
FACULDADE DE FARMÁCIA
PROTEÍNAS E MÉTODO DE
DETERMINAÇÃO EM
ALIMENTOS
DISCIPLINA: BROMATOLOGIA
DOCENTE: ANA CRISTINAS BAETAS
DISCENTES: ALINE BARRETO
ALINNE LORRANY
TULIO GONÇALVES

Introdução
• O termo proteína deriva do grego protos, "que tem
prioridade", "o mais importante“;
• São consideradas as macromoléculas mais importantes das
células. E para muitos organismos, constituem quase 50% das
suas massas;
• São compostos orgânicos de estrutura complexa e massa
molecular elevada (de 5.000 a 1.000.000 ou mais unidades de
massa atómica);
• São sintetizadas pelos organismos vivos através da
condensação de um grande número de moléculas de alfa-
aminoácidos, através de ligações denominadas ligações
peptídicas;

Introdução
• São polímeros de aminoácidos - em suas moléculas
existem ligações peptídicas em número igual ao
número de aminoácidos presentes menos um;
• Os aminoácidos são monômeros dos peptídeos e das
proteínas;
• Polímeros são macromoléculas formadas pela união
de várias moléculas menores denominadas
monômeros;

Classificação
• PROTEÍNAS SIMPLES:
São homoproteínas, constituídas, exclusivamente por aminoácidos;
• PROTEÍNAS CONJUGADAS:
São heteroproteínas, são constituídas por aminoácidos mais outro componente não-proteico, chamado grupo prostético (Cromoproteínas, as Fosfoproteínas, as glicoproteínas, as lipoproteínas e as nucleoproteínas);
• PROTEÍNAS DERIVADAS:
Formam-se a partir de outras por desnaturação ou hidrólise (proteoses e as peptonas, formadas durante a digestão);

DEPENDENDO DO GRUPO
PROSTÉTICO: Proteínas conjugadas
Grupo prostético Exemplo
Cromoproteínas pigmento hemoglobina, hemocianina
e citocromos
Fosfoproteínas ácido fosfórico caseína (leite)
Glicoproteínas carboidrato mucina (muco)
Lipoproteínas lipídio encontradas na membrana
celular e no vitelo dos ovos
Nucleoproteínas ácido nucléico ribonucleoproteínas e
desoxirribonucleoproteínas

QUANTO À FORMA:
• Proteínas Fibrosas - são insolúveis nos solventes aquosos e possuem
pesos moleculares muito elevados. São formadas geralmente por longas
moléculas mais ou menos retilíneas e paralelas ao eixo da fibra;
• Proteínas Globulares - De estrutura espacial mais complexa, são mais
ou menos esféricas. São geralmente solúveis nos solventes aquosos e os
seus pesos moleculares situam-se entre 10.000 e vários milhões. Nesta
categoria situam-se as proteínas ativas como os enzimas,
transportadores como a hemoglobina, etc.

ESTRUTURA:
Os níveis de organização Molecular de uma proteína são:
• Primário - representado pela sequência de aminoácidos unidos
através das ligações peptídicas;
• Secundário - representado por dobras na cadeia (α - hélice), que são
estabilizadas por pontes de hidrogênio;
• Terciário - ocorre quando a proteína sofre um maior grau de
enrolamento e surgem, então, as pontes de dissulfeto para estabilizar
este enrolamento.
• Quaternário - ocorre quando quatro cadeias polipeptídicas se
associam através de pontes de hidrogênio, como ocorre na formação
da molécula da hemoglobina (tetrâmero).

REPRESENTAÇÃO ESQUEMÁTICA DOS NÍVEIS
DE ORGANIZAÇÃO MOLECULAR DE UMA
PROTEÍNA:

COMO SE FORMAM AS
PROTEÍNAS?
• A partir da união de muitos aminoácidos;
• Um organismo possui milhares de enzimas e todas
elas são todas proteínas com funções importantes;
• As informações genéticas, por exemplo, são
expressas através de proteínas;
• As proteínas podem ser constituídas por milhares de
aminoácidos que se adicionam uns aos outros através
da formação sucessiva de ligações deste tipo;

MECANISMO DE FORMAÇÃO DAS PROTEÍNAS, ATRAVÉS DA JUNÇÃO DE AMINOÁCIDOS.

Função da proteínas
• Estrutural ou plástica:
- Rigidez, consistência e elasticidade;
- Estruturais: colágeno, cartilagens, actina, miosina,
queratina, fibrinogênio, albumina.
• Hormonal:
- Função específica sobre órgão ou estrutura
- Insulina, glucagon;

Função da proteínas
• Energética:
- 100g de feijão possuem 21g de proteína;
- A necessidade diária de proteínas é de cerca de 1g/kg
durante essa fase e 0,8-0,9g/kg na fase adulta;
• Enzimática:
- Lipases, catalisar diferentes reações químicas;
• Condutoras de gases:
- Hemácias;
• Defesa:
- Anticorpos, fibrinogênio, trombina;

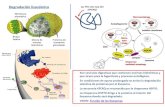
Digestão, absorção e metabolismo
• Estômago (ácido clorídrico) > desnaturação> pepsina (hidrólise) > enzimas do pâncreas (tripsina, quimotripsina, elastase e carboxipolipeptidase) > Aminoácidos transportados > fígado > fezes (1%);

Principais fontes
• Alto Valor Biológico:
Ex: Animal (Leite, ovos, carnes, pescados e derivados);
• Baixo Valor Biológico:
Ex: Vegetal (leguminosas e cereais integrais)

Sinais de deficiência
* Edema * Perda de cabelo * As linhas nas unhas * Redução da pigmentação * A perda de peso * Erupção cutânea * Pele escamosa * Constante sensação de letargia * Dor de músculo * A má cicatrização de feridas

Balanço nitrogenado
• 1) Equilibrado: Quando a quantidade de nitrogênio ingerido é igual a excretado. Ex.: adultos normais que não estão perdendo e nem aumentando músculos.
• 2) Negativo: Quando a quantidade de nitrogênio ingerido é menor que a excretado. Ex.: estado de jejum, dieta pobre em proteínas, dieta restritiva, doenças altamente catabólicas como câncer e AIDS, etc.
• 3) Positivo: Quando a quantidade de nitrogênio ingerido é maior que o excretado. Ex.: crianças (fase de crescimento), gestantes, treino de musculação com o objetivo de hipertrofia muscular, etc.

• Desnaturação da Proteína:
- Perda da função
• Patologias:
- DPE
- Marasmo
- Kwashiorko
- Deficiências enzimáticas natas

A dieta da proteína
• O que é?
• Estado de cetose
• Perigos:
- desidratação, hipoglicemia, vômitos, diarreia e dores
de cabeça, colesterol no sangue. Além disso, outros
efeitos foram observados, cálculo renal, infecções
recorrentes, hepatite, pancreatite aguda, anemia por
deficiência de ferro, podendo chegar até ao óbito.

Método de determinação –
Método de Kjeldahl
• Proposta por Kjeldahl em 1883, considerada
uma técnica confiável;
• Determinação de nitrogênio total;
• Possibilita a determinação direta de proteínas
em várias amostras biológicas;
• Decomposição de matéria orgânica, através da
digestão da amostra a 400° C;

- Materiais e equipamentos:
• Bloco digestor;
• Capela de exaustor de gases;
• Destilador de nitrogênio;
• Bureta automática;
• Agitador magnético;
• Erlenmeyr de 50ml;
• Balança analítica – precisão;
• Tubo de ensaio com borda
reforçada;
• Frascos dosadores de reagentes;
• Espátula;
• Papel impermeável;
- Reagentes e soluções;
• Ácido sulfúrico (H2SO4 – d=
1,84), p.a., concentrado;
• Hidróxido de sódio (NaOH) a 40%
(m/v);
• Sulfato de sódio (Na2SO4);
• Sulfato de cobre pentahidratado
(CuSO4.5H2O);
• Ácido clorídrico (HCl) 0,01 mol/L;
• Solução alcoólica de verde de
bromocresol, a 0,1% (m/v);
• Solução alcoólica de vermelho de
metila a 0,1% (m/v);
• Solução alcoólica de vermelho de
metila a 0,04% (m/v);
• Solução de ácido bórico, a 2%
(m/v);

1ª Etapa: Digestão

2ª Etapa: Destilação

3ª Etapa: Titulação

• Após a destilação:
Calcular o teor de nitrogênio total através da equação:
Onde:
NT – teor de nitrogênio total na amostra, em percentagem;
Va – volume da solução de ácido clorídrico gasto na titulação da amostra,
em mililitros;
Vb – volume da solução de ácido clorídrico gasto na titulação do branco, em
mililitros;
F – fator de correção para o ácido clorídrico 0,01 mol/L;
P1 – massa da amostra (em gramas).

Multiplicar o resultado pelo fator, obtendo assim
proteína bruta:
Fatores Alimentos
5,55 gelatina
5,70 pão frânces
5,74 pão doce, pão caseiro e pão de leite
5,75 PROTEÌNAS VEGETAIS
5,83 biscoitos, cevada, aveia e pão integral
6,25 PROTEÍNAS DA CARNE OU MISTURAS DE PROTEÍNAS
6,25 PROTEÍNAS DE SOJA E DE MILHO
6,38 PROTEÍNAS LÁCTEAS

OBRIGADO!!