Compostos de Coordenacao
Click here to load reader
-
Upload
amanda-eiriz-feu -
Category
Documents
-
view
217 -
download
2
description
Transcript of Compostos de Coordenacao
-
Prof. Daniela Barros de OliveiraQumica Inorgnica
COMPOSTOS DE COORDENAO OU COMPLEXOS
1- Definio e caractersticas gerais
Quando juntamos duas quantidades estequiomtricas de dois ou mais compostos
estveis, formam-se compostos de adio, como os seguintes exemplos:
KCl.MgCl2 (carnalita)
K2SO4 . Al2(SO4)3 . 24 H2O (almen de potssio)
CuSO4 . 4 NH3 . H2O (sulfato de tetramin-cobre II monohidratado)
Fe(CN)2 . 4 KCN (ferrocianeto de potssio)
Os compostos de adio pertencem a dois tipos: aqueles que perdem sua
identidade em soluo (sais duplos) e aqueles que mantm sua identidade (complexos).
Assim, quando se dissolve em gua a carnalita, a soluo mostra as propriedades dos
ons K+, Mg2+ e Cl-. De maneira semelhante, uma soluo de almen de potssio mostra
as propriedades dos ons K+, Al3+ e SO42-. Os dois casos so exemplos de sais duplos,
que s existem sob essa forma no estado cristalino.
Os dois outros exemplos de compostos de adio dados acima, quando
dissolvidos em gua, no formam ons simples, e sim ons complexos, que permanecem
intactos em soluo. Assim, o on [Cu(NH3)4(H2O)2]2+ e o on [Fe(CN)6]4- existem como
entidades distintas tanto no slido como em soluo.
Pode-se definir um composto de coordenao ou complexo como sendo um
composto formado por um tomo metlico (na quase totalidade dos casos, um metal de
transio) envolvido por tomos, molculas ou grupos de tomos, em nmero igual ou
superior ao estado de oxidao mais alto do metal (os ligantes so aqueles
representados dentro dos colchetes, junto com o metal). Um complexo pode ser um
ction, um nion ou um composto neutro. Veja alguns exemplos:
[Cu(H2O)2(NH3)4]2+ - O cobre, cujo Nox mais alto +2, tem 6 ligantes
coordenados
[Co(NO2)3(NH3)3] - O cobalto, cujo Nox mais alto +3, tem 6 ligantes
coordenados
1
-
Prof. Daniela Barros de OliveiraQumica Inorgnica
Para que um ligante possa participar de um complexo fundamental que esse
ligante possua pares eletrnicos disponveis para efetuar ligaes coordenadas. No
exemplo abaixo, molculas de amnia, que possuem um par de eltrons no-ligantes
capaz de formar uma ligao coordenada, esto ligadas ao tomo do metal:
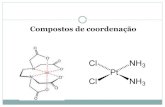
[Co(NH3)6]Cl3
Um conceito importante o de nmero de coordenao - o nmero de ligantes que
envolvem o tomo do metal. No caso do exemplo acima, o nmero de coordenao 6, pois
existem 6 molculas de amnia ligadas ao cobalto. Os ligantes representados fora dos
colchetes no fazem parte do nmero de coordenao.
2- Tipos de ligantes
Os ligantes podem apresentar mais de um tomo com disponibilidade eletrnica
para efetuar ligaes coordenadas. Assim, eles so classificados em
Monodentado - Possui apenas um tomo capaz de efetuar ligao
coordenada
Bidentado - Possui dois tomos capazes de efetuar ligao
coordenada
Tridentado - Possui trs tomos capazes de efetuar ligao
coordenada
Polidentado - Possui mais de trs tomos capazes de efetuar
ligao coordenada
Como exemplo de ligante bidentado, podemos citar o etilenodiamina (veja
abaixo). Perceba que a molcula pode fazer duas ligaes coordenadas, atravs de seus
dois tomos de nitrognio. No entanto, esse ligante s ser dito bidentado se os dois
2
-
Prof. Daniela Barros de OliveiraQumica Inorgnica
tomos de nitrognio forem utilizados em ligaes coordenadas. Se apenas um deles for
utilizado, ser dito monodentado.
Quando os dois nitrognios efetuam ligao coordenada para um mesmo tomo
metlico, o ligante dito quelante e o complexo pode ser chamado de quelato.
Quando cada um dos nitrognios efetua uma ligao coordenada para um tomo
metlico distinto (estes metais podem ser iguais ou diferentes), a ligao dita em
ponte.
3- Representao e nomenclatura
Via de regra, um composto de coordenao apresenta um metal de transio ao
qual se coordenam ligantes, que podem iguais ou diferentes. O complexo pode ser uma
espcie neutra ou um on (ction ou nion). A frmula qumica do complexo colocada
entre colchetes. Dentro dos colchetes escreve-se o smbolo do metal (tomo central) e
depois os seus ligantes, na seguinte ordem: ligantes negativos (aninicos) antes de
ligantes neutros (molculas). Ligantes positivos (catinicos) so muito raros, mas, caso
exista, dever ser escrito por ltimo, aps os demais ligantes. Veja o seguinte exemplo:
[CoCl2(NH3)4]+. O ligante cloreto (negativo) foi escrito antes do ligante amnia (neutro).
Para se dar nome a um complexo deve-se conhecer alguns nomes de ligantes
importantes. Quando espcies qumicas se encontram como ligantes de compostos de
coordenao, estes ligantes geralmente recebem nomes especiais. Veja:
3
-
Prof. Daniela Barros de OliveiraQumica Inorgnica
Ligantes Neutros:
Espcie Nome da espcie Nome do ligante
H2O gua aquo
NH3 amnio amin ou amino
CO Monxido de carbono carbonil
NO Monxido de nitrognio nitrosil
O2 oxignio dioxignio
N2 nitrognio dinitrognio
H2 hidrognio hidro
Outros ligantes:
Espcie Nome da espcie Nome do ligante
P(C6H5)3 trifenilfosfina trifenilfosfino (PPh3)*
NH2CH2CH2NH2 etilenodiamina etilenodiamino (en)
C5H5N piridina piridino (Py)
* O smbolo Ph representa o radical orgnico fenil
4
-
Prof. Daniela Barros de OliveiraQumica Inorgnica
Ligantes Aninicos:
Quando estes ons funcionam como ligantes, a terminao "ETO" substituda
por "O"
Espcie Nome da espcie Nome do ligante
F- fluoreto fluoro
Cl- cloreto cloro
Br- brometo bromo
I- iodeto iodo
CN- cianeto ciano
Oxinions:
Espcie Nome da espcie Nome do ligante
SO4- sulfato sulfato
CH3COO- acetato acetato
CH3COCHCOCH3- acetilacetonato acetilacetonato
C2O42- oxalato oxalato ou oxalo
Ligantes Ambidentados:
Estes ons so assim chamados porque podem se ligar ao metal de duas
maneiras, atravs de tomos diferentes.
Espcie Nome da espcie Ligante Nome do ligante
SCN- tiocianato - SCN- tiocianato
SCN- tiocianato - NCS- isotiocianato
5
-
Prof. Daniela Barros de OliveiraQumica Inorgnica
NO2- nitrito - ONO- nitrito
NO2- nitrito - NO2- nitro
Outros ligantes aninicos:
Espcie Nome da espcie Nome do ligante
H- hidreto hidrido
OH- hidrxido hidroxo
O2- xido oxo
O22- perxido peroxo
NH2- amideto amido
N3- nitreto nitreto
N3- azido azido
NH2- imido imido
Ligantes catinicos:
Espcie Nome da espcie Nome do ligante
NH4+ amnio amnio
H3NNH2+ hidraznio hidraznio
6
-
Prof. Daniela Barros de OliveiraQumica Inorgnica
2.1) Nomenclatura de complexos catinicos e neutros:
A nomenclatura dos complexos catinicos e neutros inicia-se pelo contra-on
(espcie representada fora dos colchetes), se houver, e depois escreve-se os nomes dos
ligantes, em ordem alfabtica. O nome deve ser inteiro, sem separao por espaos ou
hfens. Por ltimo coloca-se o nome do metal (tomo central), seguido pelo seu estado
de oxidao dentro do complexo. O nmero escrito em algarismos romanos e entre
parnteses. Quando existirem vrios ligantes iguais, usa-se o prefixo di, tri, tetra,
penta, hexa etc. No caso dos complexos catinicos, frequente o uso da palavra ON no
comeo do nome. Por exemplo: on tetraminodiclorocobalto (III). Porm, isso pode ser
omitido
O estado de oxidao do metal deve ser um valor tal que, somado s demais
cargas dos ligantes, resulte o valor da carga do complexo. Para determinar esse Nox
basta somar as cargas internas (ligantes dentro dos colchetes), considerando que os
ligantes neutros (molculas), logicamente, tm Nox igual a zero. Tambm fcil ver
que, quando um complexo tem frmula [XXX](SO4), por exemplo, a carga do complexo
s pode ser +2, j que o sulfato tem carga -2. Veja alguns exemplos:
[CoCl2(NH3)4]+ = Tetraminodiclorocobalto (III)
Nox do cobalto: Co + 2 Cl- + 4 NH3 = +1 Co -2 + 0 = +1 Co =
+3
[Co(NO2)(NH3)5] (NO3)2 = Nitrato de pentaminonitrocobalto (III)
Nox do cobalto: Co + NO2- + 5 NH3 = +2 Co -1 + 0 = +2 Co =
+3
[Ni(CO)4] = Tetracarbonilnquel (0)
Nox do nquel: Ni + 4 CO = 0 Ni + 0 = 0 Ni = 0
2.2) Nomenclatura de complexos aninicos:
A nomenclatura dos complexos aninicos feita da mesma forma, porm, o
metal acrescido da terminao "ATO". Veja alguns exemplos:
7
-
Prof. Daniela Barros de OliveiraQumica Inorgnica
[Ni(CN)4]2- = Tetracianoniquelato (II)
Nox do nquel: Ni + 4 CN- = -2 Ni -4 = -2 Ni = +2
[Fe(CN)6]3- = Hexacianoferrato (III)
Nox do ferro: Fe + 6 CN- = -3 Fe -6 = -3 Fe = +3
O complexo seguinte neutro, porm, foi colocado aqui porque o
formado por duas partes complexas, e uma delas um nion:
[Pt(Py)4] [PtCl4] = Tetracloroplatinato (II) de tetrapiridinoplatina
(II)
Nox da platina: 2 Pt + 4 Py + 4 Cl- = 0 2 Pt + 0 - 4 = 0 Pt = +2
2.3) Nomenclatura de complexos com ligantes em ponte:
Muitos complexos apresentam ligantes em ponte e a nomenclatura se torna um
pouco mais complexa e tambm o clculo do Nox dos metais associados a esses ligantes
pode ser mais trabalhoso. Normalmente usa-se a letra grega m (mi) para indicar um
ligante em ponte. Quando esse ligante (que chamaremos aqui de L) est ligado a partes
iguais (M - L - M), usa-se prefixos como bis, tris, tetraquis etc para indicar o nmero de
partes iguais existentes. Veja alguns exemplos:
8
-
Prof. Daniela Barros de OliveiraQumica Inorgnica
OBS: No primeiro exemplo h tambm um ligante quelante - o
dietilenodiamino
Veja a seguir outros exemplos:
[Cd(SCN)4] 2+ = Tetratiocianatocdmio (II)
[Zn(NCS)4] 2+ = Tetraisotiocianatozinco (II)
[(NH3)5Cr - OH - Cr(NH3)5] Cl5 = Cloreto de m -hidroxo -
bis[pentaminocromo (III)
H [Co(CO)4] = Tetracarbonilcobaltato (-I) de hidrognio
NH4 [Co(SO3)2(NH3)4] = Tetraaminodissulfitocobaltato (III) de
amnio
Cis - [PtCl2(Et3P)2] = Cis - diclorodi(trietilfosfino)platina (II)
[(NH3)5Cr - O2 - Cr(NH3)5] 4+ = m -peroxo - bis[pentaminocobalto
(III)
9