Curso BMP5748 Parasitologia Molecular Objetivos do curso Estrutura do curso:
Aula 2 Ligação e Estrutura Molecular
-
Upload
alvaro-galdos -
Category
Documents
-
view
34 -
download
0
Transcript of Aula 2 Ligação e Estrutura Molecular
-
Qumica Orgnica ILigao e Estrutura Qumica
Prof. Dr. Alvaro [email protected]
-
Objetivos de aprendizagem
Ao termino desta aula, o aluno deve ser capaz de:
Descrever os conceitos fundamentais daestrutura atmica.
Explicar vrios aspectos das ligaes qumicas.
Discutir a relevncia das ligaes qumicas nasmolculas dos frmacos e as interaes frmaco-receptor
-
tomos, elementos e compostos
O elemento bsico de toda matria.
TOMO
Conjunto de varias partculas subatmicas
Eltrons (Eletres) Prtrons (Protres) Nutrons (Neutres)
-
tomos, elementos e compostos
Prtrons (+)
Nutrons
Nuvem de Eltrons
O ncleo
pequeno
em relao
nuvem de
eltrons.
Eltrons
fora do
ncleo.
O numero decamadas que se
afastam mais do
ncleo.
Nveis diferentes deenergia
A camada mais externa a mais alta
-
tomos, elementos e compostos
C12
6
Numero de massa
(numero de prtons +
numero de nutrons)
Numero atmico (# de
prtons
Smbolo qumico
-
tomos, elementos e compostos
ELEMENTOS COMPOSTOS
So substancias que contm tomos de
apenas um tipo.
So substancias que se formam quando h unio de dois ou
mais elementos.
O2 N2
Cl2
NaCl
HCl
H2O
-
Estrutura Atmica: orbitais e configuraes eletrnicas
Localizao dos eltrons IMPORTANTE!!!
A organizao cria as ligaes entre ostomos.
Reaes qumicas destinam-se apenas a formarnovas ligaes.
Os eltrons participam nas ligaes qumicas ereaes do tomo, ocupando um orbital.
-
O que um orbital!!!
Regio do espao que pode conter doiseltrons.
Os eltrons no se movimentam, mas estolimitados a regies denominadas camadas
Tem subcamadas chamadas de orbitais atmicos
Camada pode conter at 2n2 eltrons
1 Camada 2 Camada 3 Camada
1s 2s 2p 3s 3p 3d1 orbital 1 orbital 3 orbitais 1 orbital 3 orbitais 5 orbitais
2 e- 8 e- 18 e-
-
Configurao eletrnica
a organizao do eltrons nos orbitais, subcamadase camadas.
VALNCIA: # de eltrons que um tomo deve perder ouganhar para alcanar a configurao eletrnica de um gsnobre
-
Configurao eletrnica
Na Ne2 8 1 2 8
e-
2 8 7 2 8 8
e-
Cl Ar
Grupo IA
Valncia 1
Grupo VIIA
Valncia 1
-
LIGAO QUMICA
Do espanhol Enlace qumico ou do ingls Chemistry bond.
Geometria molecular
O2 H2O
H2
C
Fe
FeO
CH4
Possam se
combinar
*Propriedades so
diferentes aos de seus
elementos
-
LIGAO QUMICA
Todas as ligaes qumicas originam-se comoresultado das atraes e repulses entre as cargaseltricas (lei de Coulumb-foras eltricas e leis damecnica quntica-movimentao e distribuio).
Para quebrar um a ligao qumica
Energia = varias dzias de Kcal/mol
Homem = Energia utilizada ENERGIA QUMICA
Substituio de ligaes qumicas Alimentos e nos combustveis
-
Porque se unem os tomos?
Por interesse!!!!
Pelo consumo mnimo de energia, ou seja,maior estabilidade.
LIGAES QUIMICAS exercem um efeito profunda nas propriedades fsicas e qumicas
das substncias.CO
Respirado
Liga-se fortemente a certas
substncias presentes nas
hemcias
Mineralizao e incapacidade de
transportar Oxignio (O2)
-
Na e- Cl
-
TEORIAS DAS LIGAES QUMICAS: FORMAO DE LIGAES QUMICAS
Obter configurao estvel.
Gs nobre (exceo do He: 2 e-)
Oito e-
Configurao eletrnica de valncia estvel
e- de camadas preenchidas eltron interno
e- de camadas no preenchidas eltron de valncia
Hoje mais utilizado os smbolos de Lewis!!!
Prof. Gilbert Newton Lewis (1875-1946)
Externo
-
PROPRIEDADES GERAIS DAS LIGAES QUMICAS
1. So foras da natureza: eltrica ou eletromagntica.
2. Participam os e- mais externos ou de valncia.
3. A eletronegatividade influi no comportamento dostomos.
4. Os tomos conservam sua identidade porque aestrutura do seus ncleos no alterada, emboragera substncias com propriedades diferentes.
5. Os tomos estados de energia mais estvelporque h diminuio da energia potencial.
6. Geram-se mudanas de energia.
-
ESTRUTURA DE LEWIS
Fornecem informaes sobre os tomos que estoligados entre si e o numero total de pares de eltronsparticipantes.
Prof. Lewis observou que muitos elementos eram maisestveis quando continham oito eltrons em suas camadasde valncia.
Eletronegatividade: a atrao que um tomo exerce sobreos eltrons em uma ligao qumica
Elementos < 8 valncias de e- se ligavam para compartilhar e- e completar suas camadas de valncia.
-
ESTRUTURA DE LEWIS
Para construir o smbolo de Lewis para um elementoescrevemos seu smbolo qumico cercado por umnumero de pontos (ou de x ou crculos, etc).
C
.... H. Cl
.......GRUPO I-A II-A III-A IV-A V-A VI-A VII-A
Smbolo .X .X .X .X .X .. .. .
...... . . ..X...
..X....
-
ESTRUTURA DE LEWIS
Qual o smbolo Lewis do Germnio? (z=32)
Qual o smbolo Lewis do Zinco? (z=30)
Qual o smbolo Lewis do Sdio? (z=11)
-
ESTRUTURA DE LEWIS
Representar a formula do CH3F(fluorometano)
-
Vrios tipos de ligaes qumicas
Um tomo que ganhe e- nion (on negativo)
Um tomo que ganhe e- ction (on positivo)
Os metais tendem a perder e-
Os no metais tendem a ganhar e-
O tamanho dos tomos diminui de esquerda paradireita e aumenta de cima para baixo ao longo de umgrupo.
mais fcil acrescentar do que remover eltrons, retirar eltrons requer uma grande quantidade de energia
-
LIGAES INICAS (eletrovalente)
a transferncia de um ou mais e- entre tomos
Li F Li FTransferncia
de eltrons
O mais eletronegativo ganha eltrons: NIONO menos
eletronegativo ganha eltrons: CTION
-
LIGAES INICAS
Estabelea as ligaes inicas do NaCl
Estabelea as ligaes inicas do K2O
-
PROPRIEDADES DO COMPOSTOS INICOS
A temperatura ambiente so slidos cristalinos.
Elevado ponto de fuso e ebulio.
A atrao inica bidirecional.
Apresentam-se como condutores eltricos quandofundidos ou em dissoluo.
Os compostos inicos so um metal + no metal.
So tambm compostos inicos os formadossomente por no metais (NH4 e NO3)
A maioria dos compostos inicos so solveis emgua.
-
PROPRIEDADES DO COMPOSTOS INICOS
CTION NOME NION NOME
Na+1 Sdico F-1 Fluoreto
K+1 Potssico Cl-1 Cloreto
Mg+1 Magnsico S= Sulfeto
Ca+2 Clcico Br-1 Brometo
NH4-1 Amnio CO3= Carbonato
-
LIGAES COVALENTES
o compartilhamento de e- entre tomos
tomos iguais.
No h formao de ons.
A fora de ligao resulta da atrao entre este eltronscompartilhados e os ncleos positivos dos tomos queparticipam da reao.
-
LIGAES COVALENTES: polares e apolares
A maioria da ligaes nas molculas, principalmentenos medicamentos so do tipo covalente.
POLARESCompartilhamento desigual de eltrons (e-) entre dois
tomos
APOLARESCompartilhamento igual de
eltrons (e-) entre dois tomos
Cl......
H. .
H..H
-
LIGAES COVALENTES: polares e apolares
A polaridade da ligao medida pelo momentodipolo
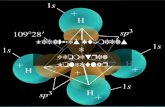
HIBRIDIZAO: Superposio de orbitais atmicosgerando orbitais hbridos.
Sigma () Pi ()
* Nunca ocorre sozinho, sem
presena do sigma
-
ELETRONEGATIVIDADE E LIGAO QUMICA
a capacidade que tem um tomo ligado a um ou mais tomos de atraireltrons fortemente em sua direo.
-
Energia de dissociao das ligaes HOMOLISE E HETEROLISE
UNIO DE ATOMOS
SEPARAO DE ATOMOS
Liberam energia
Consumem energia
Energia de dissociao da ligao (D)
Dissociao D (Kj/mol)
CH4 CH3 + H D (CH3 H) 435
CH3 CH2 + H D (CH2 H) 444
CH2 CH + H D (CH H) 444
CH C + H D (C H) 339
-
Ciso Homoltica e Heteroltica
Ciso: dissociar molculas
HOMLISE Os dois tomos que
constituem a ligaocovalente, cada um vai paraseu fragmento
A : B A + B. .
Energia de dissociaes de ligaes
homolticas
HETERLISE Na qual os dois eltrons da
ligao vo para o mesmofragmento
A : B A + B..
Energia de dissociaes de ligaes
heterolticas
-
POLARIDADE
Polaridade das ligaes: quando eltronscompartilhados entre dois tomos no sonecessariamente compartilhados com igualdade.
N, O e halognios (Cl, F, I, Br) so mais eletronegativos queo C, por tanto vai ter cargas negativas parciais.
H:H
H H. .
+
H:F
H F. .
+
+ -
LIGAO POLARLIGAO APOLAR
-
Polaridade de ligaes
LIGAES POLARES
tomos de diferentes tendncias para atrair eltrons
ELETRONEGATIVIDADE
Polaridade = Diferencia de eletronegatividade
-
ELETRONEGATIVIDADE
-
ELEMENTOS MAIS USADOS NA QUMICA ORGNICA
F O Cl, N Br C, H
-
Conceitos e usos
A polaridade influencia fortemente as propriedadefsicas e qumicas.
Influencias sobre o p. f. / p. e.
Solubilidade.
A polaridade de uma ligao determina:
Reao em que pode participar.
Reatividade das ligaes vizinhas.
-
Polaridade da ligao e foras intermoleculares
Interaes dipolo-dipolo: interao entre umaextremidade positiva e outra negativa
Foras de Van Der Waals (foras de London): soforas de atrao relativamente fracas entremolculas apolares (alcanos: isobutano e butano)
Ligao de hidrognio: a fora de atrao entre ohidrognio fixado a um tomo eletronegativo de umamolcula e um tomo eletronegativo da mesmamolcula (intramolecular) ou de uma molculadiferente (intermolecular).
-
POLARIDADE
Polaridade das molculas: uma molcula ser polarse o centro de carga negativa no coincidir com ocentro de carga positiva.
Momento dipolo: diferena entre eletronegatividades
-
Significado da ligao qumica nas interaes frmaco-receptor
Como interagem os frmacos?
Receptores localizados nas macromolculas.
Reconhecimento do sinal qumico Ligante.
Para obter o feito desejado?
O frmaco tem que se ligar a 3 pontos do receptor
Frmacos que no precisam de receptores?
Superfcie externa da pele
Trato gastrointestinalAtuam por meio de
interaes qumicas.
Neutralizao do cido gstrico por anticidos
-
Significado da ligao qumica nas interaes frmaco-receptor
Diversos tipos de ligaes qumicas.
FARMACO + RECEPTOR COMPLEXO FARMACO-RECEPTOR FUNO ALTERADA
Ligaes Energia
Interaes covalentes 40-140 Kcal/mol
Inicas 10 Kcal/mol
on-dipolo 1-7 Kcal/mol
Dipolo-dipolo 1-7 Kcal/mol
Van der Waals 0,5-1 Kcal/mol
Ligao de hidrognio 1-7 Kcal/mol
Interaes hidrofbicas 1 Kcal/mol
-
Significado da ligao qumica nas interaes frmaco-receptor
Os frmacos mais uteis ligam-se por meio deligaes fracas INICAS E MAIS FRACAS.
INTERAO FRMACO-RECEPTOR IRREVERSVEL
Ligaes covalentes so forte e irreversveis
Mitomicina C Antramicina Cis-platina
Interferem com a funo do DNA
Mitomicina C Cis-platinaDNA (guanina)
-
Bibliografia
Solomons, TWG. QUMICA ORGNICA,2005.
McMurry, J. QUMICA ORGNICA, 2005.
Morrison, RT. QUMICA ORGNICA, 1996.
Barbosa, LCA. INTRODUO QUMICA ORGNICA, 2004.
Allinger, N. QUMICA ORGNICA, 2009.