ANA CAROLINA PONTES DE MIRANDA MARANHÃO hematológico de... · Para a realização da contagem...
Transcript of ANA CAROLINA PONTES DE MIRANDA MARANHÃO hematológico de... · Para a realização da contagem...

0
CENTRO UNIVERSITÁRIO CESMAC
ANA CAROLINA PONTES DE MIRANDA MARANHÃO
PERFIL HEMATOLÓGICO DE FRANGOS DE CORTE DE CRIAÇÃO INDUSTRIAL DO AGRESTE ALAGOANO
MACEIÓ-AL 2017/02

1
ANA CAROLINA PONTES DE MIRANDA MARANHÃO
PERFIL HEMATOLÓGICO DE FRANGOS DE CORTE DE CRIAÇÃO INDUSTRIAL DO AGRESTE ALAGOANO
Trabalho de Conclusão de Curso apresentado como requisito final para conclusão do curso de Medicina Veterinária do Centro Universitário Cesmac, sob a orientação da professora Dra. Isabelle Vanderlei Martins Bastos e coorientação do Médico Veterinário Dr. Felipe José Feitoza Bastos.
MACEIÓ-AL 2017/02

2
ANA CAROLINA PONTES DE MIRANDA MARANHÃO
PERFIL HEMATOLÓGICO DE FRANGOS DE CORTE DE CRIAÇÃO INDUSTRIAL DO AGRESTE ALAGOANO
Trabalho de Conclusão de Curso apresentado como requisito final para conclusão do curso de Medicina Veterinária do Centro Universitário Cesmac, sob a orientação da professora Dra. Isabelle Vanderlei Martins Bastos e coorientação do Médico Veterinário Dr. Felipe José Feitoza Bastos.
APROVADO EM: 21 / 11 / 2017
Orientadora - Profa. Dra. Isabelle Vanderlei Martins Bastos
BANCA EXAMINADORA
Profa. Ma. Cláudia Alessandra Alves de Oliveira
Profa. Ma. Muriel Magda Lustosa Pimentel

3
AGRADECIMENTOS
Agradeço a todas as instituições que tornaram possível a minha formação
profissional, ao Centro Universitário Cesmac, à Agroceres Multimix- Nutrição Animal, pela
oportunidade e conhecimentos adquiridos, e por essa família que vou levar comigo, em
especial meus supervisores Fernando Augusto de Souza e Erika Lara pelos ensinamentos,
conselhos e amizade. Aos meus colegas de estágio, líderes de setores e auxiliares de
pesquisa da empresa, aprendi muito com eles e vivi momentos memoráveis que irei levar
para sempre.
Aos meus orientadores de TCC, a prof. Dra. Isabelle Vanderlei Martins Bastos e ao
Dr. Felipe José Feitosa Bastos pelo apoio, cuidado e carinho na condução e construção de
todo esse projeto, sem eles tenho certeza de que não teria chegado até aqui. A eles meu
eterno agradecimento e admiração.
À Silmara Raquel e Keven Djalma, que foram meus braços direito e esquerdo nas
coletas e processamento dos exames, sem eles (juntamente com a prof. Dra. Isabelle) as
noites de processamento não teriam sido possíveis. Sem esquecer os técnicos de
laboratório que tanto ajudaram na preparação dos exames, são eles Rubmery, Leandro e
Maria de Fátima.
Aos queridos professores que não participaram diretamente na construção deste
trabalho, mas que tanto somaram à minha formação. São eles Eduardo Melo, Marcelo
Araújo, Gilsan Aparecida, Giovana Patrícia, Roberto Rômulo, Muriel Pimentel, Alice Oliveira,
Cláudia Oliveira, Isaac Albuquerque e todo o corpo docente do Centro Universitário Cesmac.
Aos meus amigos que sempre estavam ali para me apoiar nas boas e más decisões
ao longo do curso, Natalia Borsato, Fabiano Rocha, Arthur Carlos, Raquel da Silva, Nilson
Tenório e Bruna Higino. Os amigos e colegas que me ajudaram nessa caminhada são
incontáveis e tiveram sua participação especial em cada momento da graduação, todos
guardados em minha memória e coração.
E por último à minha família, meus pais Carlos Ernesto e Carol, meu irmão Pedro, à
Alice e ao Lucas, meus avós e meus tios que sempre me incentivaram e acreditaram que
este projeto se tornaria realidade. Obrigada por abraçarem a ideia da área que eu pretendo
seguir sem me desencorajar em nenhum momento com as barreiras que surgirão pelo
caminho. Tenho certeza de que é só o começo de uma bela caminhada na profissão e eu
devo todas as minhas conquistas a vocês.

4
PERFIL HEMATOLÓGICO DE FRANGOS DE CORTE DE CRIAÇÃO INDUSTRIAL DO AGRESTE ALAGOANO
HEMATOLOGICAL PROFILE OF BROILER CHICKENS IN INDUSTRIAL CREATION OF ALAGOAS
Ana Carolina Pontes de Miranda Maranhão
Graduanda do Curso de Medicina Veterinária do Centro Universitário Cesmac [email protected]
Isabelle Vanderlei Martins Bastos Professora Doutora do Curso de Medicina Veterinária do Centro Universitário Cesmac
[email protected] Felipe José Feitoza Bastos
Médico Veterinário Doutor em Biociência pela UFRPE [email protected]
RESUMO A avaliação hematológica é um importante instrumento no monitoramento da saúde das aves, constituindo-se num ponto de partida para um diagnóstico rápido e preciso principalmente para frangos de corte, que apresentam altos níveis zootécnicos na produção e estes níveis estão intimamente relacionados com a saúde destas aves. No entanto, no Brasil, esses valores são pouco estudados, o que pode acarretar em erros na interpretação dos resultados obtidos. Dessa forma, objetivou-se avaliar o perfil hematológico de frangos de corte de criação industrial do Agreste Alagoano, comparando os valores hematológicos em diferentes fases de criação (pré-inicial, inicial, crescimento e final) e entre machos e fêmeas. Foram coletadas amostras sanguíneas de 10 aves em cada idade, em dois galpões de uma granja, totalizando 80 animais. Foram determinados valores de eritrócitos, hematócrito, hemoglobina, hemoglobina globular média (HCM), concentração de hemoglobina globular média (CHCM) e volume globular médio (VCM), trombócitos, proteína plasmática total (PPT), fibrinogênio plasmático, leucócitos totais, linfócitos, heterófilos, monócitos, basófilos e eosinófilos. Os resultados evidenciaram que os valores de eritrócitos, hemoglobina, índices hematimétricos e trombócitos apresentaram-se divergentes aos da literatura, enquanto que o hematócrito, PPT, fibrinogênio e leucócitos foram semelhantes. Em relação a idade, notou-se um aumento progressivo dos valores nas aves mais velhas, e quanto as diferenças entre o sexo, estas não foram significativas. Com este trabalho conclui-se que a avaliação hematólogica de frangos de corte é importante para o monitoramento da sanidade aviária, havendo a necessidade de maiores estudos com padronização de técnicas e valores de referência.
PALAVRAS-CHAVE: Frango de corte. Hematologia aviária. Hemograma.
ABSTRACT Hematological evaluation is an important instrument in the monitoring of poultry health, constituting a starting point for a quick and precise diagnosis, especially for broiler chickens, which present high zootechnical levels in production and these levels are directly related to the health of these birds. However, in Brazil, these values are little studied, which can lead to errors in the interpretation of the results obtained. The objective of this study was to evaluate the hematological profile of broilers of Alagoas, comparing the hematological values in different breeding phases (pre-initial, initial, growth and final) and between males and females. Blood samples were collected from 10 animals at each age, in two barns on a farm, totaling 80 animals. The values of erythrocytes, hematocrit, hemoglobin, mean globular hemoglobin (HCM), concentration of mean globular hemoglobin (CHCM) and mean globular volume (MCV), thrombocytes, total plasma protein (PPT), plasma fibrinogen, total leukocytes, lymphocytes, heterophiles, monocytes, basophils and eosinophils. The results showed that the values of erythrocytes, hemoglobin, hematimetric indexes and thrombocytes were different from those in the literature, whereas hematocrit, PPT, fibrinogen and leukocytes were similar. In relation to age, there was a progressive increase of values in older animals, and the differences between sex were not significant. This study concludes that hematological evaluation of broiler chickens is important for the monitoring of avian health, and there is a need for further studies with standardization of techniques and reference values.
KEY-WORDS: Broiler chicken. Avian hematology. Hemogram.

5
SUMÁRIO
1 INTRODUÇÃO ......................................................................................................... 6
2 MATERIAL E MÉTODO ........................................................................................... 7
2.1 Tipo e local de estudo ......................................................................................... 7
2.2 Amostra ................................................................................................................ 7
2.3 Seleção dos Animais........................................................................................... 8
2.4 Procedimentos .................................................................................................... 8
3 RESULTADOS E DISCUSSÃO ............................................................................. 10
4 CONCLUSÃO ........................................................................................................ 18
REFERÊNCIAS ......................................................................................................... 19
ANEXO - PARECER DO CEUA ...............................................................................21

6
1 INTRODUÇÃO
A avicultura consolidou-se como uma das mais importantes e eficientes
atividades da agropecuária brasileira, o que levou o Brasil a transformar-se no maior
exportador mundial de carne de frango. Inicialmente concentrada nas regiões Sul e
Sudeste, a atividade vem se espalhando pelo território nacional, aproximando-se
não só das regiões produtoras de matérias-primas, como é o caso do deslocamento
de criatórios e abatedouros para a região Centro-Oeste, mas também das regiões
consumidoras, o que explica em parte o seu crescimento na Região Nordeste
(EVANGELISTA; NOGUEIRA FILHO; OLIVEIRA, 2008).
Frangos de corte apresentam altos níveis zootécnicos na produção e estes
níveis estão intimamente relacionados com a saúde destas aves. Assim, o sistema
imunológico destes animais necessita atuar adequadamente e de maneira eficiente,
possibilitando um bom desempenho produtivo, impedindo a introdução de doenças
na criação (MORGULIS, 2002).
Dessa forma, as provas laboratoriais do sangue podem servir como
ferramentas importantes para auxiliar no monitoramento da saúde das aves, no
diagnóstico de doenças e também para avaliação pré-operatória, tratamento e das
condições de saúde do organismo (VOIGT, 2003).
A hematologia serve para monitorar a saúde geral do animal e avaliar sua
capacidade para transportar oxigênio e defender-se contra os agentes infecciosos
(VOIGT, 2003), orientando o profissional no estabelecimento de prognóstico e
protocolos terapêuticos para diferentes enfermidades. No entanto, para que seja
convenientemente utilizado, há necessidade do conhecimento da fisiologia padrão
nas diferentes espécies em suas respectivas regiões (CORDEIRO, 2003). Embora
sozinho o hemograma constitua recurso de diagnóstico limitado na maioria dos
casos, ele estabelece um ponto de partida para o diagnóstico rápido e preciso, e é o
exame de primeira linha no estudo da função hematológica (REBAR, 2003;
GONZÁLEZ; SANTOS, 2005).
A principal diferença entre aves e mamíferos é que as aves apresentam os
eritrócitos e os trombócitos nucleados, fato que pode interferir nas contagens
automatizadas. Além disso, o principal leucócito nas aves é o heterófilo, equivalente
ao neutrófilo dos mamíferos. Deste modo, as contagens automáticas de rotina
realizadas em mamíferos não são aplicáveis nas aves, sendo indicadas as técnicas

7
manuais (CAPITELLI; CROSTA, 2013). Para a realização da contagem manual
utiliza-se o hemocitômetro (câmara de Neubauer) que é preenchido com a amostra
diluída de sangue (CAMPBELL, 1994).
No Brasil, os clínicos veterinários utilizam como valores de normalidade do
hemograma e bioquímica sanguínea aqueles estabelecidos em outros países, onde
o clima, região, nutrição e manejo diferem dos encontrados no país, podendo assim,
acarretar em erros na interpretação dos resultados obtidos. Possivelmente em
decorrência desses fatos, os valores médios e os limites superiores e inferiores
detectados por vários autores são bastante variáveis (BORSA, 2009).
Tendo em vista estes fatos, e diante da escassez de estudos publicados
sobre hematologia em frangos de corte no Brasil, o seguinte trabalho visou avaliar o
perfil hematológico de frangos de corte de criação industriais do Agreste Alagoano,
em diferentes fases de criação (pré-inicial, inicial, crescimento e final) e entre
machos e fêmeas, através da pesquisa hematológica, servindo de embasamento
para clínicos, produtores e futuros trabalhos, bem como melhorando a qualidade de
vida dos animais das criações e para gerar mais lucro final para os proprietários.
2 MATERIAL E MÉTODO
2.1 Tipo e local de estudo
Foi realizado um estudo observacional descritivo transversal, a partir da coleta
de amostras sanguíneas de frangos de corte, em uma granja de criação industrial do
Agreste Alagoano (Arapiraca). As amostras coletadas foram processadas no
Laboratório de Análises Clínicas, da Clínica Escola de Medicina Veterinária, do
Centro Universitário Cesmac, em Marechal Deodoro, Alagoas.
2.2 Amostra
Foram coletadas amostras sanguíneas, através da veia ulnar de 80 frangos de
corte, sendo 50% fêmeas e 50% machos, pertencentes a linhagem comercial Cobb,
e apresentando-se no final das fases de criação pré-inicial (07 dias), inicial (21 dias),
crescimento (35 dias) e final (49 dias). Estas aves foram escolhidas de forma
aleatória ao longo de dois galpões da mesma granja.

8
2.3 Seleção dos Animais
Foram incluídas amostras sanguíneas de frangos de corte de mesma
linhagem comercial (Cobb), hígidas, apresentando-se no final de cada fase de
criação: pré-inicial (07 dias), inicial (21 dias), crescimento (35 dias) e final (49 dias).
Foram excluídas amostras de aves que apresentavam sintomatologia de
alguma enfermidade e as que não se encaixavam na idade referida.
2.4 Procedimentos
Em cada galpão, foram coletadas amostras sanguíneas de 10 aves para cada
fase de criação: pré-inicial, inicial, crescimento e final, sendo cinco machos e cinco
fêmeas, escolhidos aleatoriamente, totalizando 40 aves por galpão e 80 na granja.
Este procedimento foi realizado junto ao responsável técnico pela granja sempre por
volta das 8 horas da manhã.
Inicialmente, as aves escolhidas foram submetidas a um exame clínico
padrão, observando-se o escore corporal, estado geral, aspecto de mucosas e
cavidades naturais exploráveis; aspecto das excreções (fezes e urina) e presença de
ectoparasitas. As aves que não se apresentaram hígidas não foram incluídas nesta
pesquisa.
Em seguida, as amostras sanguíneas foram coletadas da veia ulnar, após a
desinfecção do local com algodão embebido de uma mistura de álcool e iodo. Foram
utilizadas seringas descartáveis de 3 ml com agulhas 20x5,5mm para os animais
com as idades 07 e 21 dias, e com agulhas 25x7mm para as aves com 35 e 49 dias,
fazendo a transferência de uma gota do sangue para lâminas de vidro para a
confecção imediata dos esfregaços sanguíneos, que foram corados pelo corante
rápido para hematologia (Panótico). Em seguida, as amostras foram acondicionadas
em microtubos de 0,5 ml, contendo EDTA; e armazenadas em caixa isotérmica com
gelo reciclável, para serem encaminhadas para o laboratório, para posterior
processamento.
A contagem total de eritrócitos e de leucócitos foi realizada em câmara de
Neubauer (hemocitômetro), utilizando amostra de sangue diluída a 1:200, em
corante de Natt e Herrick’s (THRALL et al., 2003).

9
A dosagem de hemoglobina foi efetuada pelo método cianometahemoglobina,
utilizando kit comercial Labtest®, com leitura em espectrofotômetro (modelo BIO200,
BIOPLUS), seguindo as instruções do fabricante. No entanto, os núcleos livres
obtidos após a diluição e lise dos eritrócitos foram separados, centrifugando-se a
mistura reagente cianometemoglobina/sangue a 1500 rpm por 5 minutos antes da
leitura da densidade óptica do sobrenadante para evitar concentração
superestimada de hemoglobina (THRALL et al., 2003).
A determinação do hematócrito ou volume globular se deu através do método
do microhematócrito, utilizando-se tubo capilar centrifugado a 1500 rpm por 5
minutos, sendo os resultados estimados em porcentagem através de tabelas
específicas de microhematócrito, segundo Jain (1986).
Posteriormente, a contagem diferencial leucocitária foi realizada em esfregaço
sanguíneo, sob óleo de imersão (objetiva de 100x). Foram determinados valores
relativos e absolutos de linfócitos, heterófilos, eosinófilos, monócitos e basófilos.
Adicionalmente, foi realizada a contagem indireta de trombócitos em 1.000
eritrócitos. O resultado obtido foi multiplicado pelo número de eritrócitos e dividido
por 1.000, obtendo o valor estimado de trombócitos por microlitro de sangue
(CAMPBELL, 1994). No esfregaço sanguíneo ainda foi analisado a morfologia dos
eritrócitos, dos leucócitos e dos trombócitos.
A partir dos dados obtidos no hemograma, foram calculados os seguintes
índices hematimétricos de Wintrobe: hemoglobina globular média (HCM) que é o
peso da hemoglobina no eritrócito, concentração de hemoglobina globular média
(CHCM) que é a concentração da hemoglobina dentro de cada eritrócito e volume
globular médio (VCM), que representa o tamanho dos eritrócitos. Os cálculos desses
índices foram realizados utilizando as fórmulas a seguir (THRALL et al., 2003):
VCM (fL) = (Hematócrito x 10) / Eritrócitos
HCM (pg) = (Hemoglobina x 10) / Eritrócitos
CHCM (%) = (Hemoglobina x 100) / Hematócrito
As proteínas plasmáticas totais foram determinadas pelo método de
refratometria, do mesmo modo que o fibrinogênio plasmático, seguindo a técnica de
precipitação térmica, em banho-maria a 57ºC, segundo Jain (1986).
Para a análise estatística, os dados foram tabulados em planilha EXCEL para
análise simples. Foram calculadas as médias para cada parâmetro avaliado em
cada fase estudada.

10
Este projeto foi submetido à Comissão de Ética no Uso de Animais do Centro
Universitário Cesmac (CEUA/CESMAC), obtendo parecer aprovado sob registro nº
14A 2017 (ANEXO 1).
3 RESULTADOS E DISCUSSÃO
O resultado da avaliação hematológica das aves estudadas encontra-se nas
Tabelas 1 e 2, onde os valores foram obtidos de acordo com as médias calculadas
por idade e por sexo. Na Tabela 1, podemos observar no eritrograma, que a média
dos valores, por idade, de eritrócitos e de hemoglobina encontram-se abaixo dos
valores para a mesma linhagem apresentados por Bournous e Stedman (2000) e
Samour (2006). Esse resultado também foi inferior a média encontrada por Furlan et
al. (1999), para frangos de corte da linhagem Cobb, a mesma deste estudo.

11
Tabela 1: Médias dos valores hematológicos de frangos de corte com 7, 21, 35 e 49 dias, demonstrando sexo, valores numéricos de eritrócitos (Eri), hematócrito (Ht), hemoglobina (Hb), volume corpuscular médio (VCM), hemoglobina corpuscular média (HCM), concentração de hemoglobina corpuscular média (CHCM), proteína plasmática total (PPT), fibrinogênio plasmático (FP) e trombócitos (Trom).
Idade Eri Ht Hb VCM HCM CHCM PPT FP Trom 106/ μl % g/dl fl pg % g/dl mg/dl μl
07 dias (Fêmeas)
1,71 28 5,4 174,32 33,49 18,98 3,7 180 118.760
07 dias (Machos)
2,02 27 5,6 156,53 31,62 20,42 3,6 150 259.405
MÉDIA 07 dias 1,86 28 5,5 165,43 32,55 19,70 3,6 160 189.083
21 dias (Fêmeas)
2,13 29 6,2 146,04 31,68 21,23 3,7 190 163.353
21 dias (Machos)
2,21 30 6,3 142,23 30,13 21,05 3,6 170 178.385
MÉDIA 21 dias 2,17 29 6,3 144,14 30,91 21,14 3,6 180 170.869
35 dias (Fêmeas)
1,93 28 6,7 203,54 43,91 21,27 3,9 360 133.872
35 dias (Machos)
1,98 33 7,0 225,96 48,77 21,29 3,9 220 160.448
MÉDIA 35 dias 1,96 32 6,8 214,75 46,34 21,28 3,9 290 147.160
49 dias (Fêmeas)
1,08 28 6,1 297,94 64,54 21,58 4,2 250 78.372
49 dias (Machos)
1,22 29 6,1 243,11 51,43 22,15 3,9 230 93.962
MÉDIA 49 dias 1,15 28 6,1 270,53 57,98 21,86 4,0 250 86.167
Fonte: Dados da pesquisa. Tabela 2: Médias dos valores hematológicos de frangos de corte com 7, 21, 35 e 49 dias, demonstrando sexo e valores numéricos de leucócitos totais (Leu), e valores absolutos de heterófilos (Het), linfócitos (Linf), monócitos (Mon), eosinófilos (Eos) e basófilos (Bas).
Idade Leu Het Linf Mon Eos Bas μl μl μl μl μl μl
07 dias (Fêmeas)
1.905 472 584 583 214 39
07 dias (Machos)
2.250 566 556 707 337 92
MÉDIA 07 dias 2.077 519 570 645 276 62
21 dias (Fêmeas)
4.245 1.147 878 1.308 668 168
21 dias (Machos)
3.815 1.010 896 1.178 578 152
MÉDIA 21 dias 4.030 1.078 887 1.243 586 160
35 dias (Fêmeas)
11.260 3.739 1.510 3.581 1.103 412
35 dias (Machos)
9.665 3.309 2.061 3.358 1.040 289
MÉDIA 35 dias 10.251 3.524 1.786 3.469 1.229 350
49 dias (Fêmeas)
18.960 7.734 2.990 4.674 2.164 609
49 dias (Machos)
26.510 12.655 3.343 6.316 2.790 853
MÉDIA 49 dias 22.735 10.194 3.167 5.495 2.477 731
Fonte: Dados da pesquisa.

12
Para o hematócrito, foram observados valores que corroboram os achados de
Bournous e Stedman (2000), que encontraram resultados de 22 a 35%, no entanto,
foram inferiores aos de Samour (2006), com percentuais de 30 a 49%. A variação
nos valores de eritrócitos, hematócrito e hemoglobina pode ter sido influenciada
pelas diferentes idades das aves, uma vez que os valores dos autores acima citados
são em aves adultas. Consequentemente, os índices hematimétricos VCM, HCM e
CHCM também se apresentaram discordantes da literatura pesquisada. Samour
(2006) demonstrou valores para estes índices, respectivamente, 104 a 135 fl, 32 a
43,9 pg e 30,2 a 36,2%. Comparando ainda, estes índices aos dos mamíferos, os
valores de HCM e VCM nas aves são maiores que os dos mamíferos, pois os
eritrócitos são maiores também. Contrariamente, o CHCM é menor devido à
presença do núcleo (CAPITELLI; CROSTA, 2013).
As proteínas plasmáticas no sangue são importantes para detectar processos
inflamatórios graves (CHARLES NORIEGA, 2000). As médias da proteína
plasmática total (PPT) e do fibrinogênio plasmático (Tabela 1) encontram-se de
acordo com o observado na literatura, cujos valores observados por Samour (2006)
para este último foi de 130 a 410 mg/dl. Para as proteínas, Silva et al. (2007)
verificou valores de 3 a 6 g/dl para aves. No entanto, Zhou e Yamamoto (1998)
descrevem uma média de proteína plasmática de 3,2 g/dl para frangos submetidos
ao estresse pelo calor (expostos a temperaturas ambientais de 30ºC). As coletas
deste estudo foram realizadas nos meses de março e abril do corrente ano, e nestas
ocasiões, a temperatura na granja apresentava-se acima de 30ºC. Temperaturas
mais elevadas podem provocar nos animais expostos uma diminuição da
viscosidade total do sangue, do hematócrito e do volume extracelular, quando
comparados a frangos mantidos em temperaturas mais frias (ZHOU; YAMAMOTO,
1998).
Os valores observados na contagem indireta de trombócitos (Tabela 1)
apresentaram-se elevados quando comparados com os verificados por Bournous e
Stedman (2000), 20.000 a 30.000/ μl, e Samour (2006), 3.000 a 33.000/ μl. A
trombocitose tem sido observada em situações de inflamações crônicas (MITCHELL;
JOHNS, 2008). Estas células, além de participarem do processo de coagulação
sanguínea, também tem uma importante função de defesa do organismo destes
animais (BOURNOUS; STEDMAN, 2000), pois apresentam capacidade fagocitária 2
a 3 vezes mais rápida que os heterofilos e monócitos (CHARLES NORIEGA, 2000),

13
o que pode justificar os achados deste trabalho já que as idades mais jovens são
mais desafiados imunologicamente.
Em relação às idades, os valores observados na Tabela 1 eram menores nos
animais mais jovens, aumentando progressivamente nos animais mais velhos, com
exceção dos animais de 49 dias, que apresentaram valores mais baixos. Já na
Tabela 2, os valores dos leucócitos demonstram bem essa progressão entre as
idades. Cardoso e Tessari (2003) observaram achados semelhantes em frangos de
corte. Segundo Mitchell e Johns (2008), o hematócrito e os eritrócitos tendem a ser
mais elevados em machos do que nas fêmeas, assim como tendem a aumentar com
a idade, pois de acordo com Thrall et al. (2003), o estrógeno tende a diminuir a
eritropoese e os andrógenos promovem o efeito inverso. Ao observar a Tabela 1,
pode-se notar que essa informação procede, porém, em alguns parâmetros, não foi
relevante.
No leucograma (Tabela 2), os valores dos leucócitos totais encontram-se de
acordo com os observados por Samour (2006) nas idades 07 e 21 dias,
apresentando-se elevados nas idades 35 e 49 dias. Nestas duas idades, os valores
foram semelhantes aos resultados de Cunha et al. (1987), que verificaram valores
de leucócitos mais elevados para os frangos com idade próxima ao abate.
O leucócito observado em maior frequência nas idades de 07 e 21 dias foi o
monócito, seguido do linfócito e do heterófilo. Nas idades 35 e 49 dias, o heterófilo
passou a ser o leucócito predominante, seguido do monócito e do linfócito. Bounous
e Stedman (2000) afirmam que o heterófilo é a segunda célula mais numerosa nas
aves, no entanto, Cunha et al. (1987) relata que, em frangos com idade de abate, é
a célula predominante, corroborando os achados desta pesquisa. Eosinófilos e
basófilos encontrados demonstram valores semelhantes aos da literatura
(BOURNOUS; STEDMAN, 2000; SAMOUR, 2006).
A morfologia das células foi observada no esfregaço sanguíneo, onde os
eritrócitos dos animais estudados apresentavam formato elíptico com o núcleo
acompanhando o formato da célula. Seu citoplasma era abundante e de coloração
róseo-alaranjado, como demonstra a Figura 1, sendo também observado por
Bounous; Stedman (2000).
Segundo Morgulis (2002), as células do sistema imunológico das aves
dividem-se de acordo com a morfologia nuclear. Os agranulócitos são constituídos
por linfócitos e monócitos, incluindo também os trombócitos. Os granulócitos são

14
constituídos por heterófilos, eosinófilos e basófilos. A morfologia dos granulócitos
varia de acordo com as espécies aviárias.
Os trombócitos observados apresentavam-se como células ovais e
alongadas, pouco menores que os eritrócitos, possuindo um núcleo central, com
coloração basofílica intensa e o citoplasma hialino (Figura 1).
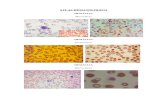
Figura 1 - Esfregaço sanguíneo demonstrando a presença de eritrócitos (seta) e trombócitos (cabeça de seta).
Fonte: Dados da pesquisa.
Os linfócitos (Figura 2) eram células redondas com citoplasma basofílico,
apresentando grânulos azurofílicos. Apresentam-se pequenos, médios ou grandes,
podendo ser facilmente confundido com trombócitos. Os achados encontram-se em
convergência com Bounous e Stedman (2000) e Thrall (2004).
Figura 2 - Esfregaço sanguíneo apresentando linfócitos (seta). Fonte: Dados da pesquisa.

15
Ainda conforme Bounous e Stedman (2000) e Thrall (2004), os maiores
leucócitos encontrados no sangue são os monócitos, o que também foi observado
neste estudo (Figura 3). Estes apresentam citoplasma cinza-azulado com grânulos e
um único núcleo de cor púrpura.
Figura 3 - Esfregaço sanguíneo com presença de monócito (seta). Fonte: Dados da pesquisa.
Na Figura 4, podem-se observar um heterófilo. Estes apresentavam
citoplasma sem coloração, com grânulos fusiformes laranja-avermelhados e núcleo
violeta segmentado, geralmente apresentando 2 lobos.
Figura 4 - Esfregaço sanguíneo apresentando heterófilo (seta) e monócito (cabeça de seta). Fonte: Dados da pesquisa.

16
Como os heterófilos, os eosinófilos (Figura 5) também apresentam o núcleo
violeta e segmentado, porém seus grânulos vermelho-alaranjados e redondos se
coram mais brilhantes, diferente dos primeiros. Outra coisa que os diferencia é a
presença do citoplasma de coloração azul.
Figura 5 - Esfregaço sanguíneo apresentando eosinófilo (seta) e trombócito (cabeça de seta). Fonte: Dados da pesquisa.
Os basófilos (Figura 6) são menores que os heterófilos e possuem o
citoplasma sem cor, com presença de grânulos púrpura escuros. Assim como seus
grânulos, seu núcleo tem cor púrpura e é não-lobulado, achado que converge com
os encontrados por Dein (1986) e Bounous e Stedman (2000).
Figura 6 - Esfregaço sanguíneo apresentando eritrócitos (seta), trombócitos (cabeça de seta) e basófilo (círculo).
Fonte: Dados da pesquisa.

17
Ainda durante a leitura dos esfregaços sanguíneos, foram observadas
bactérias em forma de bacilos, dispersos no plasma, apenas nos esfregaços das
aves com a idade de 07 dias. Esse fato pode ser justificado pela má cura do umbigo,
que deixa uma porta de entrada para bactérias e outros patógenos que podem
apresentar-se no ambiente, principalmente na cama de frango (ITO et al., 2004).
Figura 7 - Esfregaço sanguíneo apresentando bactéria em forma de bacilo (seta).
Fonte: Dados da pesquisa.
Segundo Borsa (2009), é importante salientar que vários fatores podem
influenciar nos valores hematológicos, tais como raça e linhagem das aves
analisadas, tipo de alimentação, temperatura ambiente, altitude, local da punção
venosa, bem como a técnica e o kit laboratorial empregados, dentre outros,
justificando assim as diferenças entre os valores encontrados no presente trabalho e
de outros autores.

18
4 CONCLUSÃO
Com este trabalho conclui-se que a avaliação hematólogica de frangos de
corte é importante para o monitoramento da sanidade aviária, e que idade, sexo,
linhagem, condições ambientais e diferentes localizações podem interferir
diretamente nos parâmetros hematológicos desses animais, havendo a necessidade
de maiores estudos com padronização de técnicas e valores de referência.

19
REFERÊNCIAS
BORSA, A. Valores hematológicos em frangos de corte de criação industrial. Colloquium Agrariae, v. 5, n. 1, p. 25 – 31. 2009.
BOUNOUS, D. I.; STEDMAN, N.L. Normal Avian Hematology: Chicken and Turkey. In: FELDMAN, B.F.; ZINKL, J.G.; JAIN, N.C. Schalm´s Veterinary Hematology. 5th ed, Philadelphia, Lippincot, Williams & Wilkins, 2000, p.1147-1154.
CAMPBELL, T. W. Hematology In: RITCHIE, B. W.; HARRISON, G. J.; HARRISON L. R. Avian medicine: principles and application. Lake Worth: Wingers Publishing, 1994. p. 176-198.
CAPITELLI, R.; CROSTA, L. Overview of psittacine blood analysis and comparative retrospective study of clinical diagnosis, hematology and blood chemistry in selected psittacine species. Veterinary Clinics of North America: Exotic Animal Practice, Texas, v. 16, p. 71-120, 2013.
CARDOSO, A L.S.P.; TESSARI, E.N.C. Estudo dos parâmetros hematológicos em frangos de corte. Arquivos do Instituto Biológico, v.70, n.4, p. 419-424, 2003.
CHARLES NORIEGA, M.L.V.C. Apuntes de hematología aviar: material didático para curso de hematologia aviária. Universidad Nacional Autónoma de México. Departamento de produccíon animal: Aves. México, 2000. p. 70.
CORDEIRO P.H.C. Fragmentação da Mata Atlântica no Sul da Bahia e suas implicações na conservação dos psitacídeos. In: PRADO P.I., LANDAU E.C., MOURA R.T., PINTO L.P.S., FONSECA G.A.B., ALGER K.N. Corredor de Biodiversidade da Mata Atlântica do Sul da Bahia. Ilhéus: IESB/CI/CABS/UFMG/Unicamp. 2003. (CD-ROM).
CUNHA, M.N.M. de A., et al. Leucograma em frangos de corte industrial. In: CONGRESSO BRASILEIRO DE AVICULTURA. 1987, Natal, RN. Anais... Fundação Apinco de Ciência e Tecnologia Avícola, 1987. p. 50-51.
DEIN, F. J. Hematology. In: Clinical Avian Medicine, Philadelphia, W B Sauders, 1986, p.174-191.
EVANGELISTA, F.R, NOGUEIRA FILHO, A., OLIVEIRA, A.A.P. A Avicultura industrial no Nordeste: aspectos econômicos e organizacionais. In: XLVI Congresso da Sociedade Brasileira de Economia, Administração e Sociologia Rural, 2008, Acre. Anais... Acre: Sociedade Brasileira de Economia, Administração e Sociologia Rural. 2008.

20
FURLAN, R.L., et al. Alterações hematológicas e gasométricas em diferentes linhagens de frangos de corte submetidos ao estresse calórico agudo. Revista Brasileira de Ciência Avícola, v.1, n.1, p. 77-84, 1999.
GONZÁLEZ, F.H.D., SANTOS, A.P. Patologia Clínica Veterinária. In: II Simpósio de Patologia Clínica Veterinária da Região Sul do Brasil, 2005, Porto Alegre. Anais... Porto Alegre, 91p. 2005.
ITO, N.M.KK. et al. Saúde gastrointestinal, manejo e medidas para controlar as enfermidades gastrointestinais. In: MENDES, A.A.; NÄÄS, I.A.; MACARI, M. Produção de frangos de corte. p. 205-260. Campinas: FACTA, 2004. cap.13.
JAIN, N.C. Schalm’s Veterinary Hematology, 4. ed. Philadelphia: Lea & Febiger, 1986. p.39-41.
MITCHELL, E. B.; JOHNS, J. Avian hematology and related disorders. Veterinary Clinics of North America: Exotic Animal Practice, v. 11, p. 501-522, 2008.
MORGULIS, M.S. Imunologia aplicada. In: MACARI, M., FURLAN, R.L., GONZALES, E. Fisiologia aviária aplicada a frango de corte. Jaboticabal: FUNEP/UNESP, 2002. p. 375.
REBAR, AH. Guia de Hematologia para cães e gatos. Editora Roca Ltda, São Paulo, 2003, p. 291.
SAMOUR, J. Diagnostic value of hematology. In: HARRISON, G. J.; LIGHTFOOT, T. L. Clinical Avian Medicine. v. 2., p. 587–609. Palm Beach: Spix, 2006. cap. 22.
SILVA, P.R.L. et al. Blood serum components and serum protein test of Hybro-PG broilers of different ages. Brazilian Journal of Poultry Science, Campinas, v.9, p. 213-216, 2007.
THRALL, M.A., et al. Hematologia de aves. In: Hematologia e Bioquímica Clínica Veterinária. 1 ed., p. 215-247. São Paulo: Roca, 2003. cap. 17.
VOIGT G.L. 2003. Conceptos y Técnicas Hematológicas para Técnicos Veterinários. Acribia, Zaragoza. p. 144.
ZHOU, W.T.; YAMAMOTO, S. Heat-induced the shifht of body fluid in broiler chickens. In: Proceedings 6th Asian Pacific Pouthry Congress, 1998, Nagoya, Japan. Anais… Nagoya, p. 292-293, 1998.

21
ANEXO – PARCER DO CEUA
Comitê de Ética no Uso de Animais do Centro Universitário Cesmac
(CEUA/CESMAC) Registro nº 01200702819/2016-97 – CIAEP/CONCEA – 10/10/2016.
Maceió, 23 de Maio de 2017.
PARECER CONSUBSTANCIADO
I) IDENTIFICAÇÃO: Protocolo Nº: 14A/2017 Título: Parâmetros hematológicos de frangos de corte de criação industrial do
agreste Alagoano
Pesquisador Responsável: Isabelle Vanderlei Martins Bastos Instituição Responsável: Centro Universitário Cesmac Data Entrada: 23/03/2017 II) SUMÁRIO DO PROJETO:
RESUMO DO PROJETO (Frangos de corte apresentam altos níveis zootécnicos na produção e estes níveis estão intimamente relacionados com a saúde destas aves. Assim, é de extrema importância que o sistema imunológico destes animais atue adequadamente e de maneira eficiente, possibilitando um bom desempenho produtivo, impedindo a introdução de doenças na criação. Dessa forma, as provas laboratoriais do sangue podem servir como ferramentas importantes para auxiliar no monitoramento da saúde das aves, no diagnóstico de doenças e também para avaliação pré-operatória, tratamento e das condições de saúde do organismo. A hematologia é um instrumento valioso e fundamental, pois serve para monitorar a saúde geral do animal e avaliar sua capacidade para transportar oxigênio e defender-se contra os agentes infecciosos, cujo objetivo é orientar o profissional no estabelecimento de prognóstico e protocolos terapêuticos para as diferentes enfermidades. O trabalho visa o conhecimento dos parâmetros hematológicos de frangos de corte em criatórios industriais em suas diferentes fases da vida através da pesquisa hematológica, que pode servir de embasamento para clínicos, produtores e futuros trabalhos, bem como melhorar a qualidade de vida dos animais das criações e gerar mais lucro final para os proprietários. III) COMENTÁRIOS ÉTICOS: 1) Nº de animais definido. Sim 2) Justificativa para o número de animais definida. Sim 3) Alojamento e condições especiais para os animais definidas.Sim 4) O pesquisador principal é o veterinário responsável pela pesquisa.Sim 5) Os procedimentos invasivos são justificados pela metodologia.Sim 9) Os riscos e benefícios para os animais definidos. Sim
Protocolo Nº: 14A/2017 Título: “Parâmetros hematológicos de frangos de corte de criação industrial do agreste Alagoano”. Página 1

22
IV) SITUAÇÃO DO PROTOCOLO APROVADO Ilmo Prof. (a) Dr. (a) Isabelle Vanderlei Martins Bastos, de acordo com as diretrizes para pesquisas com animais definidas pela Lei 11.794/2008 e decreto 6.899/2009, seu protocolo está APROVADO, lembre-se que:
• V.Sª. deve desenvolver a pesquisa conforme delineada no protocolo aprovado e descontinuar o estudo somente após análise das razões da descontinuidade por este CEUA, exceto quando perceber risco ou dano não previsto ao animal participante;
• O CEUA deve ser imediatamente informado de todos os fatos relevantes que alterem o curso normal do estudo. É responsabilidade do pesquisador assegurar medidas imediatas adequadas a evento adverso ocorrido e enviar notificação a este CEUA e, em casos pertinentes, à CONCEA;
• Eventuais modificações ou emendas ao protocolo devem ser apresentadas ao CEUA de forma clara e sucinta, identificando a parte do protocolo a ser modificada e suas justificativas;
• Seus relatórios parciais e final devem ser apresentados a este CEUA, inicialmente em 30/11/17 e ao término do estudo. A falta de envio de, pelo menos, o relatório final da pesquisa implicará em não recebimento de um próximo protocolo de pesquisa de vossa autoria.
Atenciosamente,
Protocolo Nº: 14A/2017 Título: “Parâmetros hematológicos de frangos de corte de criação industrial do agreste Alagoano”. Página 2








![RP 50205/01.07 Manômetro preenchido com glicerina · 1/10 Manômetro preenchido com glicerina Tipo ABZMM Tamanho nominal 40, 63 e 100 Indicação máxima 1000 bar [14500 psi] RP](https://static.fdocumentos.tips/doc/165x107/5b5d03a87f8b9aa1428d4667/rp-502050107-manometro-preenchido-com-glicerina-110-manometro-preenchido.jpg)








