UNIVERSIDADE FEDERAL DO CEARÁ FACULDADE DE … · Não há dados sobre seu potencial em reduzir...
Transcript of UNIVERSIDADE FEDERAL DO CEARÁ FACULDADE DE … · Não há dados sobre seu potencial em reduzir...

UNIVERSIDADE FEDERAL DO CEARÁ
FACULDADE DE MEDICINA
PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS MÉDICAS
TACYANO TAVARES LEITE
AVALIAÇÃO DOS DESFECHOS RENAIS EM PACIENTES GRAVES DE UNIDADE
DE TERAPIA INTENSIVA EM USO DE PROPOFOL OU MIDAZOLAM: ANÁLISE
DE ESCORE DE PROPENSÃO
FORTALEZA
2015

TACYANO TAVARES LEITE
AVALIAÇÃO DOS DESFECHOS RENAIS EM PACIENTES GRAVES DE UNIDADE
DE TERAPIA INTENSIVA EM USO DE PROPOFOL OU MIDAZOLAM: ANÁLISE
DE ESCORE DE PROPENSÃO
Dissertação apresentada ao Programa de
Pós-Graduação em Ciências Médicas da
Universidade Federal do Ceará, como
requisito parcial à obtenção do título de Mestre
em Medicina. Área de concentração: Doenças
Crônicas e Degenerativas.
Orientador: Prof. Dr. Alexandre Braga Libório.
FORTALEZA
2015

Dados Internacionais de Catalogação na Publicação
Universidade Federal do Ceará
Biblioteca de Ciências da Saúde
___________________________________________________________________________
L556a Leite, Tacyano Tavares
Avaliação dos desfechos renais em pacientes graves de unidade de terapia intensiva em uso de
propofol ou midazolam: análise de escore de propensão/ Tacyano Tavares Leite. – 2015.
40 f. : il.
Dissertação (Mestrado) – Universidade Federal do Ceará. Faculdade de Medicina. Programa de Pós-
graduação em Ciências Médicas, Fortaleza, 2015.
Área de concentração: Doenças crônicas e degenerativas.
Orientação: Prof. Dr. Alexandre Braga Libório.
1. Lesão Renal Aguda. 2. Nefropatias. 3. Diálise. I. Título.
CDD 616.61
_______________________________________________________________________________

TACYANO TAVARES LEITE
AVALIAÇÃO DOS DESFECHOS RENAIS EM PACIENTES GRAVES DE UNIDADE DE
TERAPIA INTENSIVA EM USO DE PROPOFOL OU MIDAZOLAM: ANÁLISE DE
ESCORE DE PROPENSÃO
Dissertação apresentada ao Programa de Pós-
Graduação em Ciências Médicas da
Universidade Federal do Ceará, como requisito
parcial à obtenção do título de Mestre em
Medicina. Área de concentração: Doenças
Crônicas e Degenerativas.
Aprovada em: _____/_____/______.
BANCA EXAMINADORA
________________________________________
Prof. Dr. Alexandre Braga Libório (Orientador)
Universidade Federal do Ceará (UFC)
_________________________________________
Prof.ª Dr.ª Elizabeth De Francesco Daher
Universidade Federal do Ceará (UFC)
_________________________________________
Prof. Dr. Marcelo Jacó
Universidade Federal do Ceará (UFC)

AGRADECIMENTOS
Gostaria de agradecer inicialmente ao professor Alexandre Braga Libório que
considero um grande orientador e, acima de tudo, um grande amigo, sempre auxiliando nas
duvidas que surgiram durante a realizacao deste trabalho.
Aos meus pais, Tavares e Rose, que sempre me incentivaram a alcancar caminhos
cada vez mais distantes.
Aos meus irmãos, Tamystoylls e Tayalles, que sempre compreenderam a
importancia do mestrado para mim.
Finalmente, gostaria de agradecer a Universidade Federal do Ceará e ao corpo
docente do Programa de Pós-Graduação em Ciências Médicas.

RESUMO
Introdução: O propofol tem demonstrado efeito renoprotetor contra as lesões de isquemia /
reperfusão em cenários experimentais, entretanto as evidências clínicas de tal efeito limitam-
se a pacientes submetidos a cirurgia cardíaca. Não há dados sobre seu potencial em reduzir
eventos renais nos pacientes criticamente enfermos de Unidades de terapia intensiva (UTIs)
clínicas. Métodos: Os dados foram obtidos a partir do banco de dados on-line, Intelligent
Monitoring Multiparameter in Intensive Care (MIMIC-II), entre os anos de 2001 e 2008. Fo-
ram incluídos pacientes adultos em sua primeira internação na UTI, com necessidade de ven-
tilação mecânica e em sedação com propofol ou midazolam. Um modelo de análise de escore
de propensão (1:1) foi utilizado para tratamento estatístico dos dados e os desfechos – Inci-
dência de lesão renal aguda (IRA), oligúria, balanço hídrico cumulativo e necessidade de te-
rapia renal substitutiva (TRS) - foram avaliados durante os primeiros 7 dias de internação na
UTI. Resultados: Após o balanceamento estatístico, 703 pacientes em sedação com propofol
eram comparáveis a 703 pacientes em sedação com midazolam. A incidêcnia de IRA nos
primeiros sete dias de internamento na UTI foi significativamente inferior nos pacientes em
uso de propofol quando comparados aos pacientes em uso de midazolam (OR: 0,58, 95% in-
tervalo de confiança [IC], 0,47-0,73). O uso de propofol como sedativo esteve relacionado a
proteção contra IRA independente do critério diagnóstico utilizado: débito urinário (OR
0,637, IC 95% 0,516-0,786); creatinina sérica LRA (OR 0,683, 95% CI ,546-0,854). Os paci-
entes que receberam propofol apresentaram oligúria com menor frequência (12,2 vs. 19,6%, p
<0,001) e diuréticos prescritos com menos frequência (8,5 vs 14,2%, p = 0,001). Além disso,
durante os primeiros 7 dias de internação na UTI, os pacientes que receberam propofol
atingiram um balanço hídrico acumulado > 5% dos peso corporal com menos freqüencia
(50,2 vs. 58,6%, p = 0,002). A necessidade de TRS nos primeiros 7 dias de UTI também foi
menos frequente nos doentes tratados com propofol (OR 0,571 IC 95% 0,341-0,955). A
mortalidade na UTI foi inferior nos pacientes em sedação com propofol (14,5 vs 29,7%, p
<0,001). Conclusão: Nessa grande amostra de pacientes críticos pareados por um mo-
delo de propensão, os pacientes em sedação com propofol tiveram um menor risco de desen-
volver IRA, assim como desenvolveram menos complicações relacionadas ao acúmulo de
fluidos e necessidade de TRS.
Palavras-chave: Lesão Renal Aguda. Nefropatias. Diálise.

ABSTRACT
Introduction: Propofol has been shown to provide protection against renal ische-
mia/reperfusion injury experimentally, but clinical evidence is limited to patients undergoing
cardiac surgery. There is no data about its potential renoprotection in critically-ill patients.
Methods: Data were obtained from the Multiparameter Intelligent Monitoring in Intensive
Care (MIMIC-II) database (2001–2008). Patient selection criteria included adult patients in
their first ICU admission, need for mechanical ventilation and treatment with propofol or
midazolam. Propensity score analysis (1:1) was used and renal-related outcomes - acute kid-
ney injury (AKI), oliguria, cumulative fluid balance and need for renal replacement therapy
(RRT) - were evaluated during the first 7 days of ICU stay. Results: There were 1,406
propofol–midazolam matched patients. AKI in the first 7-day ICU time period was statistical-
ly lower in propofol-treated patients when compared with midazolam-treated patients (OR:
0.58, 95% confidence interval [CI], 0.47–0.73). Propofol-related protection was observed in
both urine output (OR 0.637, 95%CI 0.516–0.786) and serum creatinine AKI criteria (OR
0.683, 95%CI 0.546-0.854). Patients receiving propofol had oliguria less frequently (12.2 vs.
19.6%, p<0.001) and had diuretics prescribed less often (8.5 vs. 14.2 %, p=0.001). Also, dur-
ing the first 7 days of ICU stay, patients receiving propofol less frequently achieved cumula-
tive fluid balance greater than 5% of body weight (50.2 vs. 58.6%, p=0.002). Need for RRT
in the first 7-day ICU time was also less frequent in propofol-treated patients (OR 0.571
95%CI 0.341- 0.955). ICU mortality was lower in propofol-treated patients (14.5 vs. 29.7%,
p<0.001). Conclusion: In this large, propensity-matched ICU population, patients treated
with propofol had a reduced risk of AKI, fluid-related complications and need for RRT.
Keywords: Acute Kidney Injury. Kidney Diseases. Dialysis.

LISTA DE FIGURAS
Figura 1 - Estrutura química do propofol (1,2-diisopropilfenol) …………………….............19
Figura 2 - Fórmulas estruturais do 2,6 - diisopropylphenol (propofol), hidroxitolueno mutila-
do e Trolox C. ……………………………………………………..........…........................... 20
Figura 3 - Distribuição do escore de propensão comparando os grupos tratados com midazo-
ram antes e após o pareamento. ………………………………………................................. 28
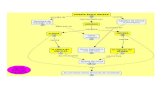
Figura 4 - Desenho do estudo ………………………………………………........................ 29
Figura 5 - Incidência de LRA nos pacientes em uso de propofol e midazolam, geral, estratifi-
cação por estágio da LRA ………………………………………………………................... 34
Figura 6- Odds ratio para LRA, conforme estágio da LRA (por nível de CrS e débito uriná-
rio).............................................................................................................................................35

LISTA DE TABELAS E QUADROS
Quadro1 - Classifição da LRA conforme o critério KDIGO ………………………….......... 15
Tabela 1 - Características clínicas da população em estudo, Propofol x Midazolam, antes e
após pareamento das amostras ………………………………………………........................ 31
Tabela 2 - Avaliação dos desfechos em ambos os grupos após o balanceamento estatístico
…………………………………………………………………………….............................. 35

LISTA DE ABREVIATURAS
AKIN Acute Kidney Injury Network
BH Balanço hídrico
BHT Hidroxitolueno butilado
BMP-2 Proteína óssea morfogenética tipo 2
CID-9 Classificação Internacional de Doenças versão 9
CrS Creatinina Sérica
DM Diabetes Mellitus
DPOC Doença pulmonar obstrutiva crônica
DRC Doença Renal Crônica
DU Débito urinário
DVA Droga vasoativa
ECG Escala de Coma de Glasgow
GABA Ácido gama-aminobutírico
HAS Hipertensão arterial Sistêmica
ICC Insuficiência cardíaca congestiva
IL-6 Interleucina-6
IL-8 Interleucina-8
IQR Interquatile range
KDIGO Kidney Disease Improving Global Outcomes
LRA Lesão renal aguda
MIMIC Intelligent Monitoring Multiparameter in Intensive Care
NMDA N-metil-D-aspartato
PAM Pressão arterial Média
RIFLE Risk, Injury, failure, Loss, End stage
SAPS Simplified Acute Physiology Score
SOFA Sequential Organ Failure Assesment
TNF-∝ Fator de necrose tumoral alfa
TRS Terapia renal substitutiva
UTI Unidade de Terapia Intensiva
VM Ventilação Mecânica

SUMÁRIO
1 INTRODUÇÃO …………………………………………………..... 14
1.1 Lesão Renal Aguda ………………………………………………… 14
1.2 Sedação na Terapia Intensiva …………………………………….. 15
1.3 Farmacologia do Midazolam ……………………………………… 17
1.4 Farmacologia do Propofol ………………………………………… 18
1.4.1 Efeito antioxidante do Propofol …………………………………… 19
1.5 Escolha do Sedativo X LRA ……………………………………… 20
1.6 Pergunta de Partida ……………………………………………… 21
1.7 Hipóteses …………………………………………………………… 21
1.8 Objetivos ………………………………………………………….. 22
1.8.1 Objetivo Geral …………………………………………………….. 22
1.8.2 Objetivos Específicos ……………………………………………… 22
2 MÉTODOS ………………………………………………………… 23
2.1 O banco de dados MIMIC II ……………………………………… 23
2.2 Critérios de inclusão e exclusão …………………………………… 23
2.3 Coleta de Dados …………………………………………………… 24
2.4 Definição de LRA ………………………………………………… 24
2.5 Análise Estatística ………………………………………………… 26
2.5.1 O Modelo de Escore de Propensão ………………………………… 27
2.5.2 Seleção do Modelo e Pareamento das Amostras …………………… 27
2.5.3 Variáveis incluídas no Escore de Propensão ………………………… 28
3 RESULTADOS …………………………………………………… 31
3.1 População em estudo ……………………………………………… 31
3.3 Coorte Balanceada ………………………………………………… 33
3.3 Desenvolvimento de LRA ………………………………………… 33

3.4 Oligúria, diurético e balanço hídrico ……………………………… 36
3.5 Terapia Renal Substitutiva ………………………………………… 37
3.6 Tempo de permanência em UTI e mortalidade ………………… 37
4 DISCUSSÃO ……………………………………………………… 38
5 CONCLUSÃO ……………………………………………………… 42
REFERÊNCIAS
ANEXOS

11
1 INTRODUÇÃO
1.1 Lesão Renal Aguda
A lesão renal aguda (LRA) é uma síndrome clínica heterogênea e complexa, definida
como um declínio abrupto, num período de horas a dias, na taxa de filtração glomerular
(TFG), resultando na retenção de produtos do metabolismo, entre os quais encontram-se a
uréia e a creatinina, e na desregulação do equilíbrio hidro-eletrolítico e ácido-básico.(TAAL,
M. W. et al, 2011) Com base no mecanismo fisiopatológico que leva à disfunção renal, a LRA
pode ser classificada em pré-renal, renal intrínseca e pós renal (FLOEGE; JOHNSON;
FEEHALLY, 2010).
Em termos clínicos, a LRA é definida, de acordo com a última diretriz do Kidney Di-
sease Improving Global Outcomes (KDIGO), como uma elevação de 0,3 mg/dl ou superior na
creatinina de base, ocorrida no intervalo de até 48 horas, uma elevação de 1,5 vezes na valor
basal de creatinina sérica, que presumivelmente tenha ocorrido num intervalo de até sete dias,
ou um volume urinário inferior a 0,5 ml/kg/h por seis horas consecutivas(LEVIN; STEVENS,
2014). Essa definição, derivada da combinação das duas classificações utilizadas previamen-
te, Risk, Injury, Failure, Loss, End Stage (RIFLE) e Acute Kidney Injury Network (AKIN)
(BAGSHAW et al., 2008; LEVIN; STEVENS, 2014), uniformizou os estudos clínicos sobre
LRA. Vem sendo amplamente utilizada na prática clínica para diagnóstico da LRA, possui
utilidade, não somente como importante ferramenta para diagnóstico precoce dessa enfermi-
dade, mas também na estratificação e estadiamento da LRA conforme a gravidade do quadro
clínico (Quadro 1), possibilitando a tomada de decisões individualizadas como elemento guia
na indicação da terapia renal substitutiva (LEITE et al., 2013).

12
Quadro 1 - Classifição da LRA conforme o critério KDIGO (KDIGO, 2012)
Estágio CrS Débito Urinário
1 1,5 - 1,9 X CrS de base ou
≧ 0,3 mg/dl < 0,5 ml/kg/h por 6-12 horas
2 2 - 2,9 X CrS de base < 0,5 ml/kg/h por 12 - 24 horas
3 3 X CrS de base ou
Aumento na CrS para ≧ 4,0 mg/dl ou
Início de terapia renal substitutiva
< 0,3 ml/kg/h por ≧ 24 horas ou
Anúria por ≧ 12 horas
Classificação da lesão renal aguda por estágios a depender da intensidade da elevação da creatinina séria e/ou redução
do débito urinário, conforme as últimas diretrizes para o diagnóstico e manejo da LRA.
LRA: Lesão Renal Aguda; KDIGO: Kidney Disease Improving Global Outcomes; CrS: creatinina sérica.
A LRA é hoje reconhecida como um importante problema de saúde pública. Afeta mi-
lhões de pacientes em todo o mundo (SINGBARTL; KELLUM, 2012). É uma complicação
comum entre os pacientes hospitalizados e gravemente enfermos. Uma revisão sistemática de
312 estudos de coorte incluindo 49 milhões de pacientes encontrou que um em cada cinco
adultos e uma em cada três crianças internados com doenças agudas apresentam LRA no cur-
so do seu internamento (SUSANTITAPHONG et al., 2013). Os pacientes graves de Unidades
de Terapia Intensiva (UTI) possuem risco ainda maior de desenvolverem a LRA. Esta é a dis-
função orgânica mais frequentes dos pacientes de UTI não-sépticos e a segunda entre aqueles
admitidos na UTI com diagnóstico de sepse ou que a desenvolvem no decorrer do interna-
mento na UTI (MURUGAN; KELLUM, 2011). A incidência da LRA durante a permanência
na UTI varia de 36 a 67%, utilizando os critérios diagnósticos mais atuais (HOSTE et al.,
2006; BAGSHAW et al., 2008). Sua ocorrência, está sabidamente associada ao tempo de
permanência na UTI, à morbidade e mortalidade desses pacientes, que se elevam conforme a
gravidade e o estágio da LRA (BARRANTES et al., 2008).
Além disso, a LRA está associada ao aumento da velocidade de progressão de doença
em pacientes com doença renal cônica (DRC) com diagnóstico prévio, ou aumento na inci-
dência de novos casos de DRC (SINGBARTL; KELLUM, 2012; LEVIN; STEVENS, 2014;
REWA; BAGSHAW, 2014) Pacientes graves são constantemente expostos às mais diversas
formas de insulto renal (ventilação mecânica, sepse, isquemia, baixo débito cardíaco, nefroto-
xicidade de drogas, e comorbidades subjacentes). Parte dos mecanismos envolvidos na pato-
gênese da LRA em pacientes graves, em grande parte, persistem desconhecidos. Sabe-se que,
além dos fatores relacionados às características clínicas dos pacientes, a LRA está altamente

13
envolvida a processos fisiopatológicos complexos e multifatoriais relacionados às alterações
pró-inflamatórias e ao estresse oxidativo encontrado especificamente nesse tipo de indivíduo
(KINSEY; OKUSA, 2011).
1.2 Sedação na terapia intensiva
Pacientes graves em ventilação mecânica frequentemente necessitam de sedativos em
infusão contínua para reduzir o desconforto e a ansiedade associados à ventilação mecânica.
Sedativos benzodiazepínicos, como o midazolam e o lorazepam, e o propofol são as drogas
mais comumente utilizadas para sedação em terapia intensiva (BARR et al., 2013). As diretri-
zes de 2002 recomendavam o uso do midazolam para sedação de curta duração, o lorazepam
para sedação de longa duração e o propofol para os pacientes com necessidade de despertar
diário (JACOBI et al., 2002).
Diversos estudos têm demonstrado as consequências negativas da sedação prolongada
e profunda e os benefícios da utilização de níveis mais brandos de sedação nos pacientes adul-
tos de terapia intensiva (GIRARD et al., 2008; TREGGIARI et al., 2009; KOLLEF et al.,
1998). A aplicação das escalas de sedação, protocolos clínicos elaborados no sentido de mi-
nimizar o uso de sedativos e o uso de sedativos não-benzodiazepínicos estão associados a
melhora dos desfechos clínicos em pacientes adultos de terapia intensiva, (ARABI et al.,
2007; ARIAS-RIVERA et al., 2008) incluindo tempo de ventilação mecânica, tempo de per-
manência hospitalar e na UTI (LONARDO et al., 2014; KOLLEF et al., 1998).
Segundo a Diretriz de 2013 para o Manejo da Dor, Agitação e Delirium no Paciente
Adulto de Terapia Intensiva a sedação de manutenção no paciente em ventilação mecânica
deve ser realizada preferencialmente com medicamentos não-benzodiazepínicos como o pro-
pofol ou dexmedetomedine (JACOBI et al., 2002). As evidências para essa mudança susten-
tam-se em estudos que identificaram o uso de benzodiazepínicos como sedativos de manuten-
ção como fator de risco independente para o desenvolvimento de delirium, aumento do tempo
de internação hospitalar e elevação de mortalidade aos seis meses (ELY et al., 2004; CAR-
SON et al., 2006).
Em uma recente metanálise (HO; NG, 2008), a administração de propofol como agen-
te sedativo de manutenção esteve associada com redução do tempo de ventilação mecânica e
do tempo de permanência na UTI. Além disso, um outro estudo retrospectivo mais recente
mostrou que a sedação com propofol estava associada a melhora sobrevida quando comparada

14
à sedação com benzodiazepínicos (LONARDO et al., 2014). Entretanto ainda há debate na
literatura sobre qual deveria ser a estratégia de escolha para sedação de manutenção em paci-
entes críticos sob ventilação mecânica.
Apesar de tais evidências, alguns estudos ainda apontam a predominância da utiliza-
ção de medicamentos benzodiazepínicos como sedativos no paciente de terapia intensiva,
sendo que o uso do midazolam para esta prática pode variar de 35 a 70% (MARTIN et al.,
2007; PAYEN et al., 2007).
1.3 Farmacologia do Midazolam
O midazolam é um depressor do sistema nervoso central (SNC), largamente utilizado
em anestesiologia e terapia intensiva. Seu efeito decorre da sua ativação dos receptores neu-
ronais tipo A do ácido γ-aminobutírico (GABAA) provocando redução da ansiedade, amnésia
anterógrada, sedação, hipnose, efeito anticonvulsivante e relaxamento muscular (YOUNG;
PRIELIPP, 2001; GREENBLATT; HARMATZ; SHADER, 1991).
Pertence à classe farmacológica dos 5-aril-1,4-bezodiazepínicos, caracterizados pela
fusão de um anel benzeno a um anel diazepínicos e a presença de um anel aril como substituto
na posição 5 do anel diazepínico, característica comum à maioria dos benzodiazepínicos em
uso clínico. É classificado como droga de ação curta pelo seu rápido início de ação e término
de efeito em comparação aos demais compostos benzodiazepínicos. É altamente lipossolúvel
em pH fisiológico (DOS SANTOS; PORTELLA,
O principal local de metabolização é o fígado onde é metabolizado a 1’-hidroxi-
midazolam, 4-hidroximidazolam e 1’,4-dihidroximidazolam (THUMMEL et al., 1996). Seu
principal metabólito, o 1’-hidroxi-midazolam, é de excreção renal e possui 50% da atividade
do midazolam (DOS SANTOS; PORTELLA. É classificada como droga intermediária em
relação à sua taxa de extração hepática, diferentemente do propofol que possui alta extração
hepática e dependência do fluxo sanguíneo hepático como determinante da sua taxa de meta-
bolização THUMMEL et al., 1996).

15
1.4 Farmacologia do propofol
O propofol é um agente hipnótico de curta duração administrado em infusão intrave-
nosa (GOODMAN, 1996), utilizado na indução e manutenção da anestesia geral, na sedação
para procedimentos e como agente de manutenção na sedação dos pacientes em ventilação
mecânica (JACOBI et al., 2002).
Trata-se de um composto alquifenol, 2,6-diisopropilfenol, formulado em emulsão lipí-
dica, virtualmente insolúvel em solução aquosa. Seu mecanismo de ação está principalmente
relacionado à potencialização do GABA, possui também ação inibitória do N-Metil-D-
Aspartato (NMDA), subtipo de receptor de glutamato (BARASH, 2009). Sofre rápida meta-
bolização hepática, produzindo um composto insolúvel de alto clearence plasmático excretado
pela urina. Apresenta mais completa recuperação que o tiopental, produzindo menos efeitos
desagradáveis. De maneira análoga ao tiopental, sua rápida distribuição ocorre por transferên-
cia do compartimento central (tecidos ricamente vascularizado), para tecidos menos perfundi-
dos: músculos e gordura. O despertar ocorre aproximadamente oito minutos após uma dose
simples de indução. Mantém capacidade de rápido despertar, mesmo após infusões intraveno-
sas contínuas prolongadas (GOODMAN, 1996; BARASH, 2009).
Figura 1. Estrutura química do propofol (1,2-diisopropilfenol)
A figura Evidencia a presença do radical hidroxila ligado ao anel aromático, característica comum aos outros
compostos com características anti-oxidantes e anti-inflamatórias.
1.4.1 Efeito anti-oxidante do propofol
Além das suas propriedades anestésicas intrínsecas, o propofol tem propriedades anti-
inflamatórias e imuno-moduladoras (SONG et al., 2009; HSING et al., 2010; MURPHY et
al., 1992). Parte desse efeito pode ser justificado pelo seu potencial anti-oxidante demonstra-

16
do tanto em experimentos in vitro (GREEN; BENNETT; NELSON, 1994; MURPHY et al.,
1992) e in vivo (YANG; CHOU; PEI, 2013). Tal efeito pode ser justificado pela semelhança
estrutural entre as moléculas de 2,6-diisopropylphenol (propofol), hidroxitolueno butilado, e
do Trolox C (um análogo hidrossolúvel da vitamina E), esses dois últimos amplamente co-
nhecidos como compostos anti-oxidantes (GREEN; BENNETT; NELSON, 1994; MURPHY
et al., 1992).
Murphy et al. examinaram in vitro as propriedades anti-oxidantes do propofol. Nesse
estudo foi evidenciado que o propofol reage com os radicais livres formando um radical feno-
xil. Esse é um fenômeno comum a todos os compostos com ação varredora de radicais livres
incluindo o anti-oxidante endógeno ∝-tocoferol (vitamina E).
Figura 2. Fórmulas estruturais do 2,6 - diisopropylphenol (propofol), hidroxitolueno butilado e Trolox C.
Propofol
BHT Trolox C
Os três compostos carreiam um radical hidroxila nos anéis fenícios. Essa substitiuição confere ao composto a
propriedade de limpeza dos radicais livres.
1.5 Escolha do Sedativo X LRA
Diversos estudos em animais sugeriram que o propofol é eficaz na atenuação de LRA
em diferentes modelos (YANG; CHOU; PEI, 2013; RODRÍGUEZ-LÓPEZ et al., 2006).
Yang, Chou e Pei (2013), demonstraram em modelos experimentais de isquemia reperfusão
em ratos que o propofol protegeu contra os efeitos deletérios da isquemia tecidual e esses in-
divíduos apresentaram níveis significativamente inferiores de creatina que os indivíduos con-
troles. Esses dados também correlacionaram-se com a análise histológica dos fragmentos re-
nais desses camundongos em que aqueles que receberam propofol apresentaram dano tecidual
discreto. Foram detectados maiores níveis teciduais nos rins dos camundongos tratados com

17
propofol de superóxido dismutase, um dos anti-oxidante endógenos, bem como menores ní-
veis das citocinas pró-inflamatórias IL-6, IL-8 e TNF-∝ , corroborando a hipótese do efeito
anti-inflamatório dessa droga (ABE, 2006). Esse estudo evidenciou também expressão au-
mentada do RNAm para a proteína óssea morfogenética 2 (BMP-2) que exerce efeitos vaso-
protetores, mantendo o balançoo entre a proliferação e a apoptose do endotélio.
Outro estudo mostrou que suínos submetidos a clampeamento aórtico supra-renal a-
nestesiados com propofol apresentaram menos infiltração do tecido renal por neutrófilos, me-
nor concentração plamática de citocinas pró-inflamatórias, menor produção de radicais livre
de oxigênio e menor peroxidação lipídica. Esses achados reforçam os dados do estudo anteri-
or e as propriedades anti-oxidante e anti-inflamatórias do propofol (SONG et al., 2013).
Embora seja comumente observado que as estratégias terapêuticas e preventivas rela-
cionadas à LRA são bem sucedidas em modelos animais e não em estudos humanos, em um
estudo recente, randomizado e controlado, a aplicação do propofol como agente anestésico foi
associado a uma redução na incidência de LRA em pacientes submetidos a cirurgia cardíaca
valvar em comparação à anestesia com sevoflurano (YOO et al., 2014). Embora provocativo,
o pequeno número de pacientes envolvidos e os resultados conflitantes com pequenos ensaios
semelhantes prévios também avaliando o uso do propofol limitam o nosso entusiasmo. Além
disso, a população bastante específica de doentes avaliada neste estudo não permite generali-
zar os resultados para outros procedimentos cirúrgicos ou para pacientes críticos de UTI geral.
1.6 Pergunta de Partida
Baseado nos dados da literatura sobre o efeito renoprotetor do propofol em modelos
experimentais e em pacientes submetidos a cirurgia cardíaca, seria possível demonstrar em
uma população de pacientes críticos de UTI geral tais efeitos?
1.7 Hipóteses
É possível reduzir a incidência de LRA em pacientes críticos de UTI geral especial-
mente os casos de LRA grave adotando o propofol como agente sedativo de manutenção em
pacientes críticos de UTI geral sob ventilação mecânica.
Pacientes em sedação de manutenção com propofol que apresentam LRA apresentam
menor necessidade de terapia de substituição renal.

18
A sedação de manutenção com propofol está associada a redução do balanço hídrico
acumulado e menor necessidade de de uso de diuréticos.
1.8 Objetivos
1.8.1 Objetivo Geral
Avaliar o efeito nefroprotetor do propofol em pacientes críticos em ventilação mecâni-
ca com necessidade de sedação de manutenção.
1.8.2 Ojetivos Específicos
Avaliar a incidência de LRA em pacientes em sedação de manutenção com propofol
comparado aos pacientes em sedação com midazolam.
Avaliar a ocorrência das formas graves de LRA em pacientes de terapia intensiva sob
ventilação mecânica em sedação com propofol e midazolam.
Comparar o balanço hídrico acumulado nos pacientes em sedação de manutenção com
propofol e midazolam, bem como a necessidade de diuréticos.
Avaliar a necessidade de TRS em pacientes críticos em ventilação mecânica em seda-
ção com propofol e midazolam.

19
2 MÉTODOS
2.1 O Banco de Dados MIMIC-II
O projeto Intelligent Monitoring Multiparameter in Intensive Care (MIMIC-II), man-
tido pelo Laboratório de Fisiologia Computacional do Instituto de Tecnologia de Massachu-
setts (MIT), contém dados sobre pacientes internados nas UTIs do Hospital Beth Israel Dea-
coness Medical Center compreendidos entre os anos 2001 e 2008 (SAEED et al., 2011). O
banco de dados está disponível on-line gratuitamente, de modo que qualquer pesquisador que
aceite o contrato de uso dos dados e assista ao “treinamento para proteção de seres humanos"
pode solicitar autorização para acessar os dados. Este estudo foi aprovado pelos Conselhos de
Revisão Institucional do Instituto de Tecnologia de Massachusetts e do Beth Israel Deaconess
Medical Center e foi dispensado da necessidade da coleta e assinatura do termo consentimen-
to informado.
O banco de dados inclui dados básicos sobre a admissão e informações demográficas
(dos quais nem todos foram utilizado no presente estudo), bem como sinais vitais, resultados
de laboratório e radiologia, medicamentos, diagnósticos de alta hospitalar, anotações de en-
fermagem, resumos de alta da unidade e hospitalar e datas dos óbitos. O banco de dados MI-
MIC-II contém dados de pacientes de cinco tipos de UTIs: UTI clínica, UTI cirúrgica, UTI
cardíaca, unidade de recuperação de cirurgia cardíaca e UTI neonatal. Outros dados clínicos
inclusos no banco de dados incluem os registros da farmácia, registros de entrada de pedidos
do provedor, registros de admissão e óbito, resumos de alta, e o CID-9 (Código Internacional
de Doenças) das respectivas patologia.
2.2 Critérios de Inclusão e Exclusão
Foram incluídos neste estudo todos os pacientes com idade superior a 15 anos subme-
tidos à ventilação mecânica que receberam propofol ou midazolam durante as primeiras 48
horas de internação na UTI. Os pacientes com exames laboratoriais insuficientes, aqueles com
diagnóstico prévio de doença renal crônica (DRC) avançada e aqueles que submetidos a TRS
antes da internação na UTI foram excluídos. Além disso, os pacientes com tempo de interna-
ção em UTI inferior a 24h, creatinina sérica à admissão superior a 4 mg/dL e aqueles que re-
ceberam propofol e midazolam foram excluídos.

20
2.3 Coleta de Dados
Todos os dados foram extraídos do banco de dados MIMIC-II (v2.6) e incluiu infor-
mações demográficas (por exemplo, idade, sexo) e informação clínicas dos registros de ad-
missão. Os seguintes dados de internação foram coletados nas primeiras 24 horas de interna-
ção na UTI: primeiro registro do peso corporal em Kg, escala de coma de Glasgow (ECG),
primeira dosagem de creatinina sérica (CrS) disponível e os scores de gravidade da doença,
SAPS I (Simplified Acute Physiology Score) e SOFA (Sequential Organ Failure Assessment),
ambos sem atribuição do componentes renal, pois este pode influenciar o médico na escolha
do tipo de sedativo ou os desfechos avaliados. Foram coletados ainda os parâmetros hemodi-
nâmicos das primeiras 48 horas de internação na UTI: valor médio da pressão arterial média
(PAM), necessidade de drogas vasoativas e tempo de ventilação mecânica. Os desfechos re-
nais foram avaliados nos primeiros 7 dias de internação na UTI: CrS máxima, débito urinário
(DU), uso de diuréticos, balanço hídrico (BH) acumulado e necessidade terapia de substitui-
ção renal (TRS). Os outros desfechos secundários (tempo de internação e mortalidade na UTI)
foram avaliados ao final do internamento na UTI.
2.4 Definição de Lesão Renal Aguda
LRA foi definida de acordo com o critério KDIGO (Kidney Disease Improving Global
Outcomes), em resumo, os níveis de creatinina sérica e o débito urinário foram utilizados para
classificar o estágio da LRA em que o paciente se encobtrava. Uma vez que objetivo era ava-
liar os efeitos do sedativo (propofol ou midazolam) sobre a função renal, o primeiro nível de
CrS disponível após a internação na UTI foi utilizada como referência para a função renal de
base. Os pacientes foram classificados com base no estágio máximo alcançado durante os
primeiros 7 dias de internação na UTI. Os pacientes que receberam TRS durante este período
foram consideradas como LRA estágio 3. O débito urinário foi avaliado hora a hora. Utilizou-
se o critério débito urinário de para os pacientes com pelo menos 24 horas consecutivas de
medidas válidas. O critério KDIGO foi aplicado a esses pacientes, calculando-se o débito uri-
nário normatizado pelo peso ao longo de cada período de 6 horas (MACEDO et al., 2011).
Aos pacientes com medidas insuficientes de débito urinário, apenas o critério da creatinina
sérica foi utilizado para classificação conforme a gravidade da LRA .
Foram utilizadas médias estimadas para todas as variáveis com valores em falta quan-
do eles representaram menos de 3% do total da amostra. No peso corporal, faltaram dados em

21
pelo menos 15% dos registros, os valores em falta foram imputados como as médias específi-
cas de cada gênero. Apenas a primeira internação na UTI foi considerado para cada paciente
para efeito de análise.
2.5 Análise Estatística
Aplicou-se estatística descritiva inicialmente, incluindo médias, desvios padrão ou
frequências para descrever a população conforme o caso. Para a análise univariada, os testes
qui-quadrado e testes t de Student foram utilizados para avaliar a significância estatística. To-
dos os testes foram bicaudais, e um valor de p <0,05 foi considerado como estatisticamente
significativo. Posteriormente, foram utilizadas técnicas de escore de propensão para balance-
amento de amostras e atingir o equilíbrio das características clínicas de base dos pacientes nos
dois grupos. As variáveis da admissão e aquelas obtidas durante as primeiras 48 horas de in-
ternação na UTI identificadas como potenciais fatores de confusão foram utilizadas para cons-
truir o modelo inicial de regressão logística para predizer o uso de propofol. Além disso, co-
mo a LRA tem sido associada à ventilação mecânica em uma relação de causalidade bidireci-
onal e o propofol tem sido associado com menor tempo de ventilação mecânica, incluímos
dependência de ventilação mecânica no período entre 48 h e 7 dias de UTI no escore de pro-
pensão.
2.5.1 O Modelo de Escore de Propensão
O objetivo do escore de propensão é resumir todas as informações sobre as variáveis
confundidoras de um indivíduo em um único valor, a probabilidade de receber o tratamento
de interesse (LOPES; HARRINGTON, 2015). Escores de propensão próximos de 1,0 indicam
probabilidade próxima de 100 % de um indivíduo receber determinado tratamento de interes-
se, de maneira análoga um indivíduo com escore de propensão de 0,5, possui probalidade
igual de receber o tratamento de interesse ou de não receber tratamento algum. Essa probabi-
lidade é calculada com base nas características clínico-demográficas das amostras em estudo.
todos que envolvem escores de propensao exigem duas an lises
1. Construir um modelo para estimar o escore de propensao para cada indiv duo
2. Utilizar o escore de propensao para a ustar para vi s de confusao quando estimar o
efeito de tratamento.

22
Todas as variáveis confundidoras devem ser colocados no modelo de escore de pro-
pensão. O desfecho não deve ser utilizado.
Após o ajuste, o modelo será utilizado para estimar o escore de propensão de cada
indivíduo que será utilizado para ajustar para viés de confusão em uma das seguintes formas:
estratificação, pareamento ou ponderação pela probabilidade inversa.
2.5.2 Seleção do modelo e Pareamento das amostras
Foi utilizado o procedimento de pareamento com escore balanceado, computado a par-
tir de um modelo de regressão logística que varia de 0 a 1, refletindo a probabilidade de cada
indivíduo, com base em suas características clínicas, de receber o tratamento de interesse
(propofol).
A seleção do modelo foi realizada por meio de regressão passo a passo, mantendo to-
das as co-variáveis com p <0,20. Este nível de significância foi escolhido para garantir a in-
clusão de todas as variáveis com potencial para influenciar a escolha na administração do
propofol ou do midazolam. Para parear os pacientes com escores de propensão semelhantes,
empregou-se uma correspondência entre os grupos numa proporção de 1:1 sem reposições,
usando-se uma diferença de desvio padrão da ordem 0,1, para o par mais semelhante. Não foi
necessário atingir correspondência exata em nenhuma das variáveis. Se nenhuma correspon-
dência fosse encontrada, o paciente seria removido da análise independente do grupo em que
se encontrava (figura 3).
Foram avaliados o grau de equilíbrio nas co-variáveis medidas entre os grupos nos
dois estudos (propofol vs. midazolam) comparando as distribuições das variáveis categóricas
e contínuas usando o testo do qui-quadrado e o teste t, respectivamente. Diferenças padroni-
zadas, expressas em percentagem do desvio padrão do conjunto das co-variáveis também fo-
ram utilizadas para avaliar o grau de equilíbrio antes e após o pareamento, diferenças norma-
lizados de menos de 0,1 indica que as co-variáveis estão bem equilibradas entre os grupos. A
análise estatística foi realizada usando SPSS 19.0 for Windows.
2.5.3 Variáveis incluídas no escore de Propensão
As co-variadas incluídas foram: sexo, idade, SAPS-I e SOFA não renais à admissão,
comorbidades, tipo de admissão na UTI (clínica, cirúrgica ou cardiológica), diagnóstico de
sepse, ECG, a função renal na internação em UTI (primeiro valor de creatinina sérica dispo-

23
nível), necessidade de drogas vasoativas durante primeiras 48 horas de internação na UTI e
pressão arterial média mediana nas primeiras 48 horas de internação na UTI.
Figura 3. Distribuição do escore de propensão comparando os grupos tratados com midazoram antes e após o
pareamento.
Den
sid
ade
Den
sid
ade
Den
sid
ade
Escore de Propensão
Den
sid
ade
Escore de Propensão
Escore de Propensão Escore de Propensão
Propofol não pareado Propofol pós pareamento
Midazolam pós pareamento Midazolam não pareado

24
O escore de Propensão expressa a probalidade de uma indivíduo receber um determinado tratamento de acordo
com as suas características clínicas, na situação em questão o tratamento é o uso de propofol como sedativo em
infusão contínua. A: Distribuição dos escores de propensão dos pacientes que receberam propofol antes do ba-
lanceamento; B: Distribuição dos escores de propensão dos pacientes que receberam midazolam antes do balan-
ceamento. C: Distribuição dos escores de propensão dos pacientes que receberam propofol após o balanceamen-
to; D: Distribuição dos escores de propensão dos pacientes que receberam midazolam após balanceamento. Os
pacientes que receberam o propofol como sedativo, tinham elevada probabilidade de receber tal tratamento antes
do balanceamento estatístico. Parte dos pacientes que fizeram uso do midazolam também tinham uma probabili-
dade elevada de receberem propofol. Após o tratamento estatístico os pacientes de ambos os grupos apresentam
a mesma probabilidade de receberem o propofol. Pode-se dizer que os dois grupos possuem características clíni-
cas extremamente semelhantes e portanto são dois grupos comparáveis.

25
Figura 4. Desenho do estudo

26
3 RESULTADOS
3.1 População em Estudo
O banco de dados do MIMIC-II contém os registros de 32.425 pacientes, dos quais
24.581 eram adultos com idade ≥ 15 anos, no momento da admissão. No total, 1.753 pacien-
tes foram excluídos devido a dados insuficientes de creatinina sérica, outros 3.537 pacientes
foram excluídos por permanência em UTI inferior a 24 h, e outros 538 pacientes foram exclu-
ídos por diagnóstico prévio de DRC avançada. Entre os demais, 9.697 deles receberam propo-
fol e/ou midazolam nas primeiras 48 horas após a internação na UTI. Foram excluídos mais
de 863 pacientes que receberam ambos propofol e midazolam. Finalmente, uma amostra total
de 8.834 pacientes receberam propofol ou midazolam nas primeiras 48 horas de internação na
UTI - Figura 4. O Propofol foi o sedativo mais utilizado na população em estudo, compreen-
dendo 91,7% dos pacientes.
Antes do pareamento, os pacientes que receberam propofol eram mais jovens, tinham
menos comorbidades e menor creatinina sérica à admissão na UTI. Estas diferenças são, pro-
vavelmente, devido a diferentes tipos admissão do paciente: mais da metade dos pacientes que
receberam propofol eram cirúrgicos (cirurgia cardíaca ou não cardíaca) e 49% dos pacientes
que receberam midazolam foram internações clínicas. Uma descrição completa dos parâmetro
de base para a coorte desemparelhada encontra-se na tabela 1.
Tabela 1 - Características clínicas da população em estudo, Propofol x Midazolam, antes e após
pareamento das amostras
Coorte não pareada Coorte após pareamento
Variável Propofol
(n = 8099) Midazolam (n
= 735) P
Propofol
(n = 703) Midazolam (n
= 703) P
Idade (anos)
média ± DP 62,2 ± 16,9 66,1 ± 17,0 <0,001 65,4 ± 16,5 66,0 ± 17,2 0,507
Sexo
masculino, n
(%)
5099 (63) 395 <0,001 374 (53,2) 377 (53,6) 0,873
HAS, n (%) 2425 (29,9) 227 (30,9) 0,594 204 (29) 215 (30,6) 0,521
DM, n (%) 1597 (19,7) 179 (24,4) 0,003 170 (24,2) 168 (23,9) 0,901
ICC, n (%) 1096 (13,5) 276 (37,6) <0,001 252 (36,3) 252 (36,7) 0,739

27
Tabela 1 - Características clínicas da população em estudo, Propofol x Midazolam, antes e após
pareamento das amostras
Coorte não pareada Coorte após pareamento
Variável Propofol
(n = 8099) Midazolam (n
= 735) P
Propofol
(n = 703) Midazolam (n
= 703) P
DPOC, n (%) 1158 (14,3) 199 (27,1) <0,001 170 (24,2) 186 (26,5) 0,326
Hepatopatias,
n (%) 339 (4,2) 57 (7,8) <0,001 56 (8,0) 56 (8,0) 1,0
Tumores
Sólidos, n (%) 1075 (13,3) 132 (18,0) <0,001 129 (18,3) 124 (17,6) 0,728
Doenças
Neurológicas,
n (%)
217 (2,7) 50 (6,8) <0,001 47 (7) 46 (6,5 0,750
Obesidade, n
(%) 186 (2,3) 17 (2,3) 0,977 15 (2,1) 17 (2,4) 0,721
Admissão na
UTI, n (%)
Clinica
Cirúrgica
Cardiológica
Cir. Cardíaca
2321 (25,9)
4832 (20,9)
1244 (13,9)
557 (6,2)
366 (49,3)
155 (20,9)
207 (27,9)
15 (2,0)
<0,001
355 (50,5)
132 (18,8)
201 (28,6)
15 (2,1)
337 (47,9)
154 (21,9)
197 (28,0)
15 (2,1)
0,532
Sepse, n (%) 362 (4,0) 192 (25,8) <0,001 130 (18,5) 154 (21,9) 0,111
SAPS, média
(IQR) 16 (13 - 19) 18 (15 - 21) <0,001 17 (14 - 20) 17 (14 - 18) 0,320
SOFA não-
renal, média
(IQR)
6,5 ± 3,5 7,32 ± 3,9 <0,001 7 (4 - 10) 7 (5 - 10) 0,358
ECG, média
(IQR) 6 (3 - 10) 9 (6 - 14) <0,001 7 (3 - 11) 8 (3 - 12) 0,296
PAM 48h
(mmHg),
média ± DP
78,8 ± 9,5 76,6 ± 10,1 <0,001 77,4 ± 9,7 76,7 ± 10,1 0,380
DVA 48 h, n
(%) 4139 (51,8) 309 (42) <0,001 283 (40,3) 297 (42,2) 0,448
CrS admissão
(mg/dl), média
(IQR)
0,8 (0,7 - 1,1) 1,2 (0,8 - 2,0) <0,001 1,1 (0,8 - 1,7) 1,2 (0,8 - 1,8) 0,316
Dependência
de VM, n (%)
às 48 h
aos 7 dias
2219 (27,4)
1628 (20,1)
398 (54,1)
322 (42,8)
<0,001
374 (53,2)
272 (38,7)
367 (52,2)
287 (40,8)
0,236

28
Tabela 1 - Características clínicas da população em estudo, Propofol x Midazolam, antes e após
pareamento das amostras
Coorte não pareada Coorte após pareamento
Variável Propofol
(n = 8099) Midazolam (n
= 735) P
Propofol
(n = 703) Midazolam (n
= 703) P
DP: desvio padrão; HAS: hipertensão arterial, sistêmica; DM: diabetes mellitus; ICC: insuficiência
cardíaca congestiva; DPOC: doença pulmonar obstrutiva crônica; UTI: unidade de terapia intensiva;
SAPS: simplified acute physiology ocorre; SOFA: sequential organ failure assessment; IQR:
interquatile range; ECG: escala de coma de glasgow; PAM 48 h: pressão arterial média nas primeiras
48 horas; DVA 48 h: uso de drogas vasoativas nas primeiras 48 horas; VM: ventilação mecânica.
3.2 Coorte Balanceada
Após realização da emparelhamento 1:1 para as variáveis correspondentes pré-
tratamento, havia 703 pacientes tratados com propofol pareados com 703 doentes tratados
com midazolam - Tabela 1. Todos os dados demográficos, clínicos e laboratoriais pré-TRS
foram bem equilibradas entre os grupos após o escore de propensão, como mostra a Tabela 1.
Além disso, a redução do desvio padrão das co-variáveis após realizar o escore de propensão
para cada comparação pode ser visto na figura 2. Deste modo ambos os grupos eram comple-
tamente comparados no que diz respeito a todas as co-variáveis adicionadas ao modelo, sem
necessidade de nenhum ajuste adicional para análise dos desfechos.
Os pacientes tratados com propofol receberam uma dose média de infusão de 35,5
mcg/kg/min e a grande maioria (78,5%) recebeu propofol até 72h de internação na UTI.
Quanto pacientes tratados com midazolam, a dose média foi de 0,8 mcg/Kg/min e, como no
grupo propofol, a grande maioria teve seu uso interrompido antes das 72h de internação na
UTI (80,5%).
3.3 Desenvolvimento lesão renal aguda
Embora alguns pacientes possam ter sido internados na UTI com IRA já estabelecida,
a creatinina sérica da admissão foi utilizada como valor de referência para avaliar IRA de
novo ou agravamento de IRA após uso de propofol ou midazolam. Após o balanceamento, os
pacientes em uso de propofol possuíam níveis de creatinina sérica admissionais semelhantes

29
aos dos pacientes em uso de midazolam. Apenas 178 (12,7%) pacientes foram classificados
com base apenas na creatinina sérica (sem diferença significativa entre os grupos).
Durante os primeiros 7 dias de internação na UTI, mais pacientes tratados com mida-
zolam desenvolveram AKI. Ao considerar os dois critérios (débito de urinário e creatinina
sérica), o propofol foi associada com uma redução significativa na incidência de LRA, com
um risco relativo de 0,585 (IC 95% ,471-,726). A proteção relacionada ao propofol foi obser-
vada independente do critério utilizado para o diagnóstico da IRA, débito urinário (OR 0,637,
IC 95% 0,516-0,786) e creatinina sérica (OR 0,683, 95% CI ,546-0,854). A redução no odds
ratio associada ao uso do propofol foi observada nas fases mais graves da IRA (2 e 3) -figura
5. Como mostrado na Figura 3, houve uma protecção semelhante associada ao propofol entre
os estágios da IRA independente do critério utilizado para diagnóstico de IRA.
Figura 5. Incidência de LRA nos pacientes em uso de propofol e midazolam e estratificação conforme o estadi-
amento da LRA.
Os pacientes que receberam sedação com propofol apresentaram menor incidência de LRA aos sete dias, bem
como apresentaram menor incidência das formas mais graves, LRA KDIGO 2 e 3.

30
Figura 6. Odds ratio para LRA, conforme estágio da LRA (por nível de CrS e débito urinário).
O propofol possui efeito protetor para os estágios 2 e 3 independente do critério diagnóstico utilizado, com redu-
ção da probabilidade de LRA quando utilizou-se o critério da diurese ou o critério da elevação da creatinina
sérica para classificação da LRA.
3.4 Oliguria, diurético Use e equilíbrio hídrico acumulado
Tabela 2 - Avaliação dos desfechos em ambos os grupos após o balanceamento estatístico.
Desfecho Midazolam
(n=703) Propofol
(n=703)
P Odds-ratio (95 %
CI)
Oligúria
< 400 ml/dia) 124/632
(19,6 %) 73/596
(12,2 %) <0,001 0,572 (0,418 -
0,783)
Uso de diuréticos 100 (14,2 %) 60 (8,5 %) 0,001
BH acumulado > 5%
Peso seco 412 (60,7 %) 353 (53 %) 0,004 0,731 (0,589 -
0,908)
TRS 41 (5,8 %) 24 (3,4 %) 0,031 0,571 (0,341 -
0,955)
Mortalidade na UTI 209 (29,7 %) 102 (14,5 %) <0,001 0,401 (0,308 -
0,870)
CI: confidence interval; BH: balanço hídrico; TRS: terapia renal substitutiva; UTI: unidade de terapia
intensiva

31
Os pacientes que receberam propofol tiveram oligúria com menor frequência (12,2 vs.
19,6%, p <0,001) e diuréticos foram prescritos com menos frequência (8,5 vs 14,2%, p =
0,001). Além disso, durante os primeiros 7 dias de internação na UTI, os pacientes que rece-
beram propofol atingiram com menor frequencia o balanço hídrico acumulado superior a 5%
do peso corporal (50,2 vs. 58,6, p = 0,002). Os dados completos da odds ratio relativos a estes
resultados são mostrados na tabela 2.
3.5 Terapia de substituição renal
Levando em consideração apenas os primeiros 7 dias de internação na UTI, houve
uma redução discreta, mas significativa da necessidade de TRS associada ao tratamento com
propofol (3,4 vs. 5,8%, p = 0,031, OR 0,571 IC 95% ,341-,955).
3.6 Tempo de permanência na UTI e mortalidade
Nos pacientes pareados, houve uma tendência à redução no tempo de permanência na
UTI nos pacientes tratados com propofol (8,2 ± 4,8 vs 9,1 ± 5,3 dias, p = 0,052). A mortalida-
de na UTI foi inferior nos pacientes tratados com propofol (14,5 vs 29,7%, p <0,001).

32
4 DISCUSSÃO
Neste estudo de coorte retrospectivo com pacientes críticos em ventilação mecânica,
foram selecionadas duas amostras emparelhadas de pacientes tratados com um único sedativo
nas primeiras 48 horas de internação na UTI. Nesta população balanceada de pacientes, o uso
de propofol esteve associado a uma redução significativa do risco de desenvolver IRA e ou-
tros desfechos renais importantes. Os resultados desta análise de escore de propensão, contro-
lada para importantes variáveis pré-tratamento e para a dependência de ventilação mecânica,
são reforçados por estudos prévios em animais (ABE, 2006; YANG; CHOU; PEI, 2013) e um
pequeno mas relevante ensaio clínico randomizado com pacientes submetidos a cirurgia car-
díaca valvar (YOO et al., 2014).
O propofol é um agente largamente utilizado para a indução e manutenção de aneste-
sia geral e para a sedação de pacientes críticos em ventilação mecânica, possui propriedades
anti-oxidantes e anti-inflamatórias (RODRÍGUEZ-LÓPEZ et al., 2006; MURPHY et al.,
1992). O tratamento com propofol pode inibir as citocinas pró-inflamatórias em modelos a-
nimais sépticos e também em pacientes sépticos (RODRÍGUEZ-LÓPEZ et al., 2006; SONG
et al., 2009; TSAO et al., 2005). Os efeitos benéficos do propofol sobre o rim foram demons-
trados tanto em modelos animais de isquemia / reperfusão (YANG; CHOU; PEI, 2013) como
em modelos de sepse (HSING et al., 2010). Outro mecanismo proposto para renoproteção
relacionada ao propofol é o aumento na expressão da proteína-7-morfogenética óssea durante
LRA induzida por septicemia em animais.
Embora muitas drogas tenham demonstrado benefícios potenciais na IRA utilizando
modelos animais, nenhum valor clínico foi evidenciado em pacientes sob alto risco de desen-
volver LRA. O propofol está emergindo como uma opção potencial para ser utilizado na prá-
tica clínica devido ao seu efeito potencialmente renoprotetor atingido com a dose recomenda-
da atualmente utilizada para sedaçãoe anestesia. No entanto, os pequenos estudos clínicos
sobre IRA ainda mostram resultados conflitantes. Recentementee o propofol foi associado a
redução na incidencia de IRA em pacientes submetidos a cirurgia cardíaca valvar (YOO et al.,
2014). Este foi um estudo randomizado, bem equilibrado e conduzido; no entanto, o cenário
limitado de condições clínicas (cirurgia cardíaca), pequeno número de pacientes e uma popu-
lação com relativamente poucas comorbidades limita o entusiasmo com tais resultados. Além
disso, há outros estudos que não revelam quaisquer benefícios com propofol (versus anestési-
cos inalatórios) no desenvolvimento de LRA no cenário da cirurgia cardíaca (STORY et al.,
2001; SARICAOĞLU et al., 2006). Ao estudar pacientes cirróticos submetidos à ressecção in

33
vivo randomizados para receber sevoflurano ou propofol como o principal agente anestésico,
Song et al. (2013) também não encontraram diferenças em termos de função renal no pós-
operatório. A extrapolação de tais resultados para pacientes críticos no contexto de uma UTI
geral problemático e podemos portanto, afirmar que os efeitos renais de propofol como agente
sedativo na terapia intensiva permanecem completamente desconhecidos
No presente estudo, pacientes críticos sob ventilação mecânica recebendo propofol
como agentes sedativo de manutenção durante as primeiras 48 horas de admissão na UTI fo-
ram pareados com pacientes em uso de midazolam no mesmo contexto clínico. Após o pare-
amento, as duas amostras de pacientes eram altamente semelhantes no que concerne às suas
características clínicas iniciais. Além dos dados clínicos iniciais e das variáveis no momento
da admissão na UTI, também foram incluídos na análise parâmetros dinâmicos no que diz
respeito aos dados hemodinâmicos (média da PAM e uso de drogas vasoativas) que poderiam
ter interferido na escolha do agente sedativo. No intuito de excluir os eventos renais tardios
durante a internação na UTI, que poderiam não estar diretamente associado com a escolha
inicial sedação, a ocorrência dos desfechos renais foi limitada até os primeiros 7 dias de inter-
nação na UTI. Notavelmente, houve uma redução em todos os desfechos renais adversos es-
tudados, incluindo necessidade de TRS.
Uma vez que alguns pacientes já foram internados na UTI com LRA estabelecida ou
em curso, a primeira medição da creatinina sérica após a admissão na UTI foi utilizada como
valor de referência para a creatinina de base. Ao utilizar-se esta definição, certamente avalia-
se apenas os casos novos LRA desenvolvidos ou agravados após o início da sedação. O efeito
protetor do propofol no que diz respeita à incidência da IRA foi observado sobretudo nos es-
tágios mais graves (2 e 3), os resultados foram muito semelhantes ao usar CrS ou o DU. A
elevação do balanço hídrico acumulado, outra característica associada à elevação da mortali-
dade na UTI, foi menos frequente entre os pacientes em uso de propofol, mesmo que esses
pacientes tenham recebido menos diuréticos que o grupo em uso de midazolam. Neste estudo,
preferiu-se utilizar um ponto de corte menor do que o comumente usado para definir o balan-
ço hídrico acumulado (5% do peso vivo), pois avaliou-se apenas os primeiros 7 dias de inter-
nação na UTI.
Tal como referido acima, outros estudos que avaliam os efeitos do propofol sobre a
função renal foram realizadas durante a anestesia cirúrgica. Há algumas diferenças primordi-
ais na administração de propofol como sedativo em pacientes críticos ou como agente anesté-
sico indutor durante a cirurgia. A velocidade de infusão na presente coorte foi apenas um ter-
ço da que foi utilizada no estudo randomizado realizado por Yoo et al. (2014) durante a cirur-

34
gia cardíaca valvar. No entanto, esta taxa de infusão reduzida pode ser contrabalançada pelo
tempo de infusão mais prolongada realizada nos pacientes críticos em ventilação mecânica.
Este possui vários pontos fortes. Primeiro, foi avaliado um banco de dados grande e
detalhado de pacientes graves. Isso permitiu a seleção de dois grandes grupos de pacientes
com quadros clínicos distintos. As informações detalhadas fornecidas por este banco de dados
são de extrema importância, uma vez que tornam possível expandir as características basais
além do que é possível com um banco de dados administrativo. Por exemplo, foi possível
parear e avaliar os pacientes no que diz respeito a creatinina sérica na admissão, a média da
PAM e uso de drogas vasoativas nas primeiras 48h de internação na UTI, dose média dos
sedativos e seu tempo de uso. Este pareamento criterioso aumenta a confiabilidade dos resul-
tados avaliados.
O presente estudo também tem limitações. Apesar de mais de oito mil pacientes rece-
beram propofol nas primeiras 48h de internação na UTI, houve limitação pelo número relati-
vamente baixo de pacientes que receberam midazolam. A limitação mais importante é a natu-
reza retrospectiva do estudo. Embora tenha-se tentado realizar um pareamento detalhado e
criterioso, é possível que características basais incompletas possam ter influenciado os resul-
tados. Além disso, algumas persistem algumas dúvidas se a dose do propofol administrada ou
o tempo de uso da droga podem de fato diminuir a LRA. Estas perguntas podem ser respondi-
das apenas com ensaios clínicos randomizados.

35
5 CONCLUSÃO
Em conclusão, este estudo demonstrou, em uma grande coorte de pacientes graves em
ventilação mecânica, que a sedação o propofol foi associada a menor incidência de desfechos
renais adversos renais, inclusive graves, como, necessidade de TRS. Isso reforça o uso do
propofol como um dos agentes sedativos de primeira escolha em pacientes sob ventilação
mecânica e fornece provas para realizar ensaios clínicos randomizados utilizando propofol
como um agente promissor e clinicamente disponível, não só no cenário do paciente crítico,
mas também em outras condições clínicas associadas com alto risco de desenvolver LRA.

36
REFERÊNCIAS
ABE, J.-I. Bone morphogenetic protein (BMP) family, SMAD signaling and Id helix-loop-
helix proteins in the vasculature: the continuous mystery of BMPs pleotropic effects. J. Mol.
Cell. Cardiol., v. 41, n. 1, p. 4-7 , July 2006.
ARABI, Y.; HADDAD, S.; HAWES, R.; MOORE, T.; PILLAY, M.; NAIDU, B.; ISSA, A.;
YENI, B.; GRANT, C.; ALSHIMEMERI, A. Changing sedation practices in the intensive
care unit--protocol implementation, multifaceted multidisciplinary approach and teamwork.
Middle East J. Anaesthesiol., v. 19, n. 2, p. 429-447, June 2007.
ARIAS-RIVERA, S.; SÁNCHEZ-SÁNCHEZ, M. DEL M.; SANTOS-DÍAZ, R.; GALLAR-
DO-MURILLO, J.; SÁNCHEZ-IZQUIERDO, R.; FRUTOS-VIVAR, F.; FERGUSON, N. D.;
ESTEBAN, A. Effect of a nursing-implemented sedation protocol on weaning outcome. Crit.
Care Med., v. 36, n. 7, p. 2054-2060, July 2008.
BAGSHAW, S. M.; GEORGE, C.; BELLOMO, R. A comparison of the RIFLE and AKIN
criteria for acute kidney injury in critically ill patients. Nephrol. Dial. Transplant., v. 23, n.
5, p. 1569-1574 , May 2008.
BARASH, P. G. Clinical anesthesia. [S.l.]: Lippincott Williams & Wilkins, 2009.
BARR, J.; FRASER, G. L.; PUNTILLO, K.; ELY, E. W.; GÉLINAS, C.; DASTA, J. F.;
DAVIDSON, J. E.; DEVLIN, J. W.; KRESS, J. P.; JOFFE, A. M.; COURSIN, D. B.; HERR,
D. L.; TUNG, A.; ROBINSON, B. R.; FONTAINE, D. K.; RAMSAY, M. A.; RIKER, R. R.;
SESSLER, C. N.; PUN, B.; SKROBIK, Y.; JAESCHKE, R. Clinical practice guidelines for
the management of pain, agitation, and delirium in adult patients in the intensive care unit.
Crit. Care Med., v. 41, n. 1, p. 263-306, Jan. 2013.
BARRANTES, F.; TIAN, J.; VAZQUEZ, R.; AMOATENG-ADJEPONG, Y.; MANTHOUS,
C. A. Acute kidney injury criteria predict outcomes of critically ill patients. Crit. Care Med.,
v. 36, n. 5, p. 1397-1403, May 2008.
CARSON, S. S.; KRESS, J. P.; RODGERS, J. E.; VINAYAK, A.; CAMPBELL-BRIGHT,
S.; LEVITT, J.; BOURDET, S.; IVANOVA, A.; HENDERSON, A. G.; POHLMAN, A.;
CHANG, L.; RICH, P. B.; HALL, J. A randomized trial of intermittent lorazepam versus
propofol with daily interruption in mechanically ventilated patients. Crit. Care Med., v. 34,
n. 5, p. 1326-1332, May 2006.
DOS SANTOS, C. B.; PORTELLA, A. A. V. Estrutura Química.
ELY, E. W.; SHINTANI, A.; TRUMAN, B.; SPEROFF, T.; GORDON, S. M.; HARRELL
JR, F. E.; INOUYE, S. K.; BERNARD, G. R.; DITTUS, R. S. Delirium as a predictor of mor-
tality in mechanically ventilated patients in the intensive care unit. JAMA, v. 291, n. 14, p.
1753-1762, Apr. 2004.
FLOEGE, J.; JOHNSON, R. J.; FEEHALLY, J. Comprehensive clinical nephrology. [S.l.]:
Elsevier Health Sciences, 2010.

37
GIRARD, T. D.; KRESS, J. P.; FUCHS, B. D.; THOMASON, J. W.; SCHWEICKERT, W.
D.; PUN, B. T.; TAICHMAN, D. B.; DUNN, J. G.; POHLMAN, A. S.; KINNIRY, P. A.;
JACKSON, J. C.; CANONICO, A. E.; LIGHT, R. W.; SHINTANI, A. K.; THOMPSON, J.
L.; GORDON, S. M.; HALL, J. B.; DITTUS, R. S.; BERNARD, G. R.; ELY, E. W. Efficacy
and safety of a paired sedation and ventilator weaning protocol for mechanically ventilated
patients in intensive care (Awakening and Breathing Controlled trial): a randomised con-
trolled trial. Lancet, v. 371, n. 9607, p. 126-134, Jan. 2008.
GOODMAN, L. S. Goodman and Gilman's: the pharmacological basis of therapeutics. New
York: McGraw-Hill, 1996.
GREEN, T. R.; BENNETT, S. R.; NELSON, V. M. Specificity and properties of propofol as
an antioxidant free radical scavenger. Toxicol. Appl. Pharmacol., v. 129, n. 1, p. 163-169,
Nov. 1994.
GREENBLATT, D. J.; HARMATZ, J. S.; SHADER, R. I. Clinical pharmacokinetics of anxi-
olytics and hypnotics in the elderly. Therapeutic considerations (Part II). Clin. Pharmacoki-
net., v. 21, n. 4, p. 262-273, Oct. 1991.
HO, K. M.; NG, J. Y. The use of propofol for medium and long-term sedation in critically ill
adult patients: a meta-analysis. Intensive Care Med., v. 34, n. 11, p. 1969-1979, Nov. 2008.
HOSTE, E. A. J.; CLERMONT, G.; KERSTEN, A.; R VENKATARAMAN; ANGUS , D.
C.; DE BACQUER, D.; KELLUM, J. A. RIFLE criteria for acute kidney injury are associated
with hospital mortality in critically ill patients: a cohort analysis. Crit. Care, v. 10, n. 3, p.
R73, 2006.
HSING, C.-H.; CHOU, W.; WANG, J. J.; CHEN, H. W.; YEH, C. H. Propofol increases bone
morphogenetic protein-7 and decreases oxidative stress in sepsis-induced acute kidney injury.
Nephrol. Dial. Transplant., v. 26, n. 4, p. 1162-1172, 2011.
JACOBI, J.; FRASER, G. L.; COURSIN, D. B.; RIKER, R. R.; FONTAINE, D.; WITT-
BRODT, E. T.; CHALFIN, D. B.; MASICA, M. F.; BJERKE, H. S.; COPLIN, W. M.; CRIP-
PEN, D. W.; FUCHS, B. D.; KELLEHER, R. M.; MARIK, P. E.; NASRAWAY JR, S. A.;
MURRAY, M. J.; PERUZZI, W. T.; LUMB, P. D. Clinical practice guidelines for the sus-
tained use of sedatives and analgesics in the critically ill adult. Crit. Care Med., v. 30, n. 1,
p. 119-141, Jan. 2002.
KINSEY, G. R.; OKUSA, M. D. Pathogenesis of acute kidney injury: foundation for clinical
practice. Am. J. Kidney Dis., v. 58, n. 2, p. 291-301, Aug. 2011.
KOLLEF, M. H.; LEVY, N. T.; AHRENS, T. S.; SCHAIFF, R.; PRENTICE, D.; SHER-
MAN, G. The use of continuous i.v. sedation is associated with prolongation of mechanical
ventilation. Chest, v. 114, n. 2, p. 541-548, Aug. 1998.
LEITE, T. T.; MACEDO, E.; PEREIRA, S. M.; BANDEIRA, S. R.; PONTES, P.
H.; GARCIA, A. S.; MILITÃO, F. R.; MELO SOBRINHO, I. M.; ASSUNÇÃO, L. M.; LI-
BÓRIO, A. B. Timing of renal replacement therapy initiation by AKIN classification system.
Crit. Care, v. 17, n. 2, p. R62, 2013.

38
LEVIN, A.; STEVENS, P. E. Summary of KDIGO 2012 CKD Guideline: behind the scenes,
need for guidance, and a framework for moving forward. Kidney Int., v. 85, n. 1, p. 49-61,
2014.
LONARDO, N. W.; MONE, M. C.; NIRULA, R.; KIMBALL, E. J.; LUDWIG, K.; ZHOU,
X.; SAUER, B. C.; NECHODOM, K.; TENG, C.; BARTON, R. G. Propofol Is Associated
with Favorable Outcomes Compared with Benzodiazepines in Ventilated Intensive Care Unit
Patients. Am. J. Respir. Crit. Care Med., v. 189, n. 11, p. 1383-1394, 2014.
LOPES, R. D.; HARRINGTON, R. A. Compreendendo a pesquisa clínica. [S.l.]: McGraw
Hill Brasil, 2015.
MACEDO, E.; MALHOTRA, R.; CLAURE-DEL GRANADO, R.; FEDULLO, P.; MEHTA,
R. L. Defining urine output criterion for acute kidney injury in critically ill patients. Nephrol.
Dial. Transplant., v. 26, n. 2, p. 509-515, Feb. 2011.
MARTIN, J.; FRANCK, M.; SIGEL, S.; WEISS, M.; SPIES, C. Changes in sedation man-
agement in German intensive care units between 2002 and 2006: a national follow-up survey.
Crit. Care, v. 11, n. 6, p. R124, 2007.
MURPHY, P. G.; MYERS, D. S.; DAVIES, M. J.; WEBSTER, N. R.; JONES, J. G. The an-
tioxidant potential of propofol (2,6-diisopropylphenol). Br. J. Anaesth., v. 68, n. 6, p. 613-
618, June 1992.
MURUGAN, R.; KELLUM, J. A. Acute kidney injury: what's the prognosis? Nat. Rev.
Nephrol., v. 7, n. 4, p. 209-217, Apr. 2011.
PAYEN, J.-F.; CHANQUES, G.; MANTZ, J.; HERCULE, C.; AURIANT, I.; LEGUILLOU,
J. L.; BINHAS, M.; GENTY, C.; ROLLAND, C.; BOSSON, J. L. Current practices in seda-
tion and analgesia for mechanically ventilated critically ill patients: a prospective multicenter
patient-based study. Anesthesiology, v. 106, n. 4, p. 687-95; quiz 891-892, Apr. 2007.
REWA, O.; BAGSHAW, S. M. Acute kidney injury-epidemiology, outcomes and economics.
Nature Rev. Nephrol., v. 10, n. 4, p. 193-207, Apr. 2014.
RODRÍGUEZ-LÓPEZ, J. M.; SÁNCHEZ-CONDE, P.; LOZANO, F. S.; NICOLÁS, J. L.;
GARCÍA-CRIADO, F. J.; CASCAJO, C.; MURIEL, C. Laboratory investigation: effects of
propofol on the systemic inflammatory response during aortic surgery. Can. J. Anaesth., v.
53, n. 7, p. 701-710, July 2006.
SAEED, M.; VILLARROEL, M.; REISNER, A. T.; CLIFFORD, G.; LEHMAN, L. W.;
MOODY, G.; HELDT, T.; KYAW, T. H.; MOODY, B.; MARK, R. G. Multiparameter Intel-
ligent Monitoring in Intensive Care II (MIMIC-II): a public-access intensive care unit data-
base. Crit. Care Med., v. 39, n. 5, p. 952, 2011.
SARICAOĞLU, F.; AKINCI, S. B.; OÇ, B.; KANBAK, M.; AKBULUT, B.; CELEBI-
OGLU, B. The effect of halothane, isoflurane, sevoflurane and propofol infusion on renal
function after coronary artery bypass surgery. Middle East J. Anaesthesiol., v. 18, n. 5, p.
955-964 , June 2006.

39
SINGBARTL, K.; KELLUM, J. A. AKI in the ICU: definition, epidemiology, risk stratifica-
tion, and outcomes. Kidney Int., v. 81, n. 9, p. 819-825, May 2012.
SONG, J-C.; ZHANG, M. Z.; WU, Q. C.; LU, Z. J.; SUN, Y. M.; YANG, L. Q.; YU, W. F.
Sevoflurane has no adverse effects on renal function in cirrhotic patients: a comparison with
propofol. Acta Anaesthesiol. Scand., v. 57, n. 7, p. 896-902, Aug. 2013.
SONG, X.-M.; WANG, Y. L.; LI, J. G.; WANG, C. Y.; ZHOU, Q.; ZHANG, Z. Z.; LIANG,
H. Effects of propofol on pro-inflammatory cytokines and nuclear factor kappaB during
polymicrobial sepsis in rats. Mol. Biol. Rep., v. 36, n. 8, p. 2345-2351, Nov. 2009.
STORY, D. A.; POUSTIE, S.; LIU, G.; MCNICOL, P. L. Changes in plasma creatinine con-
centration after cardiac anesthesia with isoflurane, propofol, or sevoflurane: a randomized
clinical trial. Anesthesiology, v. 95, n. 4, p. 842-848, Oct. 2001.
SUSANTITAPHONG, P. et al. World incidence of AKI: a meta-analysis. Clin. J. Am. Soc.
Nephrol., v. 8, n. 9, p. 1482-1493, Sept. 2013.
TAAL, M. W.; CHERTOW, G. M.; MARSDEN, P. A.; SKORECKI, K.; ALAN, S. L.;
BRENNER, B. M. Brenner and Rector's the kidney. [S.l.]: Elsevier Health Sciences, 2011.
THUMMEL, K. E.; O'SHEA, D.; PAINE, M. F.; SHEN, D. D.; KUNZE, K. L.; PERKINS, J.
D.; WILKINSON, G. R. Oral first-pass elimination of midazolam involves both gastrointesti-
nal and hepatic CYP3A-mediated metabolism. Clin. Pharmacol. Therap., v. 59, n. 5, p. 491-
502, May 1996.
TREGGIARI, M. M.; ROMAND, J. A.; YANEZ, N. D.; DEEM, S. A.; GOLDBERG, J.;
HUDSON, L.; HEIDEGGER, C. P.; WEISS, N. S. Randomized trial of light versus deep se-
dation on mental health after critical illness. Crit. Care Med., v. 37, n. 9, p. 2527-2534, Sept.
2009.
TSAO, C.-M.; WU, C. C.; WANG, J. J.; WONG, C. S.; TSAI, S. K.; HO, S. T. Intravenous
anesthetics in sepsis. Acta Anaesthesiol. Taiwan, v. 43, n. 3, p. 153-163, Sept. 2005.
YANG, S.; CHOU, W.-P.; PEI, L. Effects of propofol on renal ischemia/reperfusion injury in
rats. Exp. Ther. Med., v. 6, n. 5, p. 1177-1183, Nov. 2013.
YOO, Y.-C.; SHIM, J. K.; SONG, Y.; YANG, S. Y.; KWAK, Y. L. Anesthetics influence the
incidence of acute kidney injury following valvular heart surgery. Kidney Int., v. 86, n. 2, p.
414-422, Aug. 2014.
YOUNG, C C; PRIELIPP, R C. Benzodiazepines in the intensive care unit. Critical care clin-
ics, United States, v. 17, n. 4,843-62 , Out 2001.