Prof Márcio Bandeira interações intermoleculares e funções inorgânicas
Click here to load reader
-
Upload
colegio-estadual-paulo-freire -
Category
Education
-
view
7.844 -
download
0
Transcript of Prof Márcio Bandeira interações intermoleculares e funções inorgânicas

Interações
Intermoleculares
Profº Márcio Bandeira

• A polaridade da moléculas;• Moléculas polares.
• Moléculas apolares.

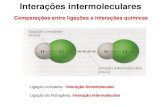
Força intermolecular (Forças de Van der Waals)
Quando duas moléculas se aproximam há
uma interação de seus campos magnéticos
o que faz surgir uma força entre elas. É o
que chamamos de força intermolecular.
Essas forças variam de
intensidade, dependendo do tipo da
molécula (polar ou apolar) e, no caso das
polares, de quão polares elas são.

EXEMPLOS
H Cl H Cl
H2S H2S
SO2 SO2

Vamos ver então como são as forças quando aproximamos:
Íon x molécula polar: É a força mais forte e sua magnitude
pode ser compatível a de uma ligação covalente.

Molécula polar x molécula polar: Ocorre entre moléculas polares
da mesma substância ou de substâncias diferentes, ambas polares.
Esta força é muito conhecida como dipolo x dipolo ou dipolo-
permanente.

Ligações de hidrogênio: Quando ligado a um átomo pequeno e de
forte eletronegatividade (F, O ou N), o hidrogênio forma ligações
polares muito fortes. Seus pólos interagirão fortemente com outras
moléculas polares, formando uma forte rede de ligações
intermoleculares.

Molécula polar x molécula apolar: Conhecida como interação
dipolo x dipolo induzido, ocorrem porque moléculas polares (dipolos
permanentes) conseguem distorcer a distribuição de carga em outras
moléculas vizinhas, através de polarização induzida. Uma interação
desse tipo é uma interação fraca.

Propriedades das Substâncias em Solução Aquosa
Diferentes substâncias apresentam diferentes comportamentos
quando colocadas na presença de um solvente. Algumas se
dissolvem, outras não. Dentre aquelas que dissolvem, dois processos
são bastante importantes: dissociação e ionização
A dissociação e ionização resultam em soluções que possuem uma
característica comum: liberam íons na água, mas a origem desses
íons é que diferencia um processo do outro.

Dissociação iônica
Nesse caso, em que já existiam íons e apenas os
separamos, chamamos o processo de dissociação iônica, pois
tudo o que fizemos, repito, foi separar íons pré-existentes. É o que
acontece com os sais e as bases.
NaCl = Na+ + Cl-
CaCO3 = Ca2+ + CO32-
NaHCO3 = Na+ + HCO3-
LiOH = Li+ + OH-
Al(OH)3 = Al3+ + 3OH-
Importante: Compostos iônicos sofrem dissociação quando em
solução e quando fundidos.

Ionização
Alguns compostos moleculares, como os ácidos, quando colocados
em um solvente são "atacados" por esse solvente e acabam
formando íons. Perceba claramente que não existiam íons na
molécula original. Quando ela foi colocada na presença do
solvente, este conseguiu, por força magnética, "arrancar" um ou
mais de seus átomos mas, nesse processo, o átomo arrancado acaba
tendo que deixar um elétron para trás, tornando-se um íon.
Nesses casos, dizemos que houve uma ionização, pois uma
molécula que não possuía originalmente íons passa a tê-los (livres
no solvente). É o que acontece com os ácidos.
HCl = H+ + Cl-
H2SO4 = 2H+ + SO42-
H3CCOOH = H+ + H3>CCOO-
Importante: Substâncias moleculares
que sofrem ionização só o fazem
quando em solução. O processo não
ocorre quando essas substâncias
estão fundidas.

O que você deve lembrar
Ácidos: por serem compostos moleculares, sofrem ionização
quando em solução.
Sais e bases: por serem compostos iônicos, sofrem dissociação
quando em solução ou fundidos.
Segundo Arrhenius (1887), os ácidos são substâncias que ionizam
fornecendo íons H+, e bases são substâncias que dissociam em
íons OH-, ambos na presença de água.
Sal de Arrhenius - Composto resultante da neutralização de um
ácido por uma base, com eliminação de água. É formado por um
cátion proveniente de uma base e um ânion proveniente de um
ácido.
Óxido - Composto binário de oxigênio com outro elemento
menos eletronegativo.

Exemplo: HCl - ácido clorídrico
ÁCIDOS
HCl(g) + H2O H+(aq) + Cl-(aq)
HCl(g) + H2O H3O+(aq) + Cl-(aq)
Força dos Ácidos (segundo Arrhenius)
Um ácido forte é aquele que se ioniza completamente na
água, isto é, libera íons H+, porém não os recebe. O exemplo
anterior (ácido clorídrico) é um ácido forte. Outro é o ácido
nítrico.
Um ácido fraco também libera íons H+, porém
parcialmente, estabelecendo um equilíbrio químico. A maioria
dos ácidos orgânicos são deste tipo, e também alguns sais como
o cloreto de alumínio.

Ao tratar de hidrácidos:
São fortes os ácidos HCl, HBr e HI. HF é o único
moderado e os demais são ácidos fracos.
Ao tratar de Oxiácidos:
Considere a notação geral: Hx(Elemento)Oy. Teremos um
ácido forte se: y - x >= 2 (y - x > 1). Um ácido moderado
se: y - x = 1 . Um ácido fraco se: y - x = 0 (y = x)

Classificação dos ácidos
Quanto ao número de hidrogênios ionizáveis
Monácidos - liberam um íon H+ por molécula: HCl, HNO3,
HClO4, etc.
Diácidos - liberam dois íons H+ por molécula: H2S, H2CO3,
H2SO4, etc.
Triácidos - liberam três íons H+ por molécula: H3BO3, H3PO4,
H3SO4, etc.
Tetrácidos - liberam quatro íons H+ por molécula: H4P2O7,
H4SiO4, etc.
Quanto a presença de oxigênio
Hidrácidos: sem oxigênio (fórmula geral: HnA)
Oxiácidos: com oxigênio (formula geral: HnA0)

Quanto a força
N é o número de moléculas que foram ionizadas pelo número total
de moléculas. Força:
Forte: Grau de ionização acima de 50%
Semi-forte: Grau de ionização entre 30% a 50%
Fraco: Grau de ionização de 10% a 30%
Semi-fraco: Grau de ionização de 4% a 10%
Superfraco: Grau de ionização de 1% a 4%
Insignificante: Grau de ionização até 1%
Quanto a volatilidade
Fixos: H2SO4, H3PO4, H3BO3, H3PO3
Voláteis : HCl, HBr, HI, H2S, HCN, HNO3, entre outros.
Classificação dos ácidos

Quanto ao número de grupos funcionais (H+)
Monopróticos: H3PO2
Dipróticos: H2S, H2Cr2O7, H2MnO4, H3PO3, etc.
Quanto ao grau de hidratação
Orto: Ácido hidratado: H3PO4 (Fosfórico)
Meta: Ácido menos uma molécula de água: H3PO4 - H2O = HPO3
(Metafosfórico)
Piro: 2 ácidos menos uma molécula de água: 2 H3PO4 - H2O =
H4P2O7 (Pirofosfórico)
Classificação dos ácidos

Hidrácidos: Nos ácidos sem oxigênio a nomenclatura é bem
simples, é só seguir a regra abaixo:
Ácido .................. ídrico
nome do elemento
Os nomes dos hidrácidos são formados acrescentando-se a
terminação ídrico às primeiras letras do nome do elemento
químico.
Exemplos:
HCl – ácido clorídrico
HBr – ácido bromídrico
HI – ácido iodídrico
NOMENCLATURA DOS ÁCIDOS

Oxiácidos: Os nomes dos ácidos com oxigênio são dados a partir das reações de
ionização dos mesmos:
Demonstração: faça a reação de ionização do ácido H2CO3.
H2CO3 → 2 H+ + CO3-2
O ânion CO3-2 é denominado de carbonato, a partir desse nome estabeleça uma
comparação seguindo o quadro abaixo:
Tabela de sufixos para Oxiácidos
Ânions Sufixo
ITO oso
ATO ico
Como a terminação de carbonato é ATO, a nomenclatura para o ácido da qual
deriva este ânion será Ácido carbônico (sufixo – ico):
H2CO3 → 2 H+ + CO3-2
Ácido carbônico Carbonato