Modelo Bohr
Click here to load reader
-
Upload
luis-fm-timoteo -
Category
Technology
-
view
15.311 -
download
0
Transcript of Modelo Bohr

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 1
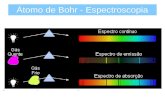
Modelos Atómicos -4Modelo de Bohr
AbsorçãoEmissão

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 2
(1885-1962)
Bohr apresentou alterações ao modelo de Rutherford: Os electrões só podem ocupar níveis de energia bem definidos, e os electrões
giram em torno do núcleo em órbitas com energias diferentes.As órbitas interiores apresentam energia mais baixa e à medida que se encontram
mais afastadas do núcleo o valor da sua energia é maior.Quando um electrão recebe energia suficiente passa a ocupar uma órbita mais
externa (com maior energia) ficando o átomo num estado excitado.Se um electrão passar de uma órbita para uma outra mais interior liberta energia
sob a forma se fotão de frequência proporcional ao nível de energia.Os electrões tendem a ter a menor energia possível - estado fundamental do
átomo.
1922
1913ÓRBITAS 3º
MODELO
1911ELÉTRON 2º MODELO
18971876V IIIELEMENTOS
18751803 18691850
ELETRÓLISE
1º MODELO 1ª TABELA PERIÓDICA
RAIOS CATÓDICOS
1895PRÓTON
RAIOS X
1905
RELATI-VIDADE
Niels H. David Bohr
RELATI-VIDAD

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 3
Os electrões movem-se ao redor do núcleo em sete órbitas bem definidas - camadas electrónicas, denominadas órbitas estacionárias K, L, M, N, O, P e Q. Em cada camada os electrões possuem uma quantidade fixa de energia; por esse motivo, as camadas são ditas estados estacionários ou níveis de energia que comportam um número máximo de electrões (7).
Movendo-se numa órbita estacionária, o electrão não emite, nem absorve energia. Ao saltar de uma órbita estacionária para outra, o electrão emite ou absorve uma quantidade bem
definida de energia, chamada "quantum de energia". Recebendo um quantum - energia (térmica, eléctrica ou luminosa) do exterior, o electrão salta de
uma órbita mais interna para outra mais externa. Ao contrário, ao "voltar" de uma órbita mais externa para outra mais interna, o electrão emite , na forma de luz de cor bem definida ou outra radiação electromagnética, como ultravioleta ou raios X (daí o nome de fotão que é dado para este quantum de energia).
Em 1913, Bohr (Niels Henrik David Bohr - 1885/1962, dinamarquês, prémio Nobel de Física, em 1922) retomou uma teoria proposta, em 1900, por Planck, segundo a qual "a energia não é emitida em forma contínua, mas em blocos, denominados quantum".
Átomo – Modelo de Bohr (1913)
Teoria atómica
Ao retomar esta teoria, Bohr propôs que o electrão ao girar em torno do núcleo, não estaria obedecendo à Mecânica Clássica, mas sim à Mecânica Quântica. Essas ideias são conhecidas por Postulados de Bohr, resumidamente os seguintes:

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 4
Niels Bohr (1885-1962)Estudava espectros de emissão do gás
hidrogénio. O gás hidrogénio aprisionado numa ampola
submetida a alta diferença de potencial emitia luz vermelha. Ao passar por um prisma, essa luz se subdividia em diferentes comprimentos de onda e frequência, caracterizando um
Espectro luminoso descontínuo.
Os electrões estão movimentando-se ao redor do Núcleo em órbitas de energia FIXA, QUANTIZADA E ESTACIONÁRIA (AS CAMADAS).
Modelo de Bohr (1913) Teoria atómica
Ao receber energia, o electrão salta para uma camada mais externa (mais energética), ficando num estado EXCITADO.
Ao retornar para uma camada menos energética, libera parte da energia absorvida na forma de ondas electromagnética (LUZ), que pode ser Visível, ou não.

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 5
Níveis espectrais de um gásTeoria atómica
PrismaRanhura
Tubo de descarga de gás
a analisar
Tela de visão das cores do
espectro do gás.
O gás hidrogénio aprisionado numa ampola submetida a alta diferença de potencial emitia luz vermelha. Ao passar por um prisma, essa luz se subdividia em diferentes comprimentos de onda e frequência, caracterizando um Espectro luminoso descontínuo.

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 6
Níveis espectrais do HidrogénioTeoria atómica
http://kimika2maila.wikispaces.com/file/detail/BorhEspectro.swf

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 7
Átomo – Modelo de BohrTeoria atómicaNíveis de Energia do Hidrogénio
http://www.dlt.ncssm.edu/core/Chapter11-Thermochemistry/Chapter11-Animations/ElectronOrbits.swf

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 8
Átomo – Modelo de BohrTeoria atómica
Maior distânciaDo núcleo
Níveis de Energia
1º Nível (N1)2º Nível (N2)3º Nível (N3)
NúcleoProtão
Neutrão
O electrão pode mover-se em determinadas órbitas sem irradiar. Essas órbitas estáveis são denominadas estados estacionários.
As órbitas estacionárias são aquelas nas quais o momento angular do electrão em torno do núcleo é igual a um múltiplo inteiro de h/2. Isto é: mvr = nh/2.
O electrão irradia quando salta de um estado estacionário para outro mais interno, sendo a energia irradiada dada por E = hf = Ei-Ef,
AbsorçãoEmissão
Modelo Planetário

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 9
Níveis atómicos – Modelo de Bohr Átomo de Germânio
Núcleo
1º Nível
2º Nível
3º Nível
4º Nível
Electrões de Valência
Cada órbita pode conter um número máximo de electrões que se pode determinar pela expressão 2n2, em que n é número de ordem do nível correspondente à órbita a partir do núcleo, sendo 7 o nível máximo.
Energia
Maior distânciaDo núcleo
NúcleoElectrõesn = 3
n = 2n = 1

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 10
Divisão dos Níveis em subníveis 1ª Camada (K) = Não foi subdividida (Só 1 Subnível) 2ª Camada (L) = 2 Subníveis 3ª Camada (M) = 3 Subníveis 4ª Camada (N) = 4 Subníveis 5ª Camada (O) = 5 Subníveis 6ª Camada (P) = 6 Subníveis 7ª Camada (Q) = 7 Subníveis
Existem 4 Tipos de sub\níveis úteis :s = 2 Electrões p = 6 Electrões d = 10 Electrões f = 14 Electrões
1 Subnível vazio
3 Subníveis vazios
5 Subníveis vazios
Átomo – Modelo de Bohr (1913) Teoria atómica
Núcleo
KLMNOP
Q
12 3
45
67

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 11
MODELOS ATÓMICOS MODELO ATÓMICO DE BOHRA ELETROSFERA
A energia do electrão, numa camada é sempre a mesma.
Só é permitido ao electrão movimentar-se na Camada.
Quanto mais afastada do núcleo, maior a Energia da camada.
Cada camada de energia possui uma quantidade máxima de electrões.
A energia emitida pelo electrão corresponde à diferença entre a energia das camadas de origem e destino.
Quanto maior a energia transportada, maior será a frequência da onda electromagnética.
Retornos electrónicos para a camada K, libertação de luz no ULTRAVIOLETA.
Retornos electrónicos para a camada L, libertação de luz no VISÍVEL.
Retornos electrónicos para a camada M, libertação de luz no INFRAVERMELHO.
K L M N O P Q 2 8 18 32 32 18 8
Professor Fabiano Ramos Costa

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 12
Os postulados de Bohr
Um electrão num átomo move-se numa órbita circular em torno do núcleo, sob influência da atracção coulombiana entre o electrão e o núcleo, obedecendo às leis da mecânica clássica.
Um electrão só se pode mover numa órbita na qual seu momento angular orbital ℓ é um múltiplo inteiro da constante de Planck dividida por 2.
Apesar de estar constantemente acelerado, um electrão que se move numa dessas órbitas possíveis não emite radiação electromagnética.
É emitida radiação electromagnética se um electrão, que se move inicialmente sobre uma órbita de energia Ei, muda seu movimento descontinuamente de forma a se mover numa órbita de energia total Eft A frequência da irradiação emitida v é igual à quantidade (Ei-Ef) dividida pela constante de Planck.
Teoria atómica
(onde h é a constante de Planck (6.63 x 10-34 J.s = 4.14 x 10-15 ev.s), v é a frequência da radiação emitida, Ei e Ef são energias dos estados inicial e final, . o comprimento de onda e c a velocidade da luz (299 792 458 m/s) .
E = hv = Ei-Ef

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 13
Átomo - Modelo Bohr (1913)
Modelo de Rutherford
Planck’s E= hf
Momentum L = nh/2
)11
2122(1
nnR
f
Balmer’s formula
Qual o raio das órbitas em que o electrões não irradiam?Qual é a energia do electrão nestas órbitas?
MODELOS ATÓMICOS MODELO ATÓMICO DE BOHR
http://www.goalfinder.com/product.asp?productid=75

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 14
222 // rkermv
2
2
4
2
rervmF
o
Zee
mmv
eZemin
oedd 151052/)2)((
41
2
Electrão
Núcleo (Protão)
K- Constante de Coulomb
2ª lei de Newton
Átomo - Modelo Bohr (1913)
Níveis
MODELOS ATÓMICOS MODELO ATÓMICO DE BOHR
http://www.goalfinder.com/product.asp?productid=75

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 15
E
Teoria de Bohr (1913)
1. Os electrões têm órbitas bem definidas.2. Os electrões não irradiam.3. Órbitas Circulares: somente órbitas
específicas com um l=(n) (quanta).4. Transmissão de energia: quando os
electrões mudam de uma para outra órbita.
Znhnl 2
20
2
4 nrZe nr
mv2
Balanceamento das forças no átomo
Colombiana Centrifuga
(Z - carga nuclear l - momento angular)
núcleo núcleol l

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 16
Considere um átomo constituído de um núcleo de carga +Ze e massa M, e um electrão de carga –e e massa m.
A condição de estabilidade do electrão é:
O electrão gira numa órbita circular.O núcleo está fixo no espaço.M>>m.
Teoria de Bohr (1913)
Balanceamento das forças no átomo
20
2
4 nrZe nr
mv2

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 17
isolando r:
E isolando v e substituindo r:
,...3,2,1n
,...3,2,1n
Para o átomo de hidrogênio temos:
Teoria de Bohr (1913) Balanceamento das forças no átomo
r = 5,3x10-11m v = 2,2x106m/s

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 18
Teoria de Bohr (1913) Momento Angular:
nmrnhv2
2
nhmvrn
Zan
mZehnrn
rmhmn
rZe
nn
02
20
22
322
22
20
2
44
Á)ngstromme
ha (529,020
2
0
Para v vem: 20
2
4 nrZe nr
mv2
Como:
Podemos substituir v e resolver em ordem a rn:
Onde a0 é o raio de Bohr:
(Å – ångström (Å)=1 Å = 10-10 m.)
O momento angular orbital do electrão é:

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 19
Teoria de Bohr (1913) Raio dos orbitais do Hidrogénio:
)1(2 Zanr on
Arn 529.0)529.0(1,1 2
Arn 116.2)529.0(2,2 2
Arn 761.4)529.0(3,3 2
(Å – ångström (Å)=1 Å = 10-10 m.)

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 20
Teoria de Bohr (1913) Energia dos orbitais do átomo de Hidrogénio:E = Energia Cinética + Energia potencial
nrZemv
0
22
421
(Z - carga nuclear)
0
22
42 Z
re
re
nn
nn rmv
rZe 2
20
2
4
0
2
42 Z
re
n2
022
42
8 hnmeZ
Como:
Como: 20
22
mZehnrn
2nconstanteZ Constante = -13,6eV
Z=1 para o Hidrogénio

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 21
eVn
En 2
6.13
Teoria de Bohr (1913) Energia dos orbitais do átomo de Hidrogénio:
)1(2 Zanr on
eVn
E 6,136.132
eVn
E 4,36.132
eVn
E 5,16.132
(Å – ångström (Å)=1 Å = 10-10 m.)
Arn 529.0)529.0(1,1 2
Arn 116.2)529.0(2,2 2
Arn 761.4)529.0(3,3 2

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 22
Hidrogénio
Teoria de Bohr (1913)
Energia dos orbitais com raios e cargas nucleares diferentes
eVE 4.541
)2(6.132
2
Aar o 265.02
12
Hélio+ eVE 122
1)3(6.13
2
2
Aar o 176.03
12
Lítio2+eVE 6.13
1)1(6.13
2
2
Aar o 529.01
12
eVn
ZE 6.136.132
2
Zanr o
2

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 23
Então V a qualquer distância finita r pode ser obtida integrando-se o trabalho que seria realizado pela força coulombiana que actua de r a .
r r
Zedrr
ZeV0
2
20
2
44 A energia cinética do electrão pode ser calculada por:
20
22
421
rZemvK
A energia total do elétron , E, é então:
Teoria de Bohr (1913) Energia total do electrão:
Primeiro, definimos a energia potencial (V) como sendo zero quando o electrão está infinitamente longe do núcleo.
,...3,2,1n

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 24
Não conseguia explicar a ligação dos átomos para formar moléculas.
Falhas do Modelo de Bohr
Funcionava somente para átomos com um electrão (hidrogenóides).
Não conseguia calcular a estrutura fina das linhas espectrais - quando os átomos eram colocados em campos magnéticos.
O modelo de Bohr foi um grande passo na nova teoria quântica, mas tinha as suas falhas:

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 25
Átomo – Modelo de BohrTeoria atómica
Modelo de Neil Bohr.wmv http://www.youtube.com/watch?v=31RbAE0QkgA

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 26
Arthur Holly Compton (1892-1962)
Efeito de Compton 1927
19231913ÓRBITAS 3º
MODELO
1911ELÉTRON 2º MODELO
18971876V IIIELEMENTOS
18751803 18691850
ELETRÓLISE
1º MODELO 1ª TABELA PERIÓDICA
RAIOS CATÓDICOS
1895PRÓTON
RAIOS XNÍVEIS DE ENERGIA
1905
RELATI-VIDADE
O Efeito Compton foi observado por Arthur Holly Compton em 1923, pelo qual fez ele receber o Prémio Nobel de Física em 1927.
Este efeito é importante porque ele demonstra que a luz não pode ser explicada meramente como um fenómeno ondulatório. No espalhamento de Thomson, a clássica teoria de partículas carregadas por uma onda electromagnética, não pode explicar alguma variação no comprimento de onda…

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 27
Este efeito é importante porque ele demonstra que a luz não pode ser explicada meramente como um fenómeno ondulatório. O espalhamento de Thomson, a clássica teoria de partículas carregadas espalhadas por uma onda electromagnética, não pode explicar alguma variação no comprimento de onda.
Teoria atómica Efeito de Compton
Arthur Holly Compton (1892 -1962)
Em Física, Efeito Compton ou o Espalhamento (Scattering) de Compton, é a diminuição de energia (aumento de comprimento de onda) de um fotão de raio-X ou de raio gama, quando ele interage com a matéria.
A luz deve agir como se ela consistisse de partículas como condição para explicar o espalhamento de Compton. O experimento de Compton convenceu físicos que a luz pode agir como uma corrente de partículas cuja energia é proporcional à frequência.
O Efeito Compton foi observado por Arthur Holly Compton em 1923, pelo qual fez ele receber o Prémio Nobel de Física em 1927.

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 28
Quando um fotão penetra na matéria, ele pode interagir com um electrão e ser desviado. Vamos imaginar fotões de raios X incidindo num alvo e sendo desviados pelos electrões desse alvo. Compton observou que a radiação desviada (fotões) tinha comprimento de onda maior (`) do que a radiação incidente () e que esta variação no comprimento de onda dependia apenas do ângulo de desvio (). Este efeito ficou conhecido como Efeito Compton ou Espalhamento Compton.
O espalhamento de Compton ocorre em todos os materiais e predominantemente com fotões de média energia (entre 0.5 e 3.5 MeV). Ele é também observado com fotões de alta energia; fotões de luz visível ou de frequências mais altas, por exemplo, possuem energia suficiente para expelir os electrões saltados do átomo (efeito Fotoeléctrico).
Teoria atómica Efeito de Compton

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 29
cos1cm
h
o
Electrão alvo em repouso
Fotão raio X incidente
Conservação de momento:
Fotão antes: p = h/Fotão depois: p´ = h/´Electrão antes: P = 0Electrão depois: P = mv
Conservação de energia:
Teoria atómica Efeito de Compton
f
fff
hc
hvc
EP
c)(mecE
P222
e
i
iii
hc
hvcEP

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 30
Efeito Compton
Fotão Electromagnético
Electrão Ejectado
+

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 31
Os fotões têm energia e momento linear:Quando um fotão penetra na matéria, ele pode interagir com um electrão e
ser espalhado. Aplicando a lei da conservação da energia e do momento linear, obtemos:
/ /E hc p h
Deslocamento de Compton:A explicação do Efeito Fotoeléctrico e do Efeito Compton fornece uma forte evidência da natureza quântica da luz
Teoria atómica Efeito de Compton

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 32
(1892-1987)
Teoria da “PARTÍCULA/ONDA”1929
19231913ÓRBITAS 3º
MODELO
1911ELECTRÃO 2º MODELO
18971876V IIIELEMENTOS
18751803 18691850
ELETRÓLISE
1º MODELO 1ª TABELA PERIÓDICA
RAIOS CATÓDICOS
1895PROTÃO
RAIOS XNÍVEIS DE ENERGIA
1905
RELATI-VIDADE
Efeito Compton
1924
Aplicando esta suposição ao modelo de Bohr ele supôs que o electrão teria uma onda associada ao longo de sua órbita em torno do protão. Mas apenas algumas órbitas seriam possíveis para que a onda não interferisse destrutivamente consigo mesma. Essas órbitas especiais eram exactamente as propostas por Bohr.
Importante para a explicação dos sucessos da teoria de Bohr, e que abriria as portas para a uma teoria consistente, foi dado pelo físico francês Louis De Broglie.
Na sua tese de doutoramento, em 1924, De Broglie fez uma proposição de simetria baseada em uma teoria de Einstein de 1905 de que a luz pode, em algumas condições, se comportar como partícula. Não poderiam as partículas apresentar um comportamento de ondas?
Louis de Broglie

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 33
Teoria atómica Espectro de Frequências

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 34
Spectrum de Luz Visível
Raios Gamma
Luz Visível
Ondas RádioInfravermelhosRaios X
Comprimento de Onda (λ)
Nível de energia
Espectros atómicosTeoria atómica

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 35
Durante muito tempo, os Cientistas argumentaram acerca da natureza exacta da luz!...
Isaac Newton (1642-1727) Propôs que a luz era feita de pequenas partículas…
Christian Huygens (1629-1695) Sugeriu que a luz era feita de ondas!...
Como Newton era mais famoso que Huygens, muitos cientistas acreditaram nele… Até ao SEC XIX.
No início do século XIX, Thomas Young mostrou que a luz podia interferir nela própria!..
Os resultados da experiência da ranhura dupla ( Double slit experiment) podem ser explicados se a luz é feita de ondas!...
Em 1818, Augustin Fresnel mostrou que a difracção da luz pode ser facilmente explicada se a luz for feita de ondas!...
As suas previsões foram verificadas por fontes independentes e não poderiam ser explicadas se a luz fosse feita de partículas!...
Teoria atómica O que é a Luz ?

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 36
Em 1864, James Maxwell mostrou que a luz é uma onda (como as ondas electromagnéticas rádio)
Em 1888, Heinrich Hertz confirmou as previsões de Maxwell pelas transmissão de ondas electromagnéticas pelo ar, mas também observou um fenómeno inesperado:
O mesmo fenómeno foi também observado no Tubo de Raios Catódicos (CRT) alguns anos mais tarde, e foi chamado de efeito fotoeléctrico, mas permanecia inexplicável!...
Em 1902 Phillipp von Lenard estudou o efeito fotoeléctrico e notou que a energia dos electrões produzidos nas faíscas, dependia da cor da luz, mas não da sua intensidade. Já o número de electrões dependia da intensidade da luz mas não da sua cor!...
O Efeito Fotoeléctrico foi explicado por Albert Einsteine em 1905…
Teoria atómica que é a Luz?
No final do século XIX, os físicos estavam convencidos de que a luz era feita de ondas!...
Faíscas de transmissão eram mais facilmente criadas se o aparato estivesse iluminado por luz ultravioleta!

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 37
Teoria quântica de Max Planck (1900)
A teoria quântica refere-se a energia:
Quando a energia está em forma de radiação electromagnética (quer dizer, de uma radiação similar á luz), se denomina de energia radiante e a sua unidade mínima recebe o nome de “fotão”. A energia de um fotão é dada pela equação de Planck:
E = h×f
h: constante de Planck = 6,62×10-34 Joule/segundo f: frequência da radiação.
Qualquer quantidade de energia que se emita ou se absorva, deverá ser um número inteiro de “quantums”.
Teoria atómica que é a Luz?
Propôs que a luz só pode assumir alguns valores específicos de energia.
Ele utilizou a estatística de Boltzmann para obter uma equação teórica que concordava com os resultados experimentais para todos os comprimentos de onda:
112
5
2
kThce
hcI
Lei da Radiação de Planck:

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 38
20
2 cmKEmcE
420
22 cmcpE
Teoria atómica: De Broglie Teoria da “PARTÍCULA/ONDA” (1924)
DeBroglie Hypothesis
Aplicando a suposição de que as partículas podiam ter comportamentos de onda, ao Modelo de Bohr ele supôs que o electrão teria uma onda associada ao longo de sua órbita em torno do protão. Mas apenas algumas órbitas seriam possíveis para que a onda não interferisse destrutivamente consigo mesma. Essas órbitas especiais eram exactamente as propostas por Bohr!
Este resultado abriu caminho para uma nova interpretação do electrão e da matéria em geral. As partículas teriam um novo comportamento chamado de partícula-onda. Se o electrão colidir com um detector, um ponto bem definido será registado, como espera-se de uma partícula.
Sugeriu em 1924, que a expressão do comprimento de onda de uma partícula, era, por analogia, para o momento de um fotão. Começou com a fórmula de Einsteine…
Outra maneira de expressar isto é :

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 39
Teoria atómica De Broglie Teoria da “PARTÍCULA/ONDA” (1924)
cEp
hchvE
h
chcp
ph
Pelo que para um a partícula de 0 (zero) Massa em repouso (mo) :
Para um fotão será: Portanto:
De BroglieWavelength
m0 rest mass Mass em repouso: Uma das consequências da teoria da Relatividade de Einstein (1905), é que a massa de um objecto aumenta com a velocidade em relação ao observador. Quando um objecto está em repouso, relativamente ao observador) ele tem a massa usual (inercial= tendência para resistir a uma força aplicada) com a qual nós estamos familiarizados. Esta é a chamada massa em repouso de um objecto.
E:Energia total.p: Momentum.h: Constante de Planck.: Comprimento de onda.c: Velocidade da luz.m0: Massa em repouso.m: massa relativista.K: Energia cinética.v: Velocidade da partícula.

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 40
Teoria atómica De Broglie Teoria da “PARTÍCULA/ONDA” (1924)
– Louis era historiador e irmão do Físico Maurice de Broglie e mudou de área influenciado pelas ideias do irmão que apoiava as novas teorias de Einstein, Planck e Compton, e ficou interessado pelas modificações científicas e filosóficas que elas produziam.
hvE hp
As ideias de de Broglie não tinham evidências experimentais na época e Einstein foi quem chamou a atenção para elas.
5 anos mais tarde, a quantidade de resultados de experiências motivadas pela ideias de de Broglie que confirmavam suas hipóteses era tão grande e tão fortes, que ele ganhou o Prémio Nobel de Física.
Louis de Broglie, na sua tese de Doutorado apresentada em 1924 na Fac. de Ciências da Univ. de Paris, propôs a existência das ondas de matéria.
Ele estendeu a dualidade onda-partícula da radiação para o caso da matéria e propôs que os aspectos ondulatórios da matéria se relacionam com as propriedades corpusculares exactamente da mesma forma que a radiação.
Ou seja, para a matéria também vale: e
- comprimento de onda de de Broglie da matéria.

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 41
Einstein, Planck Luz
hE pcE
hp
Louis de BroglieDualidade onda/partícula vm
h
Característica fundamental de todas as partículas
kg10~s,J10~ 3134 emh
mas
então
Teoria atómica De Broglie Teoria da “PARTÍCULA/ONDA” (1924)

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 42
Hipótese ondulatória de De Broglie
Tese de doutorado
Broglie) (De
(Bohr)
hm
nhrm
v
2v
rn 2
Teoria atómica De Broglie Teoria da “PARTÍCULA/ONDA” (1924)
“trajectórias” estacionárias postuladas por Bohr.

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 43
exp=1,65 Å
dB=1,66 Å
Teoria atómica De Broglie Teoria da “PARTÍCULA/ONDA” (1924)
Comprovação experimental das ondas de De Broglie

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 44
Teoria atómica Teoria da “PARTÍCULA/ONDA”
Experiência Davisson – Germer (1927) Davisson e Germer obteve a confirmação experimental da natureza ondulatória da
partícula, ao medir o comprimento de onda do electrão (descoberta feita acidentalmente).
Esta experiência confirmou a natureza ondulatória do electrão, confirmando a anterior hipóteses de De Broglie. Confirmar a dualidade onda-particula numa base experimental representou um passo muito importante no desenvolvimento da Mecânica Quântica. d
θ

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 45
Teoria atómica Teoria da “PARTÍCULA/ONDA” Experiência Davisson – Germer (1927)
Davisson e Germer observaram experimentalmente que electrões eram difractados (muito parecido com os raios X) ,em cristais de níquel.
George P. Thomson (1892–1975), filho de J. J. Thomson, fez experimentos de transmissão onde observou difracção de electrões em diversos materiais, como celulose, ouro, alumínio, e platina. Uma amostra policristalina de SnO2, aleatoriamente orientada, produziu anéis de interferência.

Como sabe que este vaso é azul?Luz é energia. Ela propaga-se em ondas, cada uma com a sua frequência e comprimento de onda…
Comprimento de onda: () Distância entre pontos correspondentes nas ondas sucessivas. Frequência: (f) Número de ondas
que passam por um ponto no espaço de tempo de um segundo.
Os Átomos podem absorver energia: Mas apenas se a onda transporta a frequência certa para excitar o átomo. A Maior parte das ondas passam através do cobalto , o pigmento do vaso….
Os átomos ficam excitados e um dos seus electrões, salta para um nível de energia mais alto
Energia com um comprimento de onda de cerca de 475 nm (cerca de 4.75 mil milhões de ondas por centímetro) é absorvida.
O electrão depois regressa ao seu nível de energia inicial …
… O quer causa a emissão de um fotão com a mesma frequência…
… O fotão é captado pelo olho humano que interpreta a vibração como cor azul…
… O nosso cérebro processa milhares de milhões de informações por segundo, outros materiais no vaso enviam informações sobre textura, reflectividade, espessura, etc.,
Modelos Atómicos: Modelo de Bohr

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 47
No início do século XIX, Thomas Young mostrou que a luz podia interferir nela própria!..
Os resultados da experiência da ranhura dupla ( Double slit experiment) podem ser explicados se a luz é feita de ondas!...
Teoria atómica O que é a Luz?“Experiência Fenda Dupla” ou “Young's experiment”
A experiência da fenda dupla consiste em deixar que a luz visível se difracte através de duas fendas, produzindo bandas num ecrã. As bandas formadas, ou padrões de interferência, mostram regiões claras e escuras que correspondem aos locais onde as ondas luminosas interferiram entre si construtivamente e destrutivamente.
A experiência da fenda dupla prova inequivocamente a chamada mecânica quântica, ou ondulatória, que deve basear-se em noções essencialmente diferentes da mecânica clássica. Pois na quântica não existe o conceito de trajetória da partícula. Esta circunstância constitui o conteúdo do chamado princípio da incerteza, ou princípio da indeterminação, que é um dos fundamentais da mecânica quântica e foi descoberto em 1927 por Werner Heisenberg.

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 48
Teoria atómica O que é a Luz?
A mecânica quântica demonstra as naturezas inseparáveis de onda e partícula da luz e de outras partículas quânticas. Uma fonte de luz coerente, ilumina uma fina placa com duas ranhuras cortadas em paralelo, e a luz passando através das ranhuras vai projectar-se numa tela a frente. A natureza de onda da luz causa que as ondas de luz ao passarem através das duas ranhuras, interfiram uma na outra, criando um padrão de bandas de luz e sombra na tela. Porém se a luz passar somente através de uma ranhura, na tela nota-se uma absorção (desvanecimento) da luz como se ela fosse feita de partículas!...
“Experiência Fenda Dupla” ou “Young's experiment”

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 49
Teoria atómica O que é a Luz?“Experiência da Fenda Dupla” ou “Young's experiment”
dr-quantum_Luz 2Fendas.wmvhttp://www.youtube.com/watch?v=lytd7B0WRM8

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 50
Dúvidas?
Obrigado!

Modelos Atómicos: Modelo de Bohr
03-05-2023 Por : Luís Timóteo 51
BibliografiaUCS - Universidade de Caxias do Sul – Núcleo de Apoio ao Ensino da Químicahttp://hermes.ucs.br/ccet/defq/naeq/http://www.fisica.ufs.br/CorpoDocente/mvalerio/index_arquivos/Cursos/2007-1/IntroMecQuanthttp://pt.wikipedia.org/wiki/Experiência_da_dupla_fendahttp://pt.wikipedia.org/wiki/Efeito_Comptonwww.youtube.comUNICAMP – Laboratório de Química do Estado Sólidohttp://lqes.iqm.unicamp.br/canal_cientifico/www.physics.gatech.edu/froghttp://www.maloka.org/f2000/applets/a2.html
UFSC – Universidade Federal de Santa Catarinahttp://quark.qmc.ufsc.br/qmcweb/artigos/nuclear/
NOBEL – e-Museumhttp://www.nobel.se/physics/laureates/index.html
UFC – Universidade Federal do Ceará – Depto. de Físicahttp://www.fisica.ufc.br/index.htmlTribuna virtual.comUFC – Universidade Estadual de CampinasRepresentações Imagéticas dos Modelos Teóricos para a Estrutura da Matériahttp://www.iar.unicamp.br/pgmultimeios/pesquisa/a_meleiro/home.htm
http://www.tribunavirtual.comhttp://hyperphysics.phy-astr.gsu.edu/hbase/mod1.html#c3
http://scienceblogs.com/sciencepunk/2011/09/five_iconic_science_images_and.php
http://physics-pelago.blogspot.com/2011/03/compton-effect.html
http://www.nicepedia.com/science-technology/quantum-theory-part-ii/
http://micro.magnet.fsu.edu/primer/java/interference/doubleslit/
http://hyperphysics.phy-astr.gsu.edu/hbase/davger.html