FOTOSSÍNTESE E METABOLISMO DE … Aos colegas da Fisiologia: José R. Magalhães Filho, Paulo E. R....
Transcript of FOTOSSÍNTESE E METABOLISMO DE … Aos colegas da Fisiologia: José R. Magalhães Filho, Paulo E. R....

INSTITUTO AGRONÔMICO
CURSO DE PÓS-GRADUAÇÃO EM AGRICULTURA TROPICAL E
SUBTROPICAL
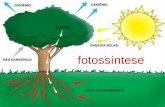
FOTOSSÍNTESE E METABOLISMO DE
CARBOIDRATOS EM PLANTAS JOVENS DE
CANA-DE-AÇÚCAR SOB BAIXA TEMPERATURA E
DEFICIÊNCIA HÍDRICA
DANIELA FAVERO SÃO PEDRO MACHADO
Orientadora: Ana Maria Magalhães Andrade Lagôa
Tese submetida como requisito parcial para
obtenção do grau de Doutor em Agricultura
Tropical e Subtropical, Área de Concentração
em Tecnologia da Produção Agrícola.
Campinas, SP
Fevereiro 2014

Ficha elaborada pela bibliotecária do Núcleo de Informação e Documentação do Instituto Agronômico
M149f Machado, Daniela Favero São Pedro Fotossíntese e metabolismo de carboidratos em plantas jovens de cana-de-açúcar sob baixa temperatura e deficiência hídrica / Daniela Favero São Pedro Machado. Campinas, 2013. 75 fls.
Orientadora: Ana Maria Magalhães Andrade Lagôa Tese (Doutorado) Agricultura Tropical e Subtropical – Instituto Agronômico
1 Plantas jovens de cana-de-açúcar 2. Trocas gasosas 3. Fluorescência da clorofila 3. Síntese de sacarose fosfato I. Lagoa, Ana Maria Magalhães Andrade III. Título
CDD. 633.61


iv
Aos meus pais
Nelva e Abílio (in memorian),
por todo amor.
DEDICO
Ao meu marido Ricardo e à minha filha
Carolina por todo amor, paciência,
auxílio e apoio durante a execução deste
trabalho,
OFEREÇO

v
AGRADECIMENTOS
- A Deus.
- À Pós-Graduação e ao Instituto Agronômico pela oportunidade.
- À Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (CAPES) pela bolsa de
estudos concedida.
- À Fundação de Amparo à Pesquisa do Estado de São Paulo (Fapesp) pelo financiamento do
projeto.
- À Dra. Ana Maria M. A. Lagôa pela oportunidade, orientação e ensinamentos.
- Ao Dr. Eduardo Caruso Machado por todo apoio, paciência e ensinamentos.
- Ao Severino Nogueira por todo auxílio e ideias na montagem dos experimentos.
- À minha sogra Celina, por todo amor, carinho, paciência e dedicação nestes anos cuidando
da Carolina.
- Ao meu marido Ricardo S. Machado por todo auxílio na execução dos experimentos e acima
de tudo paciência e compreensão nos momentos de ausência.
- Aos colegas da Fisiologia: José R. Magalhães Filho, Paulo E. R. Marchiori, Fernanda
Castro, Verònica L. Dovis, Guilherme G. Roberto, Cristina R. G. Sales e Karina I. Silva por
todo auxílio durante os experimentos e análises bioquímicas.
- À Dra. Norma de M. Erismann e Dra. Rose M. A. G. Tomaz pelo auxílio e sugestões nas
análises bioquímicas.
- Aos professores da área de concentração Tecnologia da Produção Agrícola da PG-IAC,
pelos ensinamentos transmitidos.
- Ao Prof. Dr. Joaquim Albenísio G. Silveira e aos alunos da Universidade Federal do Ceará,
Ana Karla M. Lobo, Márcio O. Martins e Adilton de V. Fontenele por todo auxílio nas
determinações das atividades enzimáticas.
- Ao Prof. Dr. Joaquim Albenísio G. Silveira, Prof. Dr. Marcelo de A. Silva e Dra. Norma de
M. Erismann pelas sugestões na pré-banca.
- Enfim, a todos aqueles que de uma forma direta ou indireta contribuíram para a realização
deste trabalho.

vi
"Desistir... eu sempre pensei seriamente nisso, mas nunca me
levei realmente a sério; é que tem mais chão nos meus olhos
do que o cansaço nas minhas pernas, mais esperança nos
meus passos do que tristeza nos meus ombros, mais estrada
no meu coração do que medo na minha cabeça."
(Cora Coralina)

vii
SUMÁRIO
LISTA DE SÍMBOLOS E ABREVIATURAS............................................................... ix
ÍNDICE DE FIGURAS.................................................................................................. xii
ÍNDICE DE TABELAS.................................................................................................. xvi
Resumo............................................................................................................................. xvii
Abstract............................................................................................................................ xix
CAPÍTULO I
1 INTRODUÇÃO............................................................................................................ 2
2 REVISÃO DE LITERATURA.................................................................................... 3
3 REFERÊNCIAS BIBLIOGRÁFICAS........................................................................ 13
CAPÍTULO II - Baixa temperatura noturna e deficiência hídrica na fotossíntese de
cana-de-açúcar
RESUMO......................................................................................................................... 20
ABSTRACT..................................................................................................................... 21
1 INTRODUÇÃO............................................................................................................ 22
2 MATERIAL E MÉTODOS.......................................................................................... 23
2.1 Variáveis medidas e calculadas.................................................................................. 25
Assimilação de CO2 e fluorescência da clorofila a.......................................................... 25
Teor de carboidratos solúveis.......................................................................................... 27
Teor de amido.................................................................................................................. 28
Potencial da água na folha............................................................................................... 28
Delineamento experimental............................................................................................. 28
3 RESULTADOS E DISCUSSÃO................................................................................ 29
4 CONCLUSÕES........................................................................................................... 38
5 REFERÊNCIAS BIBLIOGRÁFICAS....................................................................... 39
CAPÍTULO III - Metabolismo de carboidratos em duas cultivares de cana-de-açúcar
sob baixa temperatura e deficiência hídrica
RESUMO........................................................................................................................ 44
ABSTRACT.................................................................................................................... 45
1 INTRODUÇÃO........................................................................................................... 46
2 MATERIAL E MÉTODOS......................................................................................... 48
2.1 Variáveis medidas e calculadas................................................................................. 49
Assimilação de CO2 e fluorescência da clorofila a......................................................... 49
Potencial da água na folha............................................................................................... 50
Teor de carboidratos........................................................................................................ 50
Atividade de enzimas do metabolismo de carboidratos.................................................. 51
Proteína solúvel total....................................................................................................... 51
Atividade da sintase de sacarose fosfato........................................................................ 51
Atividade da sintase de sacarose.................................................................................... 52
Atividade das invertases ácidas...................................................................................... 52
Atividade das invertases neutras.................................................................................... 53
Delineamento experimental............................................................................................. 53
3 RESULTADOS............................................................................................................ 53
4 DISCUSSÃO................................................................................................................ 63
Período de baixa temperatura e deficiência hídrica......................................................... 63

viii
Período de recuperação.................................................................................................... 69
5 CONCLUSÕES........................................................................................................... 70
REFERÊNCIAS BIBLIOGRÁFICAS.......................................................................... 72

ix
LISTA DE SÍMBOLOS E ABREVIATURAS
A Assimilação de CO2, μmol m-2
s-1
Ai Assimilação diária de CO2, mmol m-2
d-1
AMI Amido
Apot Assimilação máxima de CO2 em concentração saturante de CO2, μmol m-2
s-1
AS Açúcares solúveis
ATP Adenosina trifosfato
A/Ci Eficiência aparente de carboxilação, μmol m-2
s-1
Pa-1
BFV Bainha do feixe vascular
BSA Albumina sérica bovina
cc-ec Células companheiras - elementos crivados
Ci Concentração intercelular de CO2, μmol mol-1
DAP Dias após plantio
DH Deficiência hídrica
E Transpiração, mmol m-2
s-1
EDTA Ácido etilenodiamino tetra-acético
ETR Transporte aparente de elétrons, μmol m-2
s-1
EUAi Eficiência intrínseca do uso da água, μmol mol-1
Fo Fluorescência mínima em tecidos adaptados ao escuro
Fo' Fluorescência mínima em tecidos iluminados
Fm Fluorescência máxima em tecidos adaptados ao escuro
Fm' Fluorescência máxima em tecidos iluminados
Fq' Extinção fotoquímica da fluorescência pelos centros oxidados do
fotossistema II
Fq'/Fm' Eficiência operacional do fotossistema II
Fq'/Fv' Fator de eficiência do fotossistema II
FRU Frutose
Fru-6-P Frutose-6-fosfato
FSII Fotossistema II
Fv Fluorescência variável em tecidos adaptados ao escuro
Fv' Fluorescência variável em tecidos iluminados
Fv/Fm Eficiência quântica máxima do fotossistema II em tecidos adaptados ao

x
escuro
Fv'/Fm' Eficiência quântica máxima do fotossistema II em tecidos iluminados
GLU Glicose
Glu-6-P Glicose-6-fosfato
gs Condutância estomática, mol m-2
s-1
H2SO4 Ácido sulfúrico
IVA Invertase ácida solúvel (EC 3.2.1.25)
IVN Invertase neutra (EC 3.2.1.26)
KOH Hidróxido de potássio
LM Limitação metabólica, %
MF Massa fresca
MgCl2 Cloreto de magnésio
MOPS Ácido 3-(N-morfolino)-propanossulfônico
MS Massa seca
NADPH Nicotinamida adenina dinucleotídeo de piridina fosfato reduzida
NPQ Coeficiente de extinção não-fotoquímico da fluorescência
OAA Ácido oxaloacético
PEP Fosfoenolpiruvato
PEPcase Fosfoenolpiruvato carboxilase
Pi Fosfato inorgânico
PPDK Piruvato ortofosfato diquinase
PVPP Polivinilpolipirrolidona
Q Radiação fotossinteticamente ativa
QA Quinona A
Rubisco Ribulose-1,5-bisfosfato carboxilase/ oxigenase
RuBP Ribulose-1,5-bisfosfato
SAC Sacarose
SPP Fosfatase de sacarose fosfato (EC 3.1.3.24)
SPS Sintase de sacarose fosfato (EC 2.4.1.14)
SuSy Sintase de sacarose (EC 2.4.1.13)
TN Temperatura noturna
UDP-glicose Uridina-5'-difosfoglicose
Vmax Eficiência máxima de carboxilação, μmol m-2
s-1

xi
Vpmax Eficiência aparente de carboxilação da fosfoenolpiruvato carboxilase, mol m-
2 s
-1
Ψw6h Potencial da água na folha medido antes do amanhecer, MPa
Ψw14h Potencial da água na folha medido às 14:00 h, MPa
CO2 Eficiência quântica da fotossíntese, μmol CO2 (μmol fótons)-1

xii
ÍNDICE DE FIGURAS
CAPÍTULO I
Figura 1- Produção, transporte e acúmulo de sacarose em cana-de-açúcar.
Adaptado de GROF e CAMPBELL (2001)................................................
4
CAPÍTULO II
Figura 1- Fotografias ilustrando (A) bandeja para germinação contendo substrato
comercial e mini-toletes de cana-de-açúcar, (B) detalhe do mini-tolete
contendo gema, e (C) visão geral das plantas em casa de vegetação aos
56 dias após o plantio..................................................................................
24
Figura 2- Variação da radiação solar (A) e da temperatura (B) durante o período
experimental. Setas indicam os dias de medidas de trocas gasosas e
fluorescência da clorofila a em cana-de-açúcar..........................................
29
Figura 3- Variação da assimilação diária de CO2 (Ai) de cana-de-açúcar, cv.
IACSP94-2094 aos seguintes tratamentos: TN20, temperatura noturna de
20 °C - irrigada; DH/TN20, temperatura noturna de 20 °C - não irrigada;
TN12, temperatura noturna de 12 °C - irrigada e DH/TN12, temperatura
noturna de 12 °C - não irrigada. As colunas indicam média de três
repetições (± erro padrão)...........................................................................
30
Figura 4- A, Resposta da assimilação de CO2 (A) e B, condutância estomática (gs)
em cana-de-açúcar cv. IACSP94-2094. Tratamentos: TN20, temperatura
noturna de 20 °C - irrigada (■); DH/TN20, temperatura noturna de 20 °C
- não irrigada (○); TN12, temperatura noturna de 12 °C - irrigada (∆) e
DH/TN12, temperatura noturna de 12 °C - não irrigada (▼). Dados
retirados da curva A vs. Ci, sob saturação de luz e 400 μmol mol-1
de
CO2. Período de aplicação dos tratamentos, dias 1 a 5; período de
recuperação com retorno da irrigação das plantas e temperatura noturna
de 20 °C, dias 5 a 9.....................................................................................
31
Figura 5- A, Variação de potencial da água na folha (W14) e B, transpiração (E)
em cana-de-açúcar cv. IACSP94-2094 submetida aos tratamentos: TN20,
temperatura noturna de 20 °C - irrigada; DH/TN20, temperatura noturna
de 20 °C - não irrigada; TN12, temperatura noturna de 12 °C - irrigada e
DH/TN12, temperatura noturna de 12 °C - não irrigada. As colunas
indicam média de três repetições (± erro padrão). Período de aplicação
dos tratamentos, dias 1 a 5; período de recuperação com retorno da
irrigação das plantas e temperatura noturna de 20 °C, dias 5 a 9...............
32
Figura 6- A,Variação de assimilação máxima em CO2 saturante (Apot); B,
limitação metabólica (LM); C, eficiência de carboxilação da PEPcase
(Vpmax) e D, eficiência máxima da Rubisco (Vmax) em cana-de-açúcar cv.
IACSP94-2094 submetida aos tratamentos: TN20, temperatura noturna
de 20 °C - irrigada (■); DH/TN20, temperatura noturna de 20 °C - não

xiii
irrigada (○);TN12, temperatura noturna de 12 °C - irrigada (∆) e
DH/TN12, temperatura noturna de 12 °C - não irrigada (▼). Os símbolos
indicam média de três repetições (± erro padrão). Período de aplicação
dos tratamentos, dias 1 a 5; período de recuperação com retorno da
irrigação das plantas e temperatura noturna de 20 °C, dias 5 a 9...............
33
Figura 7- A, Resposta de eficiência quântica máxima do fotossistema II (Fv/Fm);
B, eficiência operacional do FSII (Fq'/Fm'); C, transporte aparente de
elétrons (ETR) e D, fator de eficiência do FSII (Fq'/Fv') em cana-de-
açúcar cv. IACSP94-2094 submetida aos tratamentos: TN20, temperatura
noturna de 20 °C - irrigada (■); DH/TN20, temperatura noturna de 20 °C
- não irrigada (○);TN12, temperatura noturna de 12 °C - irrigada (∆) e
DH/TN12, temperatura noturna de 12 °C - não irrigada (▼). Os símbolos
indicam média de três repetições (± erro padrão). Período de aplicação
dos tratamentos, dias 1 a 5; período de recuperação com retorno da
irrigação das plantas e temperatura noturna de 20 °C, dias 5 a
9...................................................................................................................
35
Figura 8- Relação entre eficiência quântica de CO2 (CO2) e eficiência
operacional do fotossistema II (Fq’/Fm’) em cana-de-açúcar cv.
IACSP94-2094 submetida aos tratamentos: TN20 (), temperatura
noturna de 20 °C - irrigada; DH/TN20 (), temperatura noturna de 20
°C - não irrigada; TN12 (), temperatura noturna de 12 °C - irrigada e
DH/TN12 (), temperatura noturna de 12 °C - não irrigada, um
(símbolos cheios e linha, CO2=-0,003+0,132*Fq´/Fm´, R2=0,93,
p<0,01) e quatro dias após os tratamentos (símbolos vazios e linha
tracejada, CO2=-0,005+0,136*Fq´/Fm´, R2=0,87, p<0,01).......................
36
CAPÍTULO III
Figura 1- (A, B) Resposta da assimilação de CO2 (A) e (C, D) assimilação diária
de CO2 (Ai) de cana-de-açúcar, cultivares IACSP94-2094 e IACSP95-
5000, sendo o dia 0 (testemunha) medida feita após 18 dias de
aclimatação a 32/20 °C (dia/ noite) com plantas irrigadas; dia 2 medida
feita após 34 horas a 22/12 °C (dia/ noite) com plantas irrigadas (I) e não
irrigadas (NI); dia 13 medida feita após 13 dias de baixa temperatura em
plantas irrigadas e não irrigadas (estresse intermediário); dia 20 medida
após 20 dias de baixa temperatura em plantas irrigadas e não irrigadas
(estresse máximo); dia 22 medida após 2 dias de retorno à temperatura
de 32/20 °C e reidratação e dia 28 medida após 8 dias de recuperação
das plantas. Símbolos indicam média de 20 repetições ± erro padrão para
A e 4 repetições ± erro padrão para Ai........................................................
55
Figura 2- (A, B) Resposta da condutância estomática (gs), (C, D) transpiração (E)
e (E, F) eficiência intrínseca do uso da água (EUAi) de cana-de-açúcar,
cultivares IACSP94-2094 e IACSP95-5000, sendo o dia 0 (testemunha)
medida feita após 18 dias de aclimatação a 32/20 °C (dia/ noite) com
plantas irrigadas; dia 2 medida feita após 34 horas a 22/12 °C (dia/
noite) com plantas irrigadas (I) e não irrigadas (NI); dia 13 medida feita
após 13 dias (estresse intermediário); de baixa temperatura em plantas

xiv
irrigadas e não irrigadas; dia 20 medida após 20 dias de baixa
temperatura em plantas irrigadas e não irrigadas (estresse máximo); dia
22 medida após 2 dias de retorno à temperatura de 32/20 °C e
reidratação e dia 28 medida após 8 dias de recuperação das plantas.
Símbolos indicam média de 20 repetições ± erro padrão...........................
56
Figura 3- (A, B) Variação da concentração intercelular de CO2 (Ci) e da (C, D)
eficiência aparente de carboxilação (A/Ci) de cana-de-açúcar, cultivares
IACSP94-2094 e IACSP95-5000, sendo: dia 0 (testemunha) medida
feita após 18 dias de aclimatação a 32/20 °C (dia/ noite) com plantas
irrigadas; dia 2 medida feita após 34 horas a 22/12 °C (dia/ noite) com
plantas irrigadas e não irrigadas; dia 13 medida feita após 13 dias
(estresse intermediário) de baixa temperatura em plantas irrigadas (I) e
não irrigadas (NI); dia 20 medida após 20 dias de baixa temperatura em
plantas irrigadas e não irrigadas (estresse máximo); dia 22 medida após
2 dias de retorno à temperatura de 32/20 °C e reidratação e dia 28
medida após 8 dias de recuperação das plantas. Símbolos indicam média
de 20 repetições ± erro padrão....................................................................
57
Figura 4- (A, B) Resposta da eficiência operacional do FSII (Fq'/Fm') de cana-de-
açúcar, cultivares IACSP94-2094 e IACSP95-5000, sendo o dia 0
(testemunha) medida feita após 18 dias de aclimatação a 32/20 °C (dia/
noite) com plantas irrigadas; dia 2 medida feita após 34 horas a 22/12 °C
(dia/ noite) com plantas irrigadas (I) e não irrigadas (NI); dia 13 medida
feita após 13 dias (estresse intermediário); de baixa temperatura em
plantas irrigadas e não irrigadas; dia 20 medida após 20 dias de baixa
temperatura em plantas irrigadas e não irrigadas (estresse máximo); dia
22 medida após 2 dias de retorno à temperatura de 32/20 °C e
reidratação e dia 28 medida após 8 dias de recuperação das plantas.
Símbolos indicam média de 20 repetições ± erro padrão...........................
58
Figura 5- (A, B) Variação do coeficiente de extinção não fotoquímico (NPQ) e da
(C, D) eficiência quântica máxima do FSII (Fv/Fm) e eficiência quântica
máxima do FSII sob Q (Fv'/Fm') de cana-de-açúcar, cultivares IACSP94-
2094 e IACSP95-5000, sendo o dia 0 (testemunha) medida feita após 18
dias de aclimatação a 32/20 °C (dia/ noite) com plantas irrigadas; dia 2
medida feita após 34 horas a 22/12 °C (dia/ noite) com plantas irrigadas
(I) e não irrigadas (NI); dia 13 medida feita após 13 dias de baixa
temperatura em plantas irrigadas e não irrigadas; dia 20 medida após 20
dias de baixa temperatura em plantas irrigadas e não irrigadas (máximo
estresse); dia 22 medida após 2 dias de retorno à temperatura de 32/20
°C e reidratação e dia 28 medida após 8 dias de recuperação das plantas.
Símbolos indicam média de 20 repetições ± erro
padrão..........................................................................................................
59
Figura 6- (A, B) Variação do fator de eficiência do FSII (Fq'/Fv') e do (C, D)
transporte aparente de elétrons (ETR) de cana-de-açúcar, cultivares
IACSP94-2094 e IACSP95-5000, sendo o dia 0 (testemunha) medida
feita após 18 dias de aclimatação a 32/20 °C (dia/ noite) com plantas
irrigadas; dia 2 medida feita após 34 horas a 22/12 °C (dia/ noite) com

xv
plantas irrigadas (I) e não irrigadas (NI); dia 13 medida feita após 13
dias de baixa temperatura em plantas irrigadas e não irrigadas; dia 20
medida após 20 dias de baixa temperatura em plantas irrigadas e não
irrigadas (máximo estresse); dia 22 medida após 2 dias de retorno à
temperatura de 32/20 °C e reidratação e dia 28 medida após 8 dias de
recuperação das plantas. Símbolos indicam média de 20 repetições ±
erro padrão..................................................................................................
60
Figura 7- (A, B) Variação no teor dos açúcares solúveis (AS), da (C, D) sacarose
(SAC) e do amido (AMI) em folhas de cana-de-açúcar, cultivares
IACSP94-2094 e IACSP95-5000, sendo o dia 0 (testemunha) medida
feita após 18 dias de aclimatação a 32/20 °C (dia/ noite) com plantas
irrigadas; dia 2 medida feita após 34 horas a 22/12 °C (dia/ noite) com
plantas irrigadas (I) e não irrigadas (NI); dia 13 medida feita após 13
dias de baixa temperatura em plantas irrigadas e não irrigadas; dia 20
medida após 20 dias de baixa temperatura em plantas irrigadas e não
irrigadas (máximo estresse); dia 22 medida após 2 dias de retorno à
temperatura de 32/20 °C e reidratação e dia 28 medida após 8 dias de
recuperação das plantas. Símbolos indicam média de quatro repetições ±
erro padrão..................................................................................................
61
Figura 8- Variação da atividade das enzimas (A, B) sintase de sacarose (SuSy) e da
(C, D) sintase de sacarose fosfato (SPS) em folhas de cana-de-açúcar,
cultivares IACSP94-2094 e IACSP95-5000, sendo o dia 0 (testemunha)
medida feita após 18 dias de aclimatação a 32/20 °C (dia/ noite) com
plantas irrigadas; dia 2 medida feita após 34 horas a 22/12 °C (dia/
noite) com plantas irrigadas e não irrigadas; dia 13 medida feita após 13
dias de baixa temperatura em plantas irrigadas e não irrigadas; dia 20
medida após 20 dias de baixa temperatura em plantas irrigadas e não
irrigadas (máximo estresse); dia 22 medida após 2 dias de retorno à
temperatura de 32/20 °C e reidratação e dia 28 medida após 8 dias de
recuperação das plantas. Símbolos indicam média de quatro repetições ±
erro padrão..................................................................................................
62
Figura 9- Variação da atividade das (A, B) invertases ácidas (IVA) e das (C, D)
invertases neutras (IVN) em folhas de cana-de-açúcar, cultivares
IACSP94-2094 e IACSP95-5000, sendo o dia 0 (testemunha) medida
feita após 18 dias de aclimatação a 32/20 °C (dia/ noite) com plantas
irrigadas; dia 2 medida feita após 34 horas a 22/12 °C (dia/ noite) com
plantas irrigadas e não irrigadas; dia 13 medida feita após 13 dias de
baixa temperatura em plantas irrigadas e não irrigadas; dia 20 medida
após 20 dias de baixa temperatura em plantas irrigadas e não irrigadas
(máximo estresse); dia 22 medida após 2 dias de retorno à temperatura
de 32/20 °C e reidratação e dia 28 medida após 8 dias de recuperação
das plantas. Símbolos indicam média de quatro repetições ± erro padrão.
63

xvi
ÍNDICE DE TABELAS
CAPÍTULO II
Tabela 1- Teor de açúcares solúveis totais (μmol g-1
MS) em folhas de cana-de-
açúcar cv. IACSP94-2094 submetida aos tratamentos: TN20, temperatura
noturna de 20 °C - irrigada; DH/TN20, temperatura noturna de 20 °C -
não irrigada; TN12, temperatura noturna de 12 °C - irrigada e DH/TN12,
temperatura noturna de 12 °C - não irrigada, no 5º dia de tratamento e 4º
dia de recuperação. Período de aplicação dos tratamentos, dias 1 a 5;
período de recuperação com retorno da irrigação das plantas e
temperatura noturna de 20 °C, dias 5 a 9....................................................
36
Tabela 2- Teor de sacarose (μmol g-1
MS) em folhas de cana-de-açúcar cv.
IACSP94-2094 submetida aos tratamentos: TN20, temperatura noturna
de 20 °C - irrigada; DH/TN20, temperatura noturna de 20 °C - não
irrigada; TN12, temperatura noturna de 12 °C - irrigada e DH/TN12,
temperatura noturna de 12 °C - não irrigada, no 5º dia de tratamento e 4º
dia de recuperação. Período de aplicação dos tratamentos, dias 1 a 5;
período de recuperação com retorno da irrigação das plantas e
temperatura noturna de 20 °C, dias 5 a 9....................................................
37
Tabela 3- Teor de amido (μmol de Glu g-1
MS) em folhas de cana-de-açúcar cv.
IACSP94-2094 submetida aos tratamentos: TN20, temperatura noturna
de 20 °C - irrigada; DH/TN20, temperatura noturna de 20 °C - não
irrigada; TN12, temperatura noturna de 12 °C - irrigada e DH/TN12,
temperatura noturna de 12 °C - não irrigada. No 5º dia de tratamento e 4º
dia de recuperação. Período de aplicação dos tratamentos, dias 1 a 5;
período de recuperação com retorno da irrigação das plantas e
temperatura noturna de 20 °C, dias 5 a 9....................................................
38
CAPÍTULO III
Tabela 1- Resposta do potencial hídrico foliar (Ψw6h) de cana-de-açúcar cv.
IACSP94-2094 e cv. IACSP95-5000 submetida aos tratamentos de baixa
temperatura e deficiência hídrica. Médias de quatro repetições (± desvio
padrão).........................................................................................................
54

xvii
Fotossíntese e metabolismo de carboidratos em plantas jovens de cana-de-açúcar sob
baixa temperatura e deficiência hídrica
RESUMO
O produto mais importante da cana-de-açúcar é a sacarose acumulada nos colmos. A
diferença na capacidade de armazenar sacarose entre genótipos de cana-de-açúcar está
relacionada com fatores fisiológicos, bioquímicos e ambientais. A ocorrência de temperaturas
baixas e deficiência hídrica afetam a fisiologia da cana-de-açúcar. O objetivo deste trabalho
foi estudar a influência da baixa temperatura e da deficiência hídrica sobre a fotossíntese,
atividade das enzimas do metabolismo de carboidratos e conteúdo de carboidratos foliares.
Foram realizados dois estudos, o primeiro utilizando a cultivar IACSP94-2094 e o segundo
experimento utilizando duas cultivares de cana-de-açúcar, IACSP94-2094 e IACSP95-5000
que exibem diferenças em sua rusticidade. No primeiro estudo, verificaram-se as respostas
fotossintéticas da cana-de-açúcar aos efeitos simultâneos e isolados da baixa temperatura
noturna (TN) e da deficiência hídrica (DH). Após 128 dias do plantio, as plantas da cultivar
IACSP94-2094 foram submetidas aos seguintes tratamentos: 1) testemunha, com temperatura
noturna (TN) de 20 °C irrigada (TN20); 2) TN de 20 °C com deficiência hídrica (TN20/DH); 3)
TN de 12 °C irrigada (TN12) e 4) TN de 12 °C com deficiência hídrica (TN12/DH) por cinco
dias. Após o período de tratamento, as plantas foram irrigadas e retornaram à temperatura
noturna de 20 °C por mais quatro dias, para recuperação. Houve decréscimos na assimilação
de CO2 nos tratamentos TN20/DH, TN12 e TN12/DH. A recuperação total da assimilação de
CO2 foi observada apenas nas plantas do tratamento de baixa temperatura noturna. Com a
ocorrência simultânea da baixa temperatura noturna e da deficiência hídrica foram observados
efeitos negativos na condutância estomática, na eficiência máxima da ribulose-1,5-bisfosfato
carboxilase, no transporte aparente de elétrons, no fator de eficiência e na eficiência
operacional do fotossistema II, causando limitações difusivas, bioquímicas e fotoquímicas da
fotossíntese. A ocorrência de baixa temperatura noturna e déficit hídrico causou queda no teor
de amido foliar, favorecendo o aumento do teor de sacarose foliar. No segundo estudo
verificou-se as respostas da fotossíntese e do metabolismo de carboidratos de cana-de-açúcar
sob baixa temperatura e deficiência hídrica. Para tanto foram utilizadas duas cultivares de
cana-de-açúcar, IACSP94-2094 e IACSP95-5000. Aos 87 dias após o plantio, as plantas
foram submetidas aos tratamentos de baixa temperatura (22±1/12±1 °C) e deficiência hídrica,
por 22 dias, em câmara de crescimento. Após este período, as plantas foram reidratadas e a
temperatura retornou a 32±1/20±1 °C, por 9 dias. Sob condições ambientais ideais, a cultivar

xviii
IACSP95-5000 tem maior capacidade fotossintética que a cultivar IACSP94-2094. Após
imposição dos tratamentos, em ambas as cultivares, foram observados decréscimos da
assimilação de CO2 devido a fatores difusivos, metabólicos e fotoquímicos. Entretanto, a
cultivar IACSP95-5000 foi mais tolerante ao frio devido à menor redução da assimilação de
CO2 e melhor recuperação. No entanto, sob frio e deficiência hídrica, a cultivar IACSP94-
2094 foi mais tolerante. Com a imposição dos tratamentos, foi observado aumento no teor de
açúcares solúveis e amido foliar em ambas cultivares. Entretanto, na cultivar IACSP94-2094
sob baixa temperatura e deficiência hídrica o aumento dos açúcares solúveis totais foi devido
ao aumento da sacarose, quando há também aumento da atividade da sintase de sacarose
fosfato.
Palavras-Chave: Saccharum spp., trocas gasosas, fluorescência da clorofila, resfriamento,
sintase de sacarose fosfato

xix
Sugarcane photosynthesis and carbohydrate metabolism in young sugarcane at low
temperature and water deficit
ABSTRACT
Sucrose accumulated in stems is the most important product of sugarcane. The ability
difference to store sucrose among genotypes of sugarcane is related to physiological,
biochemical and environmental factors. The occurrence of low temperatures and water deficit
are common factors affecting the physiology of sugarcane. The aim of this work was to study
the influence of low temperature and water deficit on photosynthesis, carbohydrate
metabolism enzymes activity and leaf carbohydrate profile. Two studies were conducted, first
using IACSP94-2094 cultivar and in the second study we using two sugarcane cultivars,
IACSP94-2094 and IACSP95-5000 which have differences in their hardiness. In the first, it
was verified the photosynthetic responses of sugarcane at low night temperature (TN) and
water deficit (DH) applied isolated and combined. After 128 planting days, IACSP94-2094
plants were treated for five days with the following treatment: 1) control, with night
temperature (TN) 20 °C and watered (TN20); 2) TN 20 °C and water deficit (TN20/DH); 3) TN
12 °C and watered (TN12) and 4) TN 12 °C and water deficit (TN12/DH). After the treatment
period, plants were watered and returned to the nighttime temperature of 20 °C for four days
for recovery. There was a decrease in the CO2 assimilation in treatments TN20/DH, TN12 e
TN12/DH. The total CO2 assimilation recovery was observed only in low night temperature.
The combined low night temperature and water deficit caused a negative effect on stomatal
conductance, maximum capacity of ribulose-1,5-bisphosphate carboxylase, apparent electron
transport, PSII efficiency factor and PSII operating efficiency, causing diffusive, biochemical
and photochemical limitations of photosynthesis. Low night temperature and water deficit
caused decreases in leaf starch content, favoring an increase in sucrose content. In the second
study, it was examined the responses of photosynthesis and carbohydrate metabolism of
sugarcane under low temperature and water deficit. We used two sugarcane cultivars,
IACSP94-2094 and IACSP95-5000. At 87 days after planting, plants were treated with low
temperature (22±1/12±1 °C) and water deficit for 22 days in a growth chamber. After this
period, plants were rehydrated and the temperature returned to 32 ± 1/20 ± 1 °C for 9 days.
Under ideal environmental conditions IACSP95-5000 has a higher photosynthetic capacity
than IACSP94-2094 cultivar. After imposition of the treatments in both cultivars were
observed decreases in CO2 assimilation due to diffusive, metabolic, and photochemical

xx
factors. However the IACSP95-5000 cultivar was more tolerant to chilling, due to lower
reduction in CO2 assimilation and better recovery. While under low temperature and water
deficit, the IACSP94-2094 cultivar was more tolerant. With the imposition of the treatments,
it was observed an increase in soluble sugars and starch in both cultivars. However, the
soluble sugars increase on IACSP94-2094 cultivar under low temperature and water deficit,
was due sucrose increase, when there is an activity increase of sucrose phosphate synthase.
Key Words: Saccharum spp., gas exchange, chlorophyll fluorescence, chilling, sucrose
phosphate synthase

1
CAPÍTULO I

2
1 INTRODUÇÃO
A cana-de-açúcar tem importância mundial como fonte alimentar e de energia e o seu
cultivo no Brasil tem crescido significativamente nos últimos anos. Essa expansão foi
ocasionada pelo incentivo da indústria sucro-alcooleira, alavancada pelo consumo crescente
de etanol e pela política mundial de bioenergia (FRONZAGLIA, 2007; YUAN et al., 2008).
A sustentabilidade da produção agrícola da cana-de-açúcar no Brasil está fundamentada no
suprimento contínuo de variedades com maior tolerância às pragas e doenças e às variações
ambientais (MACEDO, 2007).
A necessidade dos países desenvolvidos substituírem os derivados de petróleo por
biocombustíveis estimulou a demanda global de etanol. Em vários países, sobretudo nos
Estados Unidos, a produção local não vem sendo suficiente para o consumo e o setor
sucroalcooleiro do Brasil rapidamente respondeu a essa nova demanda com safras recordes
consecutivas (FNP CONSULTORIA & COMÉRCIO, 2009). Porém, recentemente na região
Centro-Sul do Brasil, houve uma queda da produtividade devido às adversidades ambientais,
chuvas em excesso e geadas, e entre os meses de junho e agosto houve períodos longos com
baixas temperaturas (FNP CONSULTORIA & COMÉRCIO, 2012; UNICA, 2012).
O Estado de São Paulo responde por 60% da produção nacional de cana-de-açúcar
(FNP CONSULTORIA & COMÉRCIO, 2012) e a área cultivada com cana-de-açúcar tem se
expandido para regiões situadas a Oeste e Noroeste do Estado (EMBRAPA, 2009), em áreas
marginais onde há variação anual acentuada da disponibilidade hídrica (ROLIM et al., 2007).
O produto mais importante da cana-de-açúcar é a sacarose acumulada nos colmos. O
acúmulo de sacarose em cana-de-açúcar é o resultado final do ciclo de síntese e hidrólise da
sacarose, envolvendo a atividade de várias enzimas tanto na fonte como no dreno. A diferença
na capacidade de armazenar sacarose entre genótipos de cana-de-açúcar está relacionada com
fatores morfológicos, enzimáticos e ambientais (MOORE, 2005; RAE et al., 2005). Para
entender o armazenamento de sacarose no colmo é necessário identificar os principais fatores
limitantes desse processo, ou seja: fotossíntese e síntese de sacarose; taxa de carregamento,
transporte e descarregamento no floema durante a maturação e taxa de transporte de sacarose
para o armazenamento no parênquima e vacúolos. Nos meses de inverno há acúmulo
significativo de sacarose no colmo, quando a baixa temperatura e a seca são fatores
ambientais que afetam a fisiologia da cana-de-açúcar. Estas condições causam a queda no

3
crescimento da cana-de-açúcar e favorecem o acúmulo de sacarose nos vacúolos das células
do parênquima (RAE et al., 2005). Tais condições causam queda no processo fotossintético da
cana-de-açúcar, cujo metabolismo fotossintético C4 é menos eficiente sob frio e seca
(CARMO-SILVA et al., 2008; DU & NOSE, 2002; MACHADO et al., 2009; SAGE, 2007).
Os efeitos da ocorrência de deficiência hídrica e de baixa temperatura causam várias
alterações fisiológicas, e o grau dessas alterações é decorrente da intensidade do estresse e
depende do genótipo (DU & NOSE, 2002; MACHADO et al., 2009; RIBEIRO et al., 2013;
SALES et al., 2012; SMIT & SINGELS, 2006).
O objetivo deste trabalho foi testar a hipótese que cultivares de cana-de-açúcar
tolerantes à deficiência hídrica e/ou à baixa temperatura apresentam metabolismo do carbono
menos suscetível a estes fatores ambientais, estudando seus efeitos sobre a fotossíntese,
atividade das enzimas do metabolismo de carboidratos e conteúdo de carboidratos foliares em
plantas jovens de duas cultivares de cana-de-açúcar.
Esta tese foi dividida em dois experimentos, sendo o primeiro avaliando o efeito
simultâneo da deficiência hídrica e baixa temperatura noturna sobre a fotossíntese e conteúdo
de carboidratos foliares de plantas jovens de cana-de-açúcar na cultivar IACSP94-2094.
No segundo experimento, foi avaliado o efeito da baixa temperatura diária e da
deficiência hídrica sobre a fotossíntese, atividade das enzimas do metabolismo de
carboidratos e conteúdo de carboidratos foliares em plantas jovens de cana-de-açúcar, nas
cultivares IACSP94-2094 e IACSP95-5000.
2 REVISÃO DE LITERATURA
A cana-de-açúcar possui metabolismo fotossintético do tipo C4, na qual a assimilação
de CO2 pode atingir valores próximos de 63 mol CO2 m-2
s-1
(MOORE & MARETZKI,
1996). Em apenas um dia, a cana-de-açúcar pode acumular 40 g m-2
de fitomassa, sendo
grande parte do carbono assimilado direcionado aos colmos (MACHADO et al., 1982;
MOORE & MARETZKI, 1996). Apesar da grande capacidade fotossintética da cana-de-
açúcar, não há relação direta com a produção de sacarose e com o acúmulo nos colmos. Essa
afirmativa é sustentada pela comparação de duas espécies de Saccharum: S. spontaneum, que
tem baixa produção de sacarose (2% sacarose/ massa fresca), enquanto a S. officinarum tem
alta produção (25% sacarose/ massa fresca), entretanto observou-se que a fotossíntese de S.
spontaneum é duas vezes maior que da S. officinarum (IRVINE, 1975; MOORE &

4
MARETZKI, 1996). A produção de sacarose em cana-de-açúcar está relacionada com a
produção de fitomassa, sendo ambos os processos incrementados pela máxima interceptação
de energia solar e/ ou alta eficiência na conversão de fitomassa (SINGELS et al., 2005). A
interceptação de radiação está relacionada com a dimensão do aparelho fotossintético, i.e.,
com o índice de área foliar. O acúmulo de sacarose nos colmos é regulado pela capacidade de
armazenar açúcar e pelo metabolismo e transporte de açúcar tanto na fonte como no dreno. Há
evidências que tanto a atividade da fonte como a do dreno são determinantes na produção e
acúmulo de sacarose (GROF & CAMPBELL, 2001; MOORE & MARETZKI, 1996;
MOORE, 2005; RAE et al., 2005).
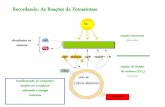
O acúmulo de sacarose é um processo complexo envolvendo diversas etapas (Figura
1).
Figura: 1 - Produção, transporte e acúmulo de sacarose em cana-de-açúcar. Adaptado de
GROF e CAMPBELL (2001).

5
É necessário compreender os fatores que limitam essas etapas, incluindo: a
fotossíntese, as enzimas envolvidas na síntese e partição de sacarose, o carregamento da
sacarose no floema das folhas e o descarregamento nos tecidos dreno, além da taxa de
armazenamento primário em células do parênquima e vacúolos e a taxa de remobilização de
sacarose para o crescimento vegetativo.
O acúmulo de sacarose varia de acordo com o genótipo, estádio de desenvolvimento
da planta e do ambiente em que é cultivada. A planta responde ao ambiente através da
transdução de sinais que coordenam o seu desenvolvimento, além do acúmulo de sacarose
(GROF & CAMPBELL, 2001; MOORE, 2005).
A fotossíntese é o principal mecanismo que transforma a energia solar em energia
química utilizável (ATP) e em NADPH, nas membranas dos tilacóides no cloroplasto.
A característica de alta produtividade de fotoassimilados em plantas C4 é atribuída à
cooperação metabólica de dois tipos de células das folhas fotossinteticamente ativas, que
constituem a anatomia do tipo Kranz, na bainha do feixe vascular (BFV) (HATCH, 1987).
As plantas de metabolismo do tipo C4 estão agrupadas em três sub-tipos bioquímicos,
que diferem principalmente no ácido C4 transportado (malato ou aspartato) e na forma de
descarboxilação. O primeiro grupo, do qual faz parte a cana-de-açúcar entre outras plantas
cultivadas, é o NADP-ME em que a enzima málica é dependente de NADPH e a
descarboxilação do ácido C4 ocorre no cloroplasto das células da BFV. O segundo grupo é o
NAD-ME, no qual a enzima málica é dependente de NADH e a descarboxilação do ácido C4
ocorre na mitocôndria das células da BFV. No terceiro grupo a descarboxilação é realizada
pela fosfoenolpiruvato carboxiquinase (PCK) e ocorre predominantemente no citoplasma das
células da BFV (GHANNOUM, 2009; TAIZ & ZEIGER, 2009; VON CAEMMERER &
FURBANK, 2003).
A fixação de CO2 ocorre inicialmente nos cloroplastos das células do mesofilo foliar
através da enzima fosfoenolpiruvato (PEP) carboxilase (PEPcase), onde é produzido ácido
oxaloacético (OAA) que é convertido em malato, que se difunde para as células da BFV. Na
BFV o OAA é descarboxilado resultando em CO2 que é fixado através da ribulose bisfosfato
carboxilase/oxigenase (Rubisco), no ciclo de Calvin. Na BFV a descarboxilação do malato
resulta em CO2 e piruvato em reação catalisada pela enzima citoplasmática NADP-málica
(HATCH, 1987). O produto de três carbonos (piruvato) do ciclo de Calvin retorna ao mesofilo
sendo utilizado na síntese de PEP, receptor inicial de CO2, com utilização de ATP. A via C4
funciona como uma "bomba" bioquímica que concentra o CO2 nas células da BFV de tal
forma a saturar eficazmente o ciclo de Calvin e inibir a fotorrespiração (LUNN &

6
FURBANK, 1999), que em plantas C3 é responsável por uma perda substancial de
fotoassimilados devido à oxidação.
Assim, a energia extra envolvida na supressão da fotorrespiração nas plantas C4 lhe
permite um aumento significativo na produtividade potencial sobre as plantas C3,
especialmente em ambientes onde a temperatura e intensidade de luz são altas (SAGE, 2007).
No estroma dos cloroplastos das células da BFV, ATP e NADPH são utilizados na redução do
CO2 à triose-P. A partir da triose-P são sintetizados a sacarose e o amido. A sacarose é
transportada para todos os órgãos da planta (HARTT et al., 1963), e constitui o substrato
primário para o crescimento e desenvolvimento enquanto o amido é um carboidrato de reserva
temporário nas folhas. Em cana-de-açúcar supõe-se que o amido seja sintetizado no
cloroplasto das células da BFV e a sacarose no citoplasma do mesofilo (GROF & CAMPBEL,
2001; LUNN & FURBANK, 1999).
Em cana-de-açúcar a sacarose além de principal produto da fotossíntese, é uma
molécula de transporte envolvida no crescimento, desenvolvimento, armazenamento,
transdução de sinais e aclimatação a estresses ambientais (HARTT et al., 1963; SALERNO &
CURATTI, 2003). A síntese de sacarose pode ser catalisada por duas enzimas: a sintase de
sacarose fosfato (SPS):
e a sintase de sacarose (SuSy):
A SPS é uma proteína de baixa abundância (< 0,1% da proteína solúvel foliar) e é
relativamente instável (HUBER & HUBER, 1996). É considerada uma enzima chave no
processo de síntese de sacarose, porém ambas as enzimas (SPS e SuSy) estão solúveis no
citoplasma e catalisam livremente as reações. Entretanto, a principal via de síntese de sacarose
envolve a ação sequencial da SPS, que catalisa a penúltima etapa da rota de síntese e da
enzima fosfatase de sacarose fosfato (SPP;) que remove rapidamente o fosfato inorgânico (Pi)
da sacarose-6-fosfato liberando a sacarose. A liberação da sacarose torna a reação da SPS
irreversível, proporcionando uma eficiente produção de sacarose, mesmo em condições de
baixa concentração de substrato (HUBER & HUBER, 1996; SALERNO & CURATTI, 2003).
A SPS exerce controle maior em altas taxas fotossintéticas e, como tal, tem grande
controle sobre o fluxo máximo através da rota de síntese de sacarose (HUBER & HUBER,
1996). Além disso, a SPS é o passo limitante da velocidade da biossíntese da sacarose, e se
UDP-glicose + frutose sacarose + UDP + H+
UDP-glicose + frutose-6-fosfato sacarose-6-fosfato + UDP + H+

7
correlaciona com exportação deste açúcar (HUBER & HUBER, 1996; STITT et al.,1988).
GROF & CAMPBEL (2001) observaram que a atividade da SPS foliar está correlacionada
com o conteúdo de sacarose entre cultivares de cana-de-açúcar, entretanto isso somente no
tecido fonte.
A SPS também está presente em outros tecidos que atuam na síntese de sacarose,
como por exemplo, frutos em fase de amadurecimento, e em cana-de-açúcar (RAE et al.,
2005), tendo importante ação sobre o acúmulo e metabolismo da sacarose nos colmos (GROF
et al., 2007). Os mecanismos de controle da SPS são: a expressão gênica, o controle alostérico
pela glicose-6-fosfato (Glu-6-P) (ativador) e Pi (inibidor) e ainda pela fosforilação reversível
da porção seril da molécula da enzima (HUBER & HUBER, 1996; VERMA et al., 2011).
A sacarose é sintetizada nas células do mesofilo e também como resultado da hidrólise
de amido na BFV (Figura 1). A sacarose sintetizada nas folhas da cana-de-açúcar é
transportada para os outros tecidos, via floema. Duas hipóteses de como a sacarose entra no
floema foram postuladas: o carregamento simplástico, através do plasmodesmata, e
carregamento apoplástico, mediada por um sistema de transporte ativo (FROMMER &
SONNEWALD, 1995). Em cana-de-açúcar, as células do floema não estão conectadas a
outras células da folha por plasmodesmas (ROBINSON-BEERS & EVERT, 1991) sugerindo
que o carregamento do floema ocorra, principalmente, via apoplasto. O carregamento ativo
ocorre no sentido da célula do mesofilo para as células do floema, contra um gradiente de
concentração. O gradiente de prótons, que é necessário para o co-transporte de sacarose e de
prótons (DELROT, 1981), é gerado por uma H+-ATPase, localizada na membrana plasmática
das células companheiras (BOUCHE-PILLON et al., 1994).
O transporte da sacarose da fonte para os drenos inicia-se com seu movimento a partir
do citoplasma das células do mesofilo para os complexos células companheiras-elementos
crivados (cc-ec) do floema. Ou seja, o carregamento do floema, é uma interface entre a
produção de fotoassimilados na fonte e o seu consumo nos drenos. O carregamento do floema
é regulado tanto pela fonte como pelo dreno (SMITH & STITT, 2007). Em cana-de-açúcar o
carregamento do floema ocorre possivelmente via apoplasto nas folhas. No floema o
transporte da sacarose a partir das folhas para os outros órgãos drenos, ocorre em resposta a
um gradiente de concentração (VAN BEL, 2003; RAE et al., 2005).
O fluxo de sacarose das células do mesofilo para o complexo cc-ec é afetado pela
temperatura (DU & NOSE, 2002), deficiência hídrica (DU et al., 1998), e pela atividade de
enzimas relacionadas com o metabolismo da sacarose, como a SPS, SuSy, invertases neutras
(IVN), invertases ácidas (IVA) (VERMA et al., 2010) e demanda por fotoassimilados pelo

8
dreno (WARDLAW, 1990). Em condições limitantes na folha, o aumento da fotossíntese
líquida acarreta aumentos proporcionais ao fluxo de fotoassimilados. Durante o curso de um
dia há variação no fluxo de radiação e consequentemente, na produção fotossintética. Sob alta
radiação o excesso de fotoassimilado é armazenado como amido no cloroplasto (PAUL &
PELLNY, 2003) e/ou como sacarose nos vacúolos (SOUZA, 2011). Conforme ocorre
diminuição da radiação e queda na fotossíntese pode ocorrer mobilização e exportação de
amido acumulado durante o dia (SMITH & STITT, 2007; SOUZA, 2011). Durante a noite o
amido é degradado produzindo sacarose, a qual é transportada e utilizada metabolicamente. A
intensidade de remobilização e de exportação durante a noite é consistente com o teor de
amido nas folhas no final do dia (HENDRIX & GRANGE 1991).
O fluxo de exportação da sacarose parece ser definido pela atividade da SPS
(GALTIER et al., 1993; HARTT et al., 1963; VERMA et al., 2011) que é afetada pela
demanda do dreno e pelo ambiente (DU et al., 1998; DU & NOSE, 2002; YANG et al., 2001).
Por exemplo, a duração do dia tem efeito significativo sobre a partição de fotoassimilados
entre a sacarose e o amido. Há forte correlação na proporção de sacarose e de amido em
folhas com a atividade da SPS (GALTIER et al., 1993). Sob condições de dias curtos o
acúmulo de amido aumenta e há queda na atividade da SPS. O aumento da síntese de amido
durante o dia possibilita a manutenção da exportação de fotoassimilados durante o período da
noite (SMITH & STITT, 2007). A taxa de exportação de sacarose está relacionada com o teor
de amido nas folhas no final do dia. Desta forma, a atividade da SPS nas folhas desempenha
um papel crucial na partição de carbono, a partir do substrato da hidrólise do amido. Além
disso, os níveis elevados de SPS têm o potencial de aumentar as taxas fotossintéticas em
condições favoráveis (GALTIER et al., 1993). Ocorre, portanto uma coordenação entre a
produção de fotoassimilados e a utilização destes produtos para o metabolismo e crescimento
(GRAHAM & MARTIN, 2000).
O movimento da sacarose a partir do floema para o parênquima de armazenamento
inicia-se com o descarregamento do floema. A presença de inúmeros plasmodesmas nas
células sugere que as células sejam conectadas simplasticamente e que o transporte de
sacarose poderia ser potencialmente via simplasto. No entanto, a presença de sacarose no
apoplasto sugere que a sacarose também seja descarregada via apoplasto (RAE et al., 2005).
Assim, a sacarose e os produtos da sua hidrólise (hexoses) pelas IVA (GLASZIOU &
GAYLER, 1972) podem ser acumulados nas células do parênquima, via transportadores de
membrana. Sugere-se que a atividade das invertases mantém o gradiente de sacarose entre a
fonte e o floema, dando continuidade ao descarregamento do floema.

9
A rota do movimento de sacarose e o local da sua quebra, além de serem fundamentais
para o mecanismo de importação, têm importância devido aos sinais gerados pelos açúcares.
Dependendo da via de entrada de sacarose nos drenos, ou seja, via plasmodesmata ou parede
celular, a sacarose pode ser quebrada pela invertase de parede celular, invertase
citoplasmática ou invertase vacuolar (produzindo hexoses) ou pela SuSy (gerando frutose e
UDP-glicose) (KOCH, 2004). Entretanto na quebra da sacarose via invertases há duas vezes
mais produção de hexoses que pela SuSy.
Como descrito anteriormente, a SuSy também está envolvida com a síntese, assim
como na quebra da sacarose, gerando UDP-glicose e frutose, sendo esta última a, sua função
principal (SALERNO & CURATTI, 2003). A quebra da sacarose é vital em plantas, não só na
alocação do carbono, mas na sinalização a base de hexoses nos drenos. Apenas as reações das
invertases e da SuSy estão envolvidas na rota da quebra da sacarose in vivo, sendo a regulação
dessas reações e suas consequências, importantes no metabolismo de carbono em plantas
(KOCH, 2004). De maneira geral, a SuSy está envolvida em processos de direcionamento da
sacarose a processos anabólicos, partição de sacarose entre fonte e dreno, em respostas à
anaerobiose e frio, armazenamento e maturação (KOCH, 2004; STURM & TANG, 1999).
As invertases estão relacionadas com a quebra da sacarose em glicose e frutose. As
invertases presentes no citoplasma tem pH ótimo entre 6,5 e 8,0, sendo chamadas de
invertases neutras (IVN) e as presentes nos vacúolos e parede celular, tem um pH ótimo ácido
(pH 5,0), portanto sendo chamadas de invertases ácidas (IVA). Geralmente a invertase da
parede celular está envolvida na partição da sacarose entre fonte e dreno, respiração, redução
do turgor em zonas relacionadas ao carregamento do floema, respostas a ferimentos e
infecções e no controle da diferenciação celular e desenvolvimento da planta. A invertase
vacuolar está envolvida no processo de osmorregulação e expansão celular, respiração,
máxima geração de hexoses no vacúolo, controle da composição de açúcares em frutas e
órgão de armazenamento e resposta ao frio. A invertase citoplasmática tem provável função
no catabolismo (STURM & TANG, 1999; KOCH, 2004).
Em cana-de-açúcar, um acúmulo significativo de sacarose ocorre no inverno, quando
as baixas temperaturas e a seca são fatores ambientais comuns que afetam a fisiologia da
planta. No inverno, a baixa taxa de crescimento da planta favorece os processos de acúmulo
de sacarose nos colmos, ou seja, crescimento ativo e armazenamento são processos
competitivos e determinados pelas condições do ambiente (HATCH & GLASZIOU, 1963).
A baixa temperatura e a deficiência hídrica são fatores que afetam diretamente o
crescimento e produtividade dos cultivos agrícolas (MACHADO et al., 2009; PEARCE,

10
1999; PIMENTEL, 2004). A taxa máxima de crescimento da cana-de-açúcar ocorre entre 25 e
35 °C e quando expostas a temperatura de 15 °C já se observa inibição do crescimento
vegetativo (EBRAHIM et al., 1998; SALES et al., 2012).
A mudança de temperatura incide diretamente sobre todo processo cinético e
termodinâmico nos aspectos bioquímicos e fisiológicos da planta (PEARCE, 1999). Sob baixa
temperatura, as plantas são classificadas em três categorias em relação a sensibilidade: 1)
suscetíveis ao frio, ou seja, são danificadas por temperaturas abaixo de 12 °C; 2) tolerante ao
frio, mas suscetíveis ao congelamento, ou seja, podem aclimatar em temperaturas inferiores a
12 °C, mas são incapazes de sobreviver ao congelamento; e 3) tolerantes ao congelamento, ou
seja, capazes de se adaptarem para sobreviver em temperaturas abaixo de zero. A baixa
temperatura tem efeito direto sobre as células, enquanto o congelamento, muitas vezes age de
forma indireta e danificando as células pela desidratação (PEARCE, 1999). Entretanto, em
espécies tropicais sensíveis ao resfriamento podem ocorrer danos mesmo quando expostas a
temperaturas superiores à de congelamento do tecido (KAKANI et al., 2008; SAGE, 2007).
Folhas de plantas expostas ao resfriamento mostram inibição da fotossíntese,
translocação de sacarose, menor respiração, inibição do metabolismo de proteínas, geração de
espécies reativas de oxigênio, crescimento lento e murcha foliar. Estas modificações são
causadas por disfunções em processos metabólicos promovidos por alterações das
propriedades da membrana, mudanças na estrutura de proteínas e nas interações entre
macromoléculas, além de inibição de reações enzimáticas (CARMO-SILVA et al., 2008;
KAKANI et al., 2008; LIU et al., 2012; SOARES-CORDEIRO et al., 2010).
Entretanto, plantas que permanecem ativas durante o inverno, têm a respiração, a
fotossíntese e a síntese de proteínas reguladas pelo frio (GUY, 1990). Em geral, essa
regulação do metabolismo primário é essencial para sustentar o crescimento, ainda que este
seja menor que em temperaturas mais elevadas (PEARCE, 1999). Segundo LEVITT (1980) e
SAKAI & LARCHER (1987) citados por PEARCE (1999), durante o crescimento sob baixas
temperaturas ocorre acúmulo de solutos como aminoácidos livres e, especialmente,
carboidratos. Uma possível explicação para esse acúmulo durante a aclimatação ao frio é que
nesse período há maior limitação do crescimento do que da fotossíntese, sendo assim uma
consequência direta do menor uso do carboidrato (PEARCE, 1999). A formação de reserva
contribui para o crescimento rápido quando o ambiente torna mais quente (PEARCE, 1999;
POLLOCK & JONES, 1979). Há uma variedade de solutos que podem ser acumulados e
correlacionados com a tolerância ao frio. Em gramíneas, por exemplo, foi observado o
acúmulo de sacarose e frutanos (POLLOCK & JONES, 1979).

11
Além das condições térmicas, a deficiência hídrica do solo constitui um dos estresses
mais limitantes da produtividade vegetal (PIMENTEL, 2004). A deficiência hídrica tem
impacto variável na produtividade agrícola dependendo da fase fenológica em que ocorre e da
cultivar (INMAN-BAMBER & SMITH, 2005; MACHADO et al., 2009, SALES et al., 2012).
A emergência da plântula e o período compreendido entre a pré e pós-floração são as fases
fenológicas de maior suscetibilidade à seca em termos de produção agrícola de grãos
(PIMENTEL, 2004). Contudo, nos cultivos em que os órgãos de interesse econômico não são
os frutos ou sementes, como no caso da cana-de-açúcar (colmo), os efeitos da deficiência
hídrica são prejudiciais quando a mesma ocorre na fase inicial de estabelecimento das plantas
(MACHADO, 2009), bem como na de intenso crescimento (ROBERTSON et al., 1999).
Sob deficiência hídrica, as plantas apresentam alterações morfofisiológicas, tais como
enrolamento e alteração do ângulo da folha, redução da área foliar, da transpiração, da
condutância estomática, da fotossíntese (comprometimento das etapas fotoquímica e
bioquímica), da condutividade hidráulica das raízes, modificação da atividade de enzimas do
metabolismo do carbono e mudanças nos teores de antioxidantes (GHANNOUM, 2009;
LOPES et al., 2011; MACHADO et al., 2009; RIBEIRO et al., 2013). Algumas destas
respostas visam reduzir os efeitos deletérios da baixa disponibilidade hídrica, constituindo,
portanto, mecanismos de tolerância à seca (KRAMER, 1980). No caso da cana-de-açúcar,
alguns genótipos mostram diferentes capacidades de recuperação no crescimento após eventos
de seca (LANDELL et al., 2004; MACHADO et al., 2009; SALES et al., 2012).
A fotossíntese sob deficiência hídrica decresce inicialmente devido ao fechamento
estomático e, com o agravamento da seca, também se evidenciam limitações metabólicas
(CARMO-SILVA et al., 2008; GHANNOUM et al., 2003; GHANNOUM, 2009; LOPES et
al., 2011). O fechamento estomático é a primeira linha de defesa contra dessecação, pois é
mais rápido que as mudanças no crescimento radicular, da área foliar, da ultraestrutura dos
cloroplastos, dos pigmentos e proteínas. Espécies tolerantes à seca tem controle estomático
que permite alguma fixação de carbono durante o estresse, melhorando assim a eficiência do
uso da água, ou ainda, os estômatos abrem rapidamente após reidratação (MACHADO et al.,
2009; YORDANOV et al., 2000).
São poucos os estudos envolvendo a atividade das enzimas do metabolismo da
sacarose e amido em folhas (fonte) de cana-de-açúcar sob deficiência hídrica e/ou baixa
temperatura, assim como as trocas gasosas quando estes fatores ocorrem de forma simultânea
(SALES et al., 2012). A maioria dos trabalhos relaciona as enzimas do metabolismo de
sacarose apenas com o transporte e armazenamento nos colmos (dreno). No entanto, o

12
conhecimento de como estas enzimas atuam nas folhas e os efeitos dos estresses ambientais
sobre suas atividades são fundamentais para a compreensão da partição dos fotoassimilados,
do crescimento e do acúmulo de sacarose em cana-de-açúcar (GROF & CAMPBELL, 2001).

13
3 REFERÊNCIAS BIBLIOGRÁFICAS
BOUCHÉ-PILLON, S.; FLEURAT-LESSARD, P.; FROMONT, J.C.; SERRANO, R.,
BONNEMAIN, J.L. Immunolocalization of the plasma membrane H+-ATPase in minor veins
of Vicia faba in relation to phloem loading. Plant Physiology, Rockville, v. 105, p. 691-697,
1994.
CARMO-SILVA, A.E.; POWERS, S.J.; KEYS, A.J.; ARRABAÇA, M.C. Photorespiration in
C4 grasses remains slow under drought conditions. Plant, Cell and Environment, Oxford,
v.31, p.925-940, 2008.
DELROT, S. Proton fluxes associated with sugar uptake in Vicia faba leaf tissues. Plant
Physiology, Rockville, v. 68, p. 706-711, 1981.
DU, Y.C.; NOSE, A.; WASANO, K.; UCHIDA, Y. Responses to water stress of enzyme
activities and metabolite levels in relation to sucrose and starch synthesis, the Calvin cycle
and the C4 pathways in sugarcane (Saccharum sp.) leaves. Australian Journal of Plant
Physiology, Melbourne, v. 25, p. 253-260, 1998.
DU, Y.C.; NOSE, A. Effects of chilling temperature on the activity of enzimes of sucrose
synthesis and the accumulation of saccharides in leaves of three sugarcane cultivars differing
in cold sensitivity. Photosynthetica, Praga, v.40, p. 389-395, 2002.
EBRAHIM, M.K.H.; VOGG, G.; OSMAN, M.N.E.H; KOMOR, E. Photosynthetic
performance and adaptation of sugarcane at suboptimal temperatures. Journal of Plant
Physiology, Melbourne, v.153, p.587-592, 1998.
EMBRAPA - EMPRESA BRASILEIRA DE PESQUISA AGROPECUÁRIA. A expansão da
cana-de-açúcar e sua sustentabilidade,
http://www.embrapa.br/imprensa/artigos/2008/A%20expansao%20da%20cana-de-
acucar%20e%20a%20sua%20sustentabilidade.pdf, (15 junho 2009).
FNP CONSULTORIA e COMÉRCIO. Agrianual 2009: Anuário da Agricultura Brasileiras.
São Paulo, p.235, 2009.
FNP CONSULTORIA e COMÉRCIO. Agrianual 2012: Anuário da Agricultura Brasileiras.
São Paulo, p.221, 2012.
FROMMER, W.B.; SONNEWALD, U. Molecular analysis of carbon partitioning in
solanaceous species. Journal of Experimental Botany, Oxford, v.46, p.587-607, 1995.
FRONZAGLIA, T. Cana-de-açúcar: expansão alarmante. Análises e Indicadores do
Agronegócio, São Paulo, v.1, p. 1-3, 2007.
GALTIER, N.; FOYER, C.H.; HUBER, J.; VOELKER, T.A.; HUBER, S.C. Effects of
elevated sucrose phosphate synthase activity on photosynthesis, assimilate partitioning and

14
growth in tomato (Lycopersicon esculentum var. UC82B). Plant Physiology, Rockville, v.
101, p. 535-543, 1993.
GHANNOUM, O.; CONROY, J.P.; DRISCOLL, S.P.; PAUL, M.J.; FOYER, C.H.;
LAWLOR, D.W. Non stomatal limitations are responsible for drought-induced photosynthetic
inhibition in four C4 grasses. New Phytologist, Oxford, v.159, p.599-608, 2003.
GHANNOUM, O. C4 photosynthesis and water stress. Annals of Botany, Oxford, v.103,
p.635-644, 2009.
GLASZIOU, K.T.; GAYLER, K.R. Sugar accumulation in sugarcane. Role of cell walls in
sucrose transport. Plant Physiology, Rockville, v. 49, p. 912-913, 1972.
GRAHAM IA; MARTIN, T. Control of photosynthesis, allocation and partitioning by sugar
regulated gene expression. In: Photosynthesis: physiology and metabolism. Eds.
LEEGOOD RC; SHARKEY, TD; von CAEMMERER S. Kluwer Academic Publisher, pp.
233-248, 2000.
GROF, C.P.L.; CAMPBELL, J.A. Sugarcane sucrose metabolism: scope for molecular
manipulation. Australian Journal of Plant Physiology, Melbourne, v. 28, p. 1-12, 2001.
GROF, C.P.L.; ALBERTSON, P.L.; BURSLE, J.; PERROUX, J.M.; BONNETT, G.D.AND
JOHN M. MANNERS, J.M. Sucrose-phosphate synthase, a biochemical marker of high
sucrose accumulation in sugarcane. Crop Science, Hoboken, v. 47, p. 1530-1539, 2007.
GUY, C.L. Cold acclimation and freezing stress tolerance: Role of protein metabolism.
Annual Review of Plant Physiology and Plant Molecular Biology, Palo alto, v. 41, p. 187-
223, 1990.
HARTT C.E.; KORTSCHAK, H. P.: FORBES, A. J.; BURR, G.O. Translocation of C14
in
Sugarcane. Plant Physiology, Rockville, v. 38, p.305-318, 1963.
HATCH, M.D. GLASZIOU, K.T. Sugar accumulation cycle in sugarcane. II. Relationship of
invertase activity to sugar content & growth rate in storage tissue of plants grown in
controlled environments. Plant Physiology, Rockville, v. 38, p. 344-348, 1963.
HATCH, M.D. C4 photosynthesis: a unique blend of modified biochemistry, anatomy and
ultrastructure. Biochimica et Biophysica Acta, Amsterdam, V. 895, P. 81-106, 1987.
HENDRIX, D.L.; GRANGE, R.I. Carbon partitioning and export from mature cotton leaves.
Plant Physiology, Rockville,v.95, p. 228-233, 1991.
HUBER, S.C.; HUBER, J.L. Role and regulation of sucrose-phosohate synthase in higher
plants. Annual Review of Plant Physiology and Plant Molecular Biology, Palo Alto, v. 47,
p. 431-444, 1996.
INMAN-BAMBER, N.G.; SMITH, D.M. Water relations in sugarcane and response to water
deficits. Field Crops Research, Amsterdam, v.92, p. 185-202, 2005.
IRVINE, J.E. Relations of photosynthetic rates and leaf and canopy characters to sugarcane
yield. Crop Science, Hoboken, v. 15, p. 671-676, 1975.

15
KAKANI, V.G.; SURABHI, G.K.; REDDY, K.R. Photosynthesis and fluorescence responses
of C4 plant Andropogon gerardii acclimated to temperature and carbon dioxide.
Photosynthetica, Praga, v.46, p.420-430, 2008.
KOCH, K. Sucrose metabolism: regulatory mechanisms and pivotal roles in sugar sensing and
plant development. Current Opinion in Plant Biology, London, v. 7, p. 235-246, 2004.
KRAMER, P.J. Drought stress, and the origins of adaptations. In: Adaptation of plants to
water and high temperature stress. Turner, N.C.; Kramer, P.J. (ed). New York, Wiley, p. 7-
22, 1980.
LANDELL, M.G.A.; CAMPANA, M.P.; FIGUEIREDO, P.; VASCONCELOS, A.C.M;
XAVIER, M.A.; BIDOIA, M.A.P.; PRADO, H.; SILVA, M.A.; DINARDO-MIRANDA,
L.L.; SANTOS, A.S.; PERECIN, D.; ROSSETTO, R.; SILVA, D.N.; MARTINS, A.L.M;
GALLO, P.B.; KANTACK, R.A.D.; AZANIA, C.A.A.M.; PINTO, L.R.; SOUZA, S.A.C.D.
Variedades de cana-de-açúcar para o centro-sul do Brasil. Campinas: IAC, 2004. 32p.
(Boletim técnico IAC 195 – 14ª Liberação do Programa Cana IAC).
LEVITT, J. Responses of Plants to Environmental Stresses, vol. 1, New York: Academic
Press, 1980.
LIU, Y.F.; QI, M.F.; LI, T.L. Photosynthesis, photoinhibition, and antioxidant system in
tomato leaves stressed by low night temperature and their subsequent recovery. Plant
Science, London, v.196, p.8-17, 2012.
LOPES, M.S., ARAUS, J.L.; VAN HEERDEN, P.D.R.; FOYER, C.H. Enhancing drought
tolerance in C4 crops. Journal of Experimental Botany, Oxford, v.62, p. 3135-3153, 2011.
LUNN, J.E.; FURBANK, R.T. Sucrose biosynthesis in C4 plants. New Phytologist, Oxford,
v. 143, p. 221-237, 1999.
MACEDO, I.C. A Energia da cana-de-açúcar – Doze estudos sobre a agroindústria da
cana-de-açúcar no Brasil e a sua sustentabilidade. 2 ed. São Paulo: Berlendis &
Vertecchia: UNICA, 2007. 235p.
MACHADO, E.C.; PEREIRA, A.R.; FAHL, J.I.; ARRUDA, H.V.; CIONE, J. Índices
biométricos de duas variedades de cana-de-açúcar. Pesquisa Agropecuária Brasileira,
Brasília, v. 17, p. 1323-1329, 1982.
MACHADO, R. S. Respostas fisiológicas de genótipos de cana-de-açúcar ao déficit
hídrico imposto na fase inicial de desenvolvimento. 2009. 64p. Dissertação (Mestrado em
Agricultura Tropical e Subtropical) – Pós-Graduação – IAC.
MACHADO, R.S.; RIBEIRO, R.V.; MARCHIORI, P.E.R.; MACHADO, D.F.S.P.;
MACHADO, E.C.; LANDELL, M.G.A. Respostas biométricas e fisiológicas ao déficit
hídrico em cana-de-açúcar em diferentes fases fenológicas. Pesquisa Agropecuária
Brasileira, Brasília, v. 44, p. 1575-1582, 2009.

16
MOORE, P.H.; MARETZKI, A. Sugarcane. In: Photoassimilate distribution in plants and
crops. Zamski, E.; Schaffer, A.A. (eds), New York: Marcel Dekker, 1996. p. 643-669.
MOORE, P.H. Integration of sucrose accumulation processes across hierarchical scales:
towards developing an understanding of the gene-to-crop continuum. Fields Crops Research,
Amsterdam, v.92, p. 119-135, 2005.
PAUL, M.J.; PELLNY, T.K. Carbon metabolite feedback regulation of leaf photosynthesis
and development. Journal of Experimental Botany, Oxford, v. 54, p. 539-547, 2003.
PEARCE, R. Molecular analysis of acclimation to cold. Plant Growth Regulation,
Dordrecht, v. 29, p. 47-76, 1999.
PIMENTEL, C. A relação da planta com a água. Seropédica, Edur, 2004, 191p.
POLLOCK, C.J.; JONES, T. Seasonal patterns of fructan metabolism in forage grasses. New
Phytologist, Oxford, v. 83, p. 8-15, 1979.
RAE, A. L.; GROF, C. P. L.; CASU, R. E.; BONNETT G. D. Sucrose accumulation in the
sugarcane stem: pathways and control points for transport and compartmentation. Field
Crops Research, Amsterdam, v. 92, p. 159-168, 2005.
RIBEIRO, R.V.; MACHADO, R.S.; MACHADO, E.C.; MACHADO, D.F.S.P.;
MAGALHÃES FILHO, J.R.; LANDELL, M.G.A. Revealing drought-resistance and
productive patterns in sugarcane genotypes by evaluating both physiological responses and
stalk yield. Experimental Agriculture, Cambridge, v.49, p. 212-224, 2013.
ROBERTSON, M.J.; INMAN-BAMBER, N.G.; MUCHOW, R.C.; WOOD, A.W. Physiology
and productivity of sugarcane with early and mid-season water deficit. Field Crop Research,
Amsterdam, v. 64, p. 211-227, 1999.
ROBINSON-BEER, K.; EVERT, R.F. Ultrastruture of and plasmosdesmatal frequency in
mature leaves of sugarcane. Planta, New York, v. 184, p. 291-306, 1991.
ROLIM, G.S.; CAMARGO, M.B.P.; LANIA, D.G.; MORAES, J.F.L. Classificação climática
de Köppen e de Thornthwaite e sua aplicabilidade na determinação de zonas agroclimáticas
para o Estado de São Paulo. Bragantia, Campinas, v.66, p. 711-720, 2007.
SAGE, R.F. The temperature response of C3 and C4 photosynthesis. Plant, Cell and
Environment, Oxford, v.30, p.1086-1106, 2007.
SAKAI, A.; LARCHER, W. Frost Survival of Plants. Berlin: Springer, 1987.
SALERNO, G.L.; CURATTI, L. Origin of sucrose metabolism in higher plants: when, how
and why? Trends in Plant Science, London, v. 8, p. 63-69, 2003.
SALES, C.R.G.; RIBEIRO, R.V.; MACHADO, D.F.S.P.; MACHADO, R.S.; DOVIS, V.L.;
LAGÔA, A.M.M.A. Trocas gasosas e balanço de carboidratos em plantas de cana-de-açúcar
sob condições de estresses radiculares. Bragantia, Campinas, v.71, p.319-327, 2012.

17
SINGELS, A.; SMIT, M.A.; REDSHAW, K.A.; DONALDSON, R.A. The effect of crop start
date, crop class and cultivar on sugarcane canopy development and radiation interception.
Field Crops Research, Amsterdam, v. 92, p. 249-260, 2005.
SMIT, M.A.; SINGELS, A. The response of sugarcane canopy development to water stress.
Field Crops Research, Amsterdam, v.98, p.91-97, 2006.
SMITH AM; STITT M. Coordination of carbono supply and plant growth. Plant, Cell &
Environment, Oxford, v.30, p. 1126-1149, 2007)
SOARES-CORDEIRO, A.S.; DRISCOLL, S.P.; ARRABAÇA, M.C.; FOYER, C.H. Dorso
ventral variations in dark chilling effects on photosynthesis and stomatal function in
Paspalum dilatatum leaves. Journal of Experimental Botany, Oxford, v.62, p.687-699,
2010.
SOUZA, A.P. Mecanismos fotossintéticos e relação fonte-dreno em cana-de-açúcar
cultivada em atmosfera enriquecida em CO2. 208p. 2011. Tese (Doutorado em Ciências) -
Instituto de Biociências - Universidade de São Paulo - São Paulo.
STITT, M.; WILKE, I.; FEIL, R, H.; ELDT, H.W. Coarse control of sucrose-phosphate
synthase in leaves: alterations of the kinetic properties in response to the rate of
photosynthesis and the accumulation of sucrose. Planta, New York, v. 174:217–230, 1988.
STURM, A. TANG, G.Q. The sucrose-cleaving enzymes of plants are crucial for
development, growth and carbon partitioning. Trends in Plant Science, London, v. 4, p. 401-
407, 1999.
TAIZ, L.; ZEIGER, E. Fisiologia vegetal. 4 ed. Porto Alegre: Artmed. 2009. 819 p.
UNIÃO DA INDÚSTRIA DA CANA-DE-AÇÚCAR. (UNICA) Disponível em:
http://www.unicadata.com.br/historico-de-producao-e-moagem. Acesso em: 11 de junho de
2013.
VAN BEL, A.J.E. The phloem, a miracle of ingenuity. Plant, Cell and Environment,
Oxford, v. 26, p. 125-149, 2003.
VERMA, A.K.; UPADHYAY, S.K.; VERMA, P.C.; SOLOMON, S.; SINGH, S.B.
Functional analysis of sucrose phosphate synthase (SPS) and sucrose synthase (SS) in
sugarcane (Saccharum) cultivars. Plant Biology, Stuttgart, v. 13, p. 325-332, 2011.
VON CAEMMERER, S.; FURBANK, R.T. The C4 pathway: an efficient CO2 pump.
Photosynthesis Research, Dordrecht, v. 77, p. 191-207, 2003.
WARDLAW, I.F. The control of carbon partitioning in plants. New Phytologist, Oxford, v.
116, p. 341-381, 1990.
YANG, J.; ZHANG, J.; WANG, Z., ZHU, Q.; LIU, L. Water Deficit-Induced senescence and
its relationship to the remobilization of pre-stored carbon in wheat during grain filling.
Agronomy Journal, Madison, v. 93, p. 196-206, 2001.

18
YORDANOV, I.; VELIKOVA, V.; TSONEV, T. Plant responses to drought, acclimation, and
stress tolerance. Photosynthetica, Praga, v. 38, p. 171-186, 2000.
YUAN, J.S.; TILLER, K.H.; AL-AHMAD, H.; STEWART, N.R.; STEWART JUNIOR,
C.N. Plants to power: bioenergy to fuel the future. Trends in Plant Science, London, v.18, p.
421-429, 2008.

19
CAPÍTULO II

20
Baixa temperatura noturna e deficiência hídrica na fotossíntese de cana-de-açúcar
RESUMO
O objetivo deste trabalho foi avaliar as respostas fotossintéticas da cana-de-açúcar aos
efeitos simultâneos e isolados de temperatura noturna (TN) baixa e deficiência hídrica (DH).
Após 128 dias do plantio, as plantas da cultivar IACSP94-2094 foram submetidas aos
tratamentos: controle sem DH e TN de 20 °C (TN20); com DH e TN de 20 °C (DH/TN20); sem
DH e TN de 12 °C (TN12); e com DH e TN de 12 °C (DH/TN12) por cinco dias. Após o período
de tratamento as plantas foram irrigadas e retornaram a TN de 20 °C por mais quatro dias, para
recuperação. Houve decréscimos na assimilação de CO2 em todos os tratamentos. A
recuperação total da assimilação de CO2 foi observada apenas nas plantas do tratamento TN12.
A ocorrência simultânea da baixa temperatura noturna e da deficiência hídrica causou efeito
negativo na condutância estomática, na capacidade máxima da ribulose-1,5-bisfosfato
carboxilase e no transporte aparente de elétrons, fator de eficiência e eficiência operacional do
fotossistema II, causando limitações difusivas, bioquímicas e fotoquímicas da fotossíntese. A
ocorrência de baixa temperatura e déficit hídrico causa queda no teor de amido nas folhas,
favorecendo o aumento no teor de sacarose.
Palavras-chaves: Saccharum spp.; assimilação de CO2; PEPcase; resfriamento; Rubisco.

21
Low night temperature and water deficit on photosynthesis of sugarcane
ABSTRACT
The objective of this work was to evaluate the photosynthetic responses of sugarcane
to the isolate and simultaneous effects of low night temperature (TN) and water deficit (WD).
After 128 days of planting, plants of the cultivar IACSP94-2094 were subjected to the
following treatments: control, without WD and TN of 20 °C (TN20); with WD and TN of 20 °C
(DH/TN20); without WD and TN of 12 °C (TN12); and with WD and TN of 12 °C (DH/TN12).
After five days in each treatment, plants were irrigated and subjected to TN of 20 °C for four
days for recovering. There were decreases in leaf CO2 assimilation in all treatments. Total
recovery of CO2 assimilation was noticed only in plants of treatment TN12. The simultaneous
occurrence of low night temperature and water deficit caused a negative effect on stomatal
conductance, on the maximum capacity of ribulose-1,5-bisphosphate carboxylase and on
electron transport rate, efficiency factor and operational efficiency of photosystem II, causing
diffusive, biochemical and photochemical limitations of photosynthesis. The occurrence of
low temperature and water deficit causes a decrease in starch content in the leaves, favoring
an increase in sucrose content.
Keys-words: Saccharum spp.; CO2 assimilation; PEPcase; cooling; Rubisco.

22
1 INTRODUÇÃO
A cultura de cana-de-açúcar (Saccharum spp.) tem importância mundial como fonte de
alimento e de energia e o cultivo dessa espécie no Brasil aumentou em áreas marginais, onde
há variações anuais acentuadas de temperatura e da disponibilidade hídrica (ROLIM et al.,
2007). Episódios de baixa temperatura noturna ocorrem com certa frequência e causam danos
que podem afetar a produtividade das plantas (SALES et al., 2012; SOARES-CORDEIRO et
al., 2010). Nas regiões subtropicais, a ocorrência de baixas temperaturas noturnas é comum no
final do inverno, quando há deficiência hídrica no solo e dias com temperaturas relativamente
altas.
As plantas têm tolerância variável à baixa temperatura e em espécies tropicais
sensíveis ao resfriamento podem ocorrer danos mesmo em temperaturas bem acima da
temperatura de congelamento do tecido (KAKANI et al., 2008; SAGE, 2007). Folhas de
plantas expostas ao resfriamento mostram inibição da fotossíntese, translocação mais lenta de
carboidratos, menor respiração, inibição do metabolismo de proteínas, geração de espécies
reativas de oxigênio, crescimento lento e murcha foliar. Estas modificações são causadas por
disfunções em processos metabólicos promovidos por alterações das propriedades da
membrana, mudanças na estrutura de proteínas e nas interações entre macromoléculas, além
de inibição de reações enzimáticas (CARMO-SILVA et al., 2008; KAKANI et al., 2008;
SOARES-CORDEIRO et al., 2010; LIU et al., 2012). Em condições de baixa temperatura
noturna (5 a 12 °C), observaram-se decréscimos na fotossíntese em espécies C4 (milho e
gramíneas) devido tanto a fatores difusivos quanto metabólicos (KAKANI et al., 2008;
SOARES-CORDEIRO et al., 2010).
Além das condições térmicas, a deficiência hídrica do solo constitui um dos estresses
mais limitantes da produtividade vegetal. A deficiência hídrica tem impacto variável na
produtividade agrícola dependendo da fase fenológica em que ocorre (INMAN-BAMBER &
SMITH, 2005; MACHADO et al., 2009), havendo genótipos de cana-de-açúcar que mostram
diferentes capacidades de recuperação no crescimento após eventos de seca (LANDELL et
al., 2004; MACHADO et al., 2009). Sob deficiência hídrica, as plantas apresentam alterações
morfofisiológicas, tais como enrolamento e alteração do ângulo da folha, redução da área
foliar, da transpiração, da condutância estomática, da fotossíntese, da condutividade
hidráulica das raízes, modificação da atividade de enzimas do metabolismo de nitrogênio e de

23
carbono e mudanças nos teores de antioxidantes (GHANNOUM, 2009; LOPES et al., 2011;
MACHADO et al., 2009; RIBEIRO et al., 2013). A fotossíntese decresce inicialmente devido
ao fechamento dos estômatos e, com o agravamento da deficiência hídrica, também se
evidenciam limitações metabólicas (CARMO-SILVA et al., 2008; GHANNOUM et al., 2003;
GHANNOUM, 2009; LOPES et al., 2011).
Os estudos sobre os danos causados pela baixa temperatura noturna e deficiência
hídrica em espécies C3 são frequentes (ALLEN et al., 2000; BERTAMINI et al., 2005;
FLEXAS et al., 1999; MACHADO et al., 2010) porém, em espécies C4 como cana-de-açúcar,
são menos estudadas principalmente quando ocorrem simultaneamente (SALES et al., 2012).
O objetivo deste trabalho foi avaliar as respostas fotossintéticas e relações hídricas à
ocorrência de baixa temperatura noturna do ar e de restrição hídrica no solo, isoladamente ou
em conjunto, considerando os processos, bioquímicos, fotoquímicos e estomáticos em plantas
jovens de cana-de-açúcar.
2 MATERIAL E MÉTODOS
Em bandejas contendo substrato comercial (Carolina Soil®, Vera Cruz, RS) composto
de turfa de Sphagno, vermiculita expandida, calcário dolomítico, gesso agrícola e fertilizante
NPK (traços) foram plantados mini-toletes de cana-de-açúcar (Saccharum spp.) cv. IACSP94-
2094 (Figura 1A e B).
Aos 35 dias após o plantio (DAP), as mudas foram transplantadas para vasos plásticos
contendo 8,5 L de uma mistura de terra, areia e substrato comercial na proporção 1:1:1
(v/v/v). Foi plantada uma muda por vaso e conduzidos somente o colmo primário. As plantas
foram mantidas em casa de vegetação (Figura 1C) e receberam tanto irrigação diária quanto
aplicações de nutrientes. As aplicações dos nutrientes foram parceladas em três vezes,
totalizando, por vaso: 18,21 g de Ca(NO3)2; 5,31 g de fosfato monoamônico; 7,29 g de KCl;
2,12 g de MgSO4; 0,17 g de H3BO3; 0,20 g de MnSO4; 0,02 g de CuSO4; 0,02 g de
(NH4)6Mo7O24 x 4(H2O); 0,09 g de ZnSO4; e 0,212 mg de FeEDTA (6% Fe).
Aos 128 DAP (06/01/2011), as plantas foram submetidas aos seguintes tratamentos: 1)
testemunha, com temperatura noturna (TN) de 20 °C irrigada (TN20); 2) TN de 20 °C com
deficiência hídrica (TN20/DH); 3) TN de 12 °C irrigada (TN12) e 4) TN de 12 °C com
deficiência hídrica (TN12/DH).

24
B A
C
Para imposição da baixa temperatura noturna, as plantas foram transferidas para uma
câmara de crescimento (modelo PGR14, Conviron, Canadá) nas seguintes condições
ambientais: temperatura do ar 12±1 °C e umidade relativa de 65% e permaneceram nessa
condição durante 12 h (19:00 às 7:00h).
Figura 1 - Fotografias ilustrando (A) bandeja para germinação contendo substrato comercial
e mini-toletes de cana-de-açúcar, (B) detalhe do mini-tolete contendo a gema, e (C) visão
geral das plantas em casa de vegetação aos 56 dias após o plantio.
As plantas foram irrigadas diariamente, fazendo-se a reposição da água
evapotranspirada, que foi medida por pesagens diárias dos vasos. A deficiência hídrica foi
imposta pela suspensão da rega e o substrato foi mantido com 50% da capacidade máxima de
retenção de água, medida pela pesagem dos vasos. Ou seja, foi reposta somente a água
suficiente para manter ao substrato com 50% da capacidade de retenção total de água (SALES
et al., 2012). Os tratamentos foram impostos pelo período de cinco dias. Na sequência, as
plantas foram submetidas a um período de quatro dias de recuperação, quando os tratamentos
TN12 e TN12/DH retornaram à temperatura noturna de 20 °C e as plantas com DH foram
reidratadas. A reidratação do substrato foi realizada ao entardecer do 5º dia de tratamento, até
90% de capacidade máxima de retenção de água.

25
Durante o período experimental a temperatura do ar e a radiação solar foram
registradas continuamente pelo posto meteorológico, distante 300 m do experimento, do
Centro Experimental Central (CEC) do Instituto Agronômico (IAC), em Campinas-SP.
2.1 Variáveis medidas e calculadas
Assimilação de CO2 e fluorescência da clorofila a
Na primeira folha totalmente expandida e com a lígula aparente (folha +1), foram
realizadas simultaneamente as medidas de trocas gasosas e fluorescência da clorofila a, por
meio de um analisador de gases por infravermelho integrado com câmara de fluorescência,
modelo Li 6400-40F (Licor, Inc. Nebraska, EUA). Foram realizadas curvas de resposta da
assimilação de CO2 (A) e da fluorescência da clorofila a pela variação da concentração
intercelular de CO2 (Ci), nas condições de radiação fotossinteticamente ativa (Q) de 2000
μmol m-2
s-1
, temperatura foliar de 30 °C e déficit de pressão de vapor entre a folha e o ar ao
redor de 1,5 kPa. A variação de Ci foi obtida pela variação da concentração de CO2 do ar (Car)
de entrada da câmara de medida de acordo com LONG & BERNACCHI (2003). Essas curvas
foram realizadas no período entre 9:00 h e 12:00 h.
As variáveis analisadas em relação à fluorescência da clorofila a foram: fluorescência
mínima (Fo) e máxima (Fm), medidas após adaptação ao escuro; fluorescência no estado de
equilíbrio dinâmico (F') e máxima (Fm'), medidas após adaptação à luz (MAXWELL &
JOHNSON, 2000). A fluorescência variável máxima no escuro e à luz foram calculadas,
respectivamente, por Fv=Fm-Fo e Fv'=Fm'-Fo', onde Fo' representa a fluorescência mínima em
folhas adaptadas à luz. O termo Fq' foi calculado por Fq'=Fm'-F', representando a extinção
fotoquímica da fluorescência causada pelos centros oxidados do fotossistema II (FSII)
segundo BAKER (2008). Desta forma, calculou-se a eficiência quântica máxima (Fv/Fm) e a
eficiência operacional do FSII (Fq'/Fm'), o transporte aparente de elétrons (ETR=Fq'/Fm' x Q x
0,4 x 0,85) e o fator de eficiência do FSII (Fq'/Fv') de acordo com MAXWELL & JOHNSON
(2000) e BAKER (2008), respectivamente. Para o cálculo de ETR, considerou-se uma
distribuição de elétrons entre o FSI e FSII de 0,4 (EDWARDS et al., 1993) e a absorção de
luz 0,85. Calculou-se também a eficiência quântica da fotossíntese (CO2) pela relação
A/0,85Q, para cada valor de Ci.
A partir da curva A vs. Ci foram calculadas a eficiência aparente de carboxilação da
fosfoenolpiruvato carboxilase (PEPcase, Vpmax) e a capacidade máxima da ribulose-1,5-

26
bisfosfato carboxilase/oxigenase (Rubisco, Vmax) Os dois parâmetros bioquímicos foram
calculados à partir da solução analítica das equações propostas por COLLATZ et al. (1992):
θM² - M(Vmax + Q) + VmaxQ
Ag² - Ag (M + Vpmax /P) + M Vpmax /P = 0 (2)
onde significa a convexidade da curva A/Q, M a assimilação de CO2 no platô da curva A/Ci,
α significa a eficiência quântica aparente da curva A/Q, significa a convexidade da curva
A/Ci, Ag é a assimilação bruta de CO2, e P a pressão atmosférica. Ag foi calculada por Ag = A +
Rd, onde Rd é a respiração foliar.
Para estimar a convexidade , foi ajustada a curva A/Ci, pela equação proposta por
LIETH & REYNOLDS (1987), respectivamente:
A=(((*Ci+Amax+Rd)-((* Ci +Amax+Rd)²-(4** Ci **(Amax+Rd))0,5
)/(2*))-Rd (3)
onde Amax significa a assimilação de CO2 sob saturação de luz.
A convexidade θ relativa à curva A vs. Q, também foi estimada pela equação proposta
por LIETH & REYNOLDS (1987). As curvas de reposta de A em função da variação da luz
foram medidas aplicando-se 13 Q, de forma decrescente: 2300, 1900, 1500, 1100, 900, 700,
600, 500, 300, 200, 100, 50 e 0 mol m-2
s-1
. O tempo mínimo de equilíbrio para cada medida
em cada Q foi 180 segundos e o máximo 300 segundos, ou até que a medida apresentasse um
coeficiente de variação de 0,5 %. A concentração de CO2 e a DPVfolha-ar no ar foram de 400
mol CO2 mol-1
e 1,5 kPa, respectivamente.
Também a partir da curva A vs. Ci foram calculadas a assimilação de CO2 a 400 μmol
mol-1
no ar e a assimilação potencial de CO2 em concentração saturante de CO2 (Apot).
Estimou-se a limitação metabólica (LM) pela equação LM=[(A–A')/A]*100 conforme
LAWLOR (2002), onde A é a assimilação de CO2 das plantas controle, TN20 e A' a das plantas
sob estresse, ambas medidas em Ci de 400 μmol mol-1
. As curvas A vs. Ci foram realizadas no
1º, 2º e 4º dias após o início dos tratamentos e no 1º e 4º dias após a reidratação do solo, sob
condições naturais.
A variação diária da assimilação de CO2 foi avaliada no 3º e 5º dias após o início dos
tratamentos, considerando-se a variação natural das condições atmosféricas. Os valores de Q

27
foram medidos no início de cada horário de avaliação para ajustar a fonte de luz da câmara de
medida em Q constante homogeneizando assim as repetições. As medidas foram realizadas
entre 07:00 h e 17:00 h, em intervalos de três horas. Calculou-se a assimilação diária de CO2
(Ai) a partir da integração da assimilação instantânea de CO2 ao longo do dia.
Teor de carboidratos solúveis
No período de máximo estresse e recuperação, foram coletadas folhas +1 das plantas,
que foram imediatamente imersas em nitrogênio líquido e mantidas em freezer (-80 °C) até o
momento das análises. As folhas coletadas para análise do teor de carboidratos foram
submetidas à secagem em estufa com circulação forçada de ar à temperatura de 60 °C, por
quatro dias ou até massa constante.
Os extratos para análises de sacarose (SAC) e de açúcares solúveis totais (AST) foram
obtidos pelo método do MCW (metanol, clorofórmio e água) na proporção 12:5:3 (v/v),
descrito por BIELESK & TURNER (1966). Foram transferidos para um tubo de rosca
contendo 75 mg de amostra previamente macerada, 3 mL da solução de MCW e ficaram sob
refrigeração por 2 dias. Após a separação de fases obtida pela adição de 1,8 mL de
clorofórmio e 1,2 mL de água, coletou-se o sobrenadante que em seguida foi concentrado em
banho-maria (50 °C) para evaporação do metanol e resíduos de clorofórmio.
A determinação do teor de AST foi feita pelo método do fenol-sulfúrico (DUBOIS et
al.,1956). Em tubo de ensaio adicionaram-se 15 μL de extrato e 485 μL de água destilada,
500μL de solução de fenol 5% e 2 mL de ácido sulfúrico (H2SO4) concentrado. Após agitação
e resfriamento à temperatura ambiente, fez-se a leitura da absorbância em espectrofotômetro
(Genesys 10UV Scanning, Thermo Scientific) no comprimento de onda de 490 nm. A
concentração de AST foi calculada a partir de uma curva padrão de glicose (0,25 mg/mL) cuja
concentração variou entre 5 e 50 μg. Como branco, colocou-se água no lugar da amostra.
Determinou-se a concentração de SAC pelo método descrito por VAN HANDEL
(1968) e a dosagem pelo método do fenol-sulfúrico (DUBOIS et al.,1956). Em tubo de ensaio
adicionaram-se15 μL de extrato, 485 μL de água destilada e 500 μL de solução de hidróxido
de potássio (KOH) 30%. Os tubos foram vedados e levados ao banho-maria a 100 °C por 10
minutos. Em seguida, foram adicionados 500 μL de solução de fenol 5% e 2 mL de H2SO4
concentrado. Após agitação e resfriamento à temperatura ambiente, fez-se a leitura da
absorbância em espectrofotômetro no comprimento de onda de 490 nm. A concentração de

28
SAC foi calculada a partir de uma curva padrão de sacarose (0,25 mg/mL) cuja concentração
variou entre 5 e 50 μg. Como branco, colocou-se água no lugar da amostra.
Teor de amido
O extrato para quantificação de amido foliar foi obtido utilizando o método enzimático
descrito por AMARAL et al. (2007). Em microtubo contendo 10 mg de amostra realizou-se
uma extração prévia dos açúcares solúveis, pigmentos e fenóis adicionando-se 500 μL de
etanol 80%, levando em seguida ao banho-maria a 80 °C por 20 minutos e descartando em
seguida o sobrenadante. Este passo foi repetido quatro vezes. Após secagem do material
restante em temperatura ambiente até completa evaporação do etanol, foram adicionados 500
μL de uma solução contendo 120 U mL-1
da enzima α-amilase (EC 3.2.1.1) termoestável de
Bacillus licheniformis (Megazyme, Irlanda), diluída em tampão MOPS 10 mM e pH 6,5.
Essas amostras foram incubadas a 75 °C por 30 minutos. Este procedimento foi repetido mais
uma vez. Em seguida, adicionaram-se 500 μL de uma solução contendo 30 U mL-1
da enzima
amiloglucosidase (EC 3.2.1.3) de Aspergillus niger (Megazyme, Irlanda), diluída em tampão
acetato de sódio 100 mM e pH 4,5. Essas amostras foram incubadas a 50 °C por 30 minutos.
Este procedimento foi repetido mais uma vez. Foram acrescentados 100 μL de ácido
perclórico 0,8 M para parar a reação e precipitar as proteínas. O extrato foi centrifugado por
dois minutos a 10.000 g e procedeu-se a dosagem de amido. A glicose liberada foi dosada
adicionando-se em um microtubo 50 μL do extrato e 750 μL do reagente glicose GOD-PAP
(Laborlab, Brasil), incubados a 37 °C por 15 minutos. Fez-se a leitura da absorbância em
leitor de microplacas de ELISA (modelo EL307C, Bio- Tek Instruments, Winooski, Vermont)
no comprimento de onda de 490 nm. A concentração de glicose foi calculada a partir de uma
curva padrão de glicose (1 mg/mL) cuja concentração variou entre 2,5 e 30 µg de glicose.
Como branco, colocou-se água no lugar da amostra.
Potencial da água na folha
O potencial da água na folha (Ψw) foi medido em câmara psicrométrica (C-52, Wescor,
Logan, EUA) acoplada a um microvoltímetro (modelo HR-33T, Wescor, Logan, EUA) no
modo higrométrico às 6:00h e 14:00h (BOYER, 1995) em discos retirados da folha +2.
Delineamento experimental

29
O delineamento experimental foi inteiramente ao acaso com parcelas subdivididas no
tempo, sendo as causas de variação os quatro tratamentos (TN20; TN20/DH; TN12 e TN12/DH)
e o tempo de avaliação. Os resultados foram submetidos à análise de variância, sendo as
médias provenientes de três repetições para as medidas de fotossíntese e quatro para as
medidas de teor de carboidrato. Quando encontradas diferenças significativas, as médias
foram comparadas pelo teste de Tukey a 5% de probabilidade.
3 RESULTADOS E DISCUSSÃO
A figura 2 mostra a variação da radiação solar e da temperatura durante o período de
imposição dos tratamentos de baixa temperatura noturna e deficiência hídrica em cana-de-
açúcar, quando foram feitas as medidas de trocas gasosas e fluorescência da clorofila a.
Figura 2 - Variação da radiação solar (A) e da temperatura (B) durante o período
experimental. Setas indicam os dias de medidas de trocas gasosas e fluorescência da clorofila
a em cana-de-açúcar.
A imposição do frio noturno e da deficiência hídrica causou redução significativa na
assimilação diária de CO2 (Ai) a partir do 3o dia de tratamento, com reduções de 24%, 31% e
0
200
400
600
800
1000
Rad
iaçã
o s
ola
r (W
m-2
)
5 6 7 8 9 10 11 12 13 14 15
A
16
18
20
22
24
26
28
Tem
per
atura
(oC
)
B
Janeiro /2011

30
0
200
400
600
800 3
0 dia 5
0 dia A
Ai (
mm
ol
m-2
d-1
)
Tratamentos
TN20 DH/T
N20 TN12 DH/T
N12
42% nos tratamentos DH/TN20, TN12 e DH/TN12, respectivamente, em relação à testemunha
TN20 (Figura 3). No 5º dia de tratamento, Ai teve um decréscimo mais acentuado com 71%,
50% e 61% nos tratamentos DH/TN20, TN12 e DH/TN12, respectivamente, mostrando efeito
cumulativo conforme o tempo de estresse. Os menores valores observados, nas plantas
testemunha, em Ai no 5º dia em relação ao 3º dia foram devidos à menor incidência de
radiação solar (Figura 2A).
Figura 3 - Variação da assimilação diária de CO2 (Ai) de cana-de-açúcar, cv. IACSP94-2094
aos seguintes tratamentos: TN20, temperatura noturna de 20 °C - irrigada; DH/TN20,
temperatura noturna de 20 °C - não irrigada; TN12, temperatura noturna de 12 °C - irrigada e
DH/TN12, temperatura noturna de 12 °C - não irrigada. As colunas indicam média de três
repetições (± erro padrão).
Após o 2º dia, A nas plantas submetidas à deficiência hídrica (DH/TN20) e ao frio
noturno e deficiência hídrica (DH/TN12) continuou menor em relação a TN20, atingindo
valores menores que as plantas submetidas ao tratamento TN12 (Figura 4A). Após quatro dias
da reidratação do substrato e retorno da temperatura noturna a 20 °C, apenas as plantas TN12
apresentaram A semelhante à testemunha, persistindo o efeito do frio associado à deficiência
hídrica sobre A nas plantas DH/TN12 e DH/TN20 (Figura 4A).
O decréscimo da fotossíntese observada em plantas tanto em baixa temperatura
noturna quanto sob deficiência hídrica ou a combinação de ambos os estresses, pode ser
devido a fatores difusivos, metabólicos ou fotoquímicos (GHANNOUM et al., 2003;
GHANNOUM, 2009; MACHADO et al., 2009, 2010).
A queda em gs em plantas submetidas à baixa temperatura noturna (TN12 e DH/TN12)
ocorreu possivelmente devido à redução da condutância hidráulica ocasionada pelo

31
0 1 2 3 4 5 6 7 8 9
0,05
0,10
0,15
0,20
0,25
0 1 2 3 4 5 6 7 8 90
10
20
30
40
TN20 DH/T
N20 T
N12 DH/T
N12
Dias Dias
B
gs (m
ol m
-2 s-1)
A
A (
mol
m-2 s
-1)
decréscimo da permeabilidade do protoplasma (SELLIN & KUPPER, 2007), visto que não
houve variação do potencial da água na folha (ΨW14) nestes tratamentos (Figura 5A).
Figura 4 - A, Resposta da assimilação de CO2 (A) e B, condutância estomática (gs) em cana-
de-açúcar cv. IACSP94-2094. Tratamentos: TN20, temperatura noturna de 20 °C - irrigada
(■); DH/TN20, temperatura noturna de 20 °C - não irrigada (○); TN12, temperatura noturna de
12 °C - irrigada (∆) e DH/TN12, temperatura noturna de 12 °C - não irrigada (▼). Dados
retirados da curva A vs. Ci, sob saturação de luz e 400 μmol mol-1
de CO2. Período de
aplicação dos tratamentos, dias 1 a 5; período de recuperação com retorno da irrigação das
plantas e temperatura noturna de 20 °C, dias 5 a 9.
O fechamento estomático devido à redução da umidade do substrato está relacionado
com a diminuição do ΨW14 em DH/TN20 (Figura 5A), com a condutividade hídráulica e com o
transporte de sinais bioquímicos como o transporte e redistribuição do ácido abscísico devido
à alcalinização da seiva do xilema, desde as raízes até as folhas (GHANNOUM et al., 2009;
MACHADO et al., 2009; 2010).
Assim como observado para gs, a transpiração (E) foi menor nos tratamentos TN12,
DH/TN20 e DH/TN12 em relação à testemunha, após quatro dias dos tratamentos (Figura 5B).
Somente as plantas do tratamento DH/TN20 tiveram menor ΨW14 em relação à
testemunha (Figura 5A). Este resultado é intrigante, pois em relação às plantas DH/TN12, gs e
E foram semelhantes à DH/TN20 (Figuras 4B e 5B). No 4º dia de reidratação e retorno da
temperatura noturna a 20 °C, nas plantas DH/TN20 e DH/TN12 houve recuperação parcial de
gs e E (Figuras 4B e 5B). Somente TN12 recuperou totalmente gs e E após retorno da
temperatura noturna a 20 °C. As plantas do tratamento DH/TN20 recuperaram totalmente o
ΨW14 no 4º dia após a reidratação (Figura 5A).
A assimilação máxima de CO2 (Apot) dos tratamentos TN12, DH/TN20 e DH/TN12
foram menores que a testemunha (p<0,05) a partir do 1º dia. No 2º dia as plantas que foram

32
submetidas a TN12 e DH/TN12 apresentaram Apot menor que as DH/TN20, sugerindo efeito
mais intenso da baixa TN do que do DH no início do estresse.
Figura 5 - A, Variação de potencial da água na folha (W14) e B, transpiração (E) em cana-
de-açúcar cv. IACSP94-2094 submetida aos tratamentos: TN20, temperatura noturna de 20 °C
- irrigada; DH/TN20, temperatura noturna de 20 °C - não irrigada; TN12, temperatura noturna
de 12 °C - irrigada e DH/TN12, temperatura noturna de 12 °C - não irrigada. As colunas
indicam média de três repetições (± erro padrão). Período de aplicação dos tratamentos, dias 1
a 5; período de recuperação com retorno da irrigação das plantas e temperatura noturna de 20
°C, dias 5 a 9.
No 4º dia, Apot de DH/TN20 e DH/TN12 foram as menores, enquanto as plantas TN12
apresentaram aclimatação (Figura 6A). Apot é medida em condições de saturação de CO2 e,
portanto, desconsidera limitações difusivas. Assim, os valores inferiores em relação às plantas
TN20 indicam limitações metabólicas. Em DH/TN20 e DH/TN12 os valores de Apot foram
menores que os outros tratamentos no final do período de recuperação sugerindo que as
limitações metabólicas ainda persistiram nestes dois tratamentos, destacando DH/TN12 que foi
menor que DH/TN20. De fato, o decréscimo da fotossíntese foi associado ao aumento
significativo da limitação metabólica (LM) nas plantas que sofreram restrição hídrica
(DH/TN20 e DH/TN12) e que não apresentaram redução de LM após a reidratação do solo
(Figura 6B). Também neste caso a LM de DH/TN12 ficou maior que DH/TN20 na recuperação.
O ciclo fotossintético C4 da cana-de-açúcar caracteriza-se por adaptações celulares,
bioquímicas e fisiológicas. O CO2 atmosférico é inicialmente fixado pela fosfoenolpiruvato
carboxilase (PEPcase) em ácido C4 nas células do mesofilo. Os ácidos C4 são transportados
para as células da bainha do feixe vascular (BFV), onde são descarboxilados, e o CO2 liberado
entra no metabolismo C3 via ribulose-1,5-bisfosfato (RuBP) carboxilase/oxigenase (Rubisco)
confinada nas células da BFV. Este mecanismo concentra CO2 próximo à enzima Rubisco,
-1,0
-0,8
-0,6
-0,4
-0,2
0,01 4 9
W
14 (
MP
a)
A
1 4 90
1
2
3
4
5
6
7
E (m
mol m
-2 s-1)
TN20 DH/TN20
TN12 DH/TN12
B
Dias
Dias

33
-20
0
20
40
60
80
100
0 1 2 3 4 5 6 7 8 9
0,0
0,1
0,2
0,3
0,4
0 1 2 3 4 5 6 7 8 90
10
20
30
40
50
0
10
20
30
40
50
LM (%
)
B
Dias
Vp
ma
x (m
ol
m-2 s
-1)
Dias
C
Vm
ax (
mo
l m-2 s
-1)
D
TN20 DH/T
N20 T
N12 DH/T
N12
Ap
ot (
mo
l m
-2 s
-1)
A
permitindo sua maior atividade como carboxilase e consequente maior eficiência do uso de
água e de nitrogênio e ausência de fotorrespiração (SAGE, 2007). Desta forma, a LM da
fotossíntese pode estar relacionada a alterações na atividade enzimática da PEPcase e da
Rubisco, com a regeneração dos substratos das enzimas e transporte de elétrons (CARMO-
SILVA et al., 2008; GHANNOUM, 2009; RIPLEY et al., 2007; SOARES-CORDEIRO et al.,
2010). A eficiência aparente de carboxilação da PEPcase (Vpmax) foi menor, em relação a
testemunha, no 1º dia, em todos os tratamentos. No entanto, houve aclimatação das plantas no
início do período de recuperação, ou seja, os valores de Vpmax se igualaram aos verificados em
TN20 (Figura 6C). Alguns estudos também mostram a redução na atividade da PEPcase com a
diminuição do conteúdo de água no solo (DU et al., 1996; MARKELZ et al., 2011) e com a
baixa temperatura noturna (KAKANI et al., 2008; SOARES-CORDEIRO et al., 2010).
Figura 6 - A,Variação de assimilação máxima em CO2 saturante (Apot); B, limitação
metabólica (LM); C, eficiência de carboxilação da PEPcase (Vpmax) e D, eficiência máxima da
Rubisco (Vmax) em cana-de-açúcar cv. IACSP94-2094 submetida aos tratamentos: TN20,
temperatura noturna de 20 °C - irrigada (■); DH/TN20, temperatura noturna de 20 °C - não
irrigada (○); TN12, temperatura noturna de 12 °C - irrigada (∆) e DH/TN12, temperatura
noturna de 12 °C - não irrigada (▼). Os símbolos indicam média de três repetições (± erro
padrão). Período de aplicação dos tratamentos, dias 1 a 5; período de recuperação com retorno
da irrigação das plantas e temperatura noturna de 20 °C, dias 5 a 9.

34
A capacidade máxima da Rubisco (Vmax) in vivo foi menor que a testemunha em todos
os tratamentos no 1º dia, sendo mais acentuada em TN12 e DH/TN12 no 2º dia e DH/TN20 e
DH/TN12 no 4º dia de tratamento. Nas plantas do tratamento TN12 foi observada a aclimatação
de Vmax. Os valores de Vmax foram maiores que dos outros tratamentos e próximos a
testemunha no 4º dia de tratamento e semelhantes à testemunha no final do período de
recuperação (Figura 6D). As plantas DH/TN12 apresentaram recuperação parcial de Vmax ao
término do período de recuperação (Figura 6D).
As reduções de Vpmax e Vmax indicam limitações bioquímicas do metabolismo
fotossintético C4 da cana-de-açúcar em condições de baixa temperatura noturna e deficiência
hídrica. A atividade da Rubisco foi mais sensível aos tratamentos, em especial nas plantas
submetidas à deficiência hídrica (DH/TN20 e DH/TN12), mesmo após a reidratação quando
apresentavam LM ao redor de 25%, devido aos baixos valores de Vmax (Figura 6B, D). No 4º
dia de recuperação Vmax de DH/TN12 foi menor que DH/TN20 (Figura 6D).
Os tratamentos não causaram variações significativas na eficiência quântica máxima
do FSII (Fv/Fm), sugerindo que não houve fotoinibição da fotossíntese (Figura 7A). No
entanto, o transporte aparente de elétrons (ETR) e a eficiência operacional do FSII (Fq'/Fm')
foram menores no 1º dia dos tratamentos do que no controle (Figura 7B, C).
Apenas as plantas do tratamento DH/TN12 não recuperaram ETR e Fq'/Fm' após quatro
dias da reidratação. O decréscimo de Fq'/Fm' indica diminuição significativa da dissipação da
energia dos elétrons na etapa fotoquímica, também confirmada pela redução do fator de
eficiência do FSII (Fq'/Fv') (Figura 7D), implicando aumento na dissipação não fotoquímica
de fluorescência (RIPLEY et al., 2007). Assim, a redução de Fq'/Fm' pode estar relacionada ao
fechamento (redução) dos centros de reação do FSII sob condição de baixa temperatura e
deficiência hídrica (BAKER, 2008), refletindo em acúmulo de QA em estado reduzido,
indicado pela diminuição de Fq'/Fv', devido à significativa redução da assimilação de CO2 em
DH/TN20, TN12 e DH/TN12.
A diminuição de gs causa menor fluxo de CO2 para o mesofilo foliar podendo causar
redução na concentração de CO2 junto à Rubisco e assim estimular a atividade da oxigenase,
ou seja, a fotorrespiração (CARMO-SILVA et al., 2008). De fato, no nosso experimento
houve queda de Ci somente em DH/TN20 e no 4º dia de estresse (Ci =115±25 μmol mol-1
em
DH e Ci =176±19 μmol mol-1
nos demais tratamentos).

35
0 1 2 3 4 5 6 7 8 9
30
60
90
120
150
0,05
0,10
0,15
0,20
0,25
0,65
0,70
0,75
0,80
0 1 2 3 4 5 6 7 8 90,1
0,2
0,3
0,4
Dias Dias
ET
R (
mol
m-2 s
-1) C
Fq '/F
m '
B
TN20 DH/T
N20 T
N12 DH/T
N12
A
Fv/F
m
Fq '/F
v '
D
Figura 7 - A, Resposta de eficiência quântica máxima do fotossistema II (Fv/Fm); B,
eficiência operacional do FSII (Fq'/Fm'); C, transporte aparente de elétrons (ETR) e D, fator de
eficiência do FSII (Fq'/Fv') em cana-de-açúcar cv. IACSP94-2094 submetida aos tratamentos:
TN20, temperatura noturna de 20 °C - irrigada (■); DH/TN20, temperatura noturna de 20 °C -
não irrigada (○); TN12, temperatura noturna de 12 °C - irrigada (∆) e DH/TN12, temperatura
noturna de 12 °C - não irrigada (▼). Os símbolos indicam média de três repetições (± erro
padrão). Período de aplicação dos tratamentos, dias 1 a 5; período de recuperação com retorno
da irrigação das plantas e temperatura noturna de 20 °C, dias 5 a 9.
A relação entre a eficiência quântica CO2 e Fq'/Fm' não foi modificada pelos
tratamentos (Figura 8), sugerindo que não houve aumento na atividade de drenos alternativos
de elétrons, como fotorrespiração e reação de Mehler (GHANNOUM, 2009), e sim
decréscimo no uso da energia em reações fotoquímicas da fotossíntese. Este resultado sugere
que, apesar de ter ocorrido menor fluxo de CO2 devido à diminuição de gs, o mecanismo de
concentração de CO2 da cana-de-açúcar nos tratamentos avaliados é efetivo em limitar a
fotorrespiração (CARMO-SILVA et al., 2008).
O carboidrato gerado pela fotossíntese é a fonte de energia e substrato para o
crescimento e manutenção da fitomassa. Com relação aos carboidratos, os teores de açúcares
solúveis totais (AST) não foram alterados até o 5º dia de tratamento (Tabela 1), porém ocorreu
queda no 4º dia da recuperação em DH/TN20 e TN12, sugerindo efeito da seca e da baixa
temperatura, respectivamente.

36
0,00 0,05 0,10 0,15 0,20 0,250,00 0,05 0,10 0,15 0,20 0,25
0,00
0,01
0,02
0,03
C
O2 [
(m
ol
CO
2
mo
l fó
ton
s)-1
]
TN20 DH/T
N20 T
N12 DH/TN12
Fq'/F
m'
Figura 8 - Relação entre eficiência quântica de CO2 (CO2) e eficiência operacional do
fotossistema II (Fq’/Fm’) em cana-de-açúcar cv. IACSP94-2094 submetida aos tratamentos:
TN20 (), temperatura noturna de 20 °C - irrigada; DH/TN20 (), temperatura noturna de
20 °C - não irrigada; TN12 (), temperatura noturna de 12 °C - irrigada e DH/TN12 (),
temperatura noturna de 12 °C - não irrigada, um (símbolos cheios e linha, CO2=-
0,003+0,132*Fq´/Fm´, R2=0,93, p<0,01) e quatro dias após os tratamentos (símbolos vazios e
linha tracejada, CO2=-0,005+0,136*Fq´/Fm´, R2=0,87, p<0,01).
No 5º dia de estresse, o teor de sacarose (Tabela 2) aumentou em função da deficiência
hídrica somente a 20 °C (DH/TN20) e da baixa temperatura noturna (média de TN12).
Tabela 1 - Teor de açúcares solúveis totais (μmol g-1
MS) em folhas de cana-de-açúcar cv.
IACSP94-2094 submetida aos tratamentos: TN20, temperatura noturna de 20 °C - irrigada;
DH/TN20, temperatura noturna de 20 °C - não irrigada; TN12, temperatura noturna de 12 °C -
irrigada e DH/TN12, temperatura noturna de 12 °C - não irrigada, no 5º dia de tratamento e 4º
dia de recuperação. Período de aplicação dos tratamentos, dias 1 a 5; período de recuperação
com retorno da irrigação das plantas e temperatura noturna de 20 °C, dias 5 a 9.
5º dia de tratamento 4º dia de recuperação
TN20 296,43 ± 92,59 Aa* 251,19 ± 35,83 Aa
DH/TN20 391,92 ± 38,82 Aa 270,84 ± 34,24 Ab
Média 344,18 ± 83,22 Aa 261,02 ± 34,11 Ab
TN12 382,02 ± 41,7 Aa 209,83 ± 48,85 Bb
DH/TN12 296,32 ± 74,27 Aa 366,45 ± 70,51 Aa
Média 339,18 ± 72,16 Aa 288,15 ± 100,80 Aa
*Letras maiúsculas diferentes na coluna indicam diferença significativa ao nível de 5% pelo teste de
Tukey entre irrigações na mesma temperatura e médias. Letras minúsculas diferentes na linha indicam
diferença significativa entre 5º dia de tratamento e o 4º dia de recuperação, ao nível de 5% pelo teste
de Tukey

37
Os teores de SAC no 5º dia de tratamento aumentaram com a deficiência hídrica e com
a baixa temperatura noturna, sendo que este aumento foi maior nos tratamentos com baixa
temperatura noturna (Tabela 2).
No 4º dia de recuperação, somente os tratamentos com baixa temperatura noturna
apresentaram decréscimo de SAC (TN12 e DH/TN12) atingindo valores próximos aos do
controle (TN20, Tabela 2).
Tabela 2 - Teor de sacarose (μmol g-1
MS) em folhas de cana-de-açúcar cv. IACSP94-2094
submetida aos tratamentos: TN20, temperatura noturna de 20 °C - irrigada; DH/TN20,
temperatura noturna de 20 °C - não irrigada; TN12, temperatura noturna de 12 °C - irrigada e
DH/TN12, temperatura noturna de 12 °C - não irrigada, no 5º dia de tratamento e 4º dia de
recuperação. Período de aplicação dos tratamentos, dias 1 a 5; período de recuperação com
retorno da irrigação das plantas e temperatura noturna de 20 °C, dias 5 a 9.
5º dia de tratamento 4º dia de recuperação
TN20 36,37 ± 13,60 Ba* 56,46 ± 16,55 Aa
DH/TN20 74,13 ± 24,25 Aa 78,20 ± 13,45 Aa
Média 55,25 ± 27,18 Ba 67,33 ± 18,17 Aa
TN12 102,99 ± 30,08 Aa 59,12 ± 18,55 Ab
DH/TN12 107,69 ± 39,28 Aa 63,42 ± 24,64 Ab
Média 105,35 ± 32,49 Aa 61,27 ± 20,32 Ab
*Letras maiúsculas diferentes na coluna indicam diferença significativa ao nível de 5% pelo teste de
Tukey, entre irrigações na mesma temperatura e médias. Letras minúsculas diferentes na linha indicam
diferença significativa entre 5º dia de tratamento e o 4º dia de recuperação, ao nível de 5% pelo teste
de Tukey.
No estresse máximo, foi observado decréscimo na concentração de amido (AMI) no
tratamento DH/TN20, em função do déficit hídrico (Tabela 3). Esse decréscimo em plantas sob
estresse por temperatura e deficiência hídrica, possivelmente foi devido a dois principais
fatores: queda em A e Ai (Figuras 3 e 4) e aumento na hidrólise do AMI, permitindo assim a
manutenção do suprimento de carbono em condições de reduzida fixação de CO2 (SALES et
al., 2012). Por outro lado, o aumento do teor de SAC deve estar relacionado com o aumento da
hidrólise de AMI, além do possível aumento na atividade da sintase de sacarose fosfato (DU et
al., 1999, 2000; FU et al., 2010; VANDOORNE et al., 2012).

38
Tabela 3 - Teor de amido (μmol de Glu g-1
MS) em folhas de cana-de-açúcar cv. IACSP94-
2094 submetida aos tratamentos: TN20, temperatura noturna de 20 °C - irrigada; DH/TN20,
temperatura noturna de 20 °C - não irrigada; TN12, temperatura noturna de 12 °C - irrigada e
DH/TN12, temperatura noturna de 12 °C - não irrigada. No 5º dia de tratamento e 4º dia de
recuperação. Período de aplicação dos tratamentos, dias 1 a 5; período de recuperação com
retorno da irrigação das plantas e temperatura noturna de 20 °C, dias 5 a 9.
5º dia de tratamento 4º dia de recuperação
TN20 208,97 ± 66,92 Aa* 32,68 ± 9,02 Bb
DH/TN20 134,34 ± 82,89 Ba 55,61 ± 6,91 Ab
Média 171,65 ± 80,34 Aa 44,14 ± 14,34 Aa
TN12 140,28 ± 30,70 Aa 94,51 ± 29,27 Aa
DH/TN12 80,05 ± 48,92 Ab 162,47 ± 38,77 Aa
Média 110,17 ± 49,66 Aa 128,49 ± 48,28 Aa
*Letras maiúsculas diferentes na coluna indicam diferença significativa ao nível de 5% pelo teste de
Tukey entre irrigações na mesma temperatura e médias. Letras minúsculas diferentes na linha indicam
diferença significativa entre 5º dia de tratamento e o 4º dia de recuperação, ao nível de 5% pelo teste
de Tukey.
A deficiência hídrica e baixa temperatura noturna afetaram a fotossíntese devido a
fatores relacionados com a abertura dos estômatos e queda na atividade de Rubisco e PEPcase
(Figura 6C e D), sendo esperado que ocorresse diminuição da síntese de açúcar, no entanto,
paradoxalmente aumentou o teor de sacarose. Possivelmente o aumento da síntese de sacarose
seja devido ao estímulo da sintase de sacarose fosfato (FU et al. 2010; VANDOORNE et al.,
2012).
4 CONCLUSÕES
1. Na cultivar IACSP94-2094 a assimilação diurna de CO2 decresce em função da baixa
temperatura noturna e da deficiência hídrica, sendo associada à diminuição da condutância
estomática (fator difusivo), redução na atividade da PEPcase e da Rubisco (fatores
bioquímicos) e à menor atividade fotoquímica.
2. A ocorrência simultânea de baixa temperatura noturna e deficiência hídrica em plantas
jovens de cana-de-açúcar interferem na recuperação fotossintética das plantas.
3. A ocorrência de baixa temperatura e deficiência hídrica causa queda no teor de AMI
favorecendo o aumento no teor de SAC nas folhas.

39
5 REFERÊNCIAS BIBLIOGRÁFICAS
ALLEN, D.J.; RATNER, K.; GILLER, Y.E.; GUSSAKOVSKY, E.E.; SHAHAK, Y.; ORT,
D.R. An overnight chill induces a delayed inhibition of photosynthesis at midday in mango
(Manguifera indica L.). Journal of Experimental Botany, Oxford, v. 51, p.1893-1902, 2000.
AMARAL, L.I.V.; GASPAR, M.; COSTA, P.M.F.; AIDAR, M.P.M.; BUCKERIDGE, M.S.
Novo método enzimático rápido e sensível de extração e dosagem de amido em materiais
vegetais. Hoehnea, São Paulo, v. 34, p. 425-431, 2007.
BAKER, N.R. A probe of photosynthesis: in vivo. Annual Review of Plant Biology, Palo
Alto, v. 59, p.89–113, 2008.
BERTAMINI, K. MTHUCHELIAN, K.; RUBINIGG, M. ZORER, R. NEDUNCHEZHIAN,
N. Low-night temperature (LNT) induce changes of photosynthesis in grapevine (Vitis
vinifera L.) plants. Plant Physiology and Biochemistry, Paris, v. 43, p. 693-699, 2005.
BIELESKI, R.L.; TURNER, A. Separation and estimation of amino acids in crude plant
extracts by thin-layer electrophoresis and chromatography. Analytical biochemistry,
Amsterdam, v. 17, p. 278-293, 1966.
BOYER, J.S. Measuring the water status of plants and soils. San Diego, Academic Press,
1995, 178p.
CARMO-SILVA, A.E.; POWERS, S.J.; KEYS, A.J.; ARRABAÇA, M.C. Photorespiration in
C4 grasses remains slow under drought conditions. Plant, Cell and Environment, Oxford,
v.31, p.925-940, 2008.
COLLATZ, G.J.; RIBAS-CARBO, M.; BERRY, J.A. Coupled photosynthesis-stomatal
conductance model for leaves of C4 plants. Australian Journal of Plant Physiology,
Victoria, v.19, p.519-538, 1992.
DU, Y.C.; KAWAMITSU, Y.; NOSE, A. ; HIYANE, S.; MURAYAMA, S.; WASANO, K.;
UCHIDA, Y. Effects of water stress on carbon exchange rate and activities of photosynthetic
enzymes in leaves of sugarcane (Saccharum sp.). Functional Plant Biology, Victoria, v.23,
p.719-726, 1996.
DU, Y.C.; NOSE, A.; WASANO, K. Thermal characteristics of C4 photosynthetic enzymes
from leaves of three sugarcane species differing in cold sensitivity. Plant & Cell Physiology,
Oxford, v. 40, p. 298-304, 1999.
DU, Y.C.; NOSE, A.; KONDO, A.; WASANO, K. Diurnal changes in photosynthesis in
sugarcane leaves - II. Enzyme activities and metabolite levels relating to sucrose and starch
metabolism. Plant Production Science, Tóquio, v. 3, p. 9-16, 2000.
DUBOIS, M.; GILLES, K.A.; HAMILTON, J.K.; REBERS, P.A.; SMITH, F. Colorimetric
method for determination of sugars and related substances. Analytical Chemistry,
Washington, v. 28, n.30, p. 350-356, 1956.

40
EDWARDS, G.E.; BAKER, N.R. Can CO2 assimilation in maize leaves be predicted
accurately from chlorophyll fluorescence analysis? Photosynthesis Research, Dordrecht, v.
37, p. 89-102, 1993.
FLEXAS, J.; BADGER, M.; CHOW, W.S.; MEDRANO, H.; OSMOND, C.B. Analysis of
the relative increase in photosynthetic O2 uptake when photosynthesis in grapevine leaves is
inhibited following low night temperatures and/or water stress. Plant Physiology, Rockville,
v.121, p.675-684, 1999.
FROMMER, W.B.; SONNEWALD, U. Molecular analysis of carbon partitioning in
solanaceous species. Journal of Experimental Botany v.46, p.587-607, 1995.
FU, J.; HUANG, B.; FRY, J. Osmotic potencial, sucrose level, and activity of sucrose
metabolic enzymes in tall fescue in response to deficit irrigation. Journal of the American
Society for Horticultural Science, Alexandria, v. 135, p. 506-510, 2010.
GHANNOUM, O.; CONROY, J.P.; DRISCOLL, S.P.; PAUL, M.J.; FOYER, C.H.;
LAWLOR, D.W. Nonstomatal limitations are responsible for drought-induced photosynthetic
inhibition in four C4 grasses. New Phytologist, Oxford, v.159, p.599-608, 2003.
GHANNOUM, O. C4 photosynthesis and water stress. Annals of Botany, Oxford, v.103,
p.635-644, 2009.
INMAN-BAMBER, N.G.; SMITH, D.M. Water relations in sugarcane and response to water
deficits. Field Crops Research, Amsterdam, v.92, p.185-202, 2005.
KAKANI, V.G.; SURABHI, G.K.; REDDY, K.R. Photosynthesis and fluorescence responses
of C4 plant Andropogon gerardii acclimated to temperature and carbon dioxide.
Photosynthetica, Praga, v.46, p.420-430, 2008.
LANDELL, M.G.A.; CAMPANA, M.P.; FIGUEIREDO, P.; VASCONCELOS, A.C.M;
XAVIER, M.A.; BIDOIA, M.A.P.; PRADO, H.; SILVA, M.A.; DINARDO-MIRANDA,
L.L.; SANTOS, A.S.; PERECIN, D.; ROSSETTO, R.; SILVA, D.N.; MARTINS, A.L.M;
GALLO, P.B.; KANTACK, R.A.D.; AZANIA, C.A.A.M.; PINTO, L.R.; SOUZA, S.A.C.D.
Variedades de cana-de-açúcar para o Centro-Sul do Brasil. Campinas: IAC, 2004. 32p.
(Boletim técnico IAC 195 – 14ª Liberação do Programa Cana IAC).
LAWLOR, D.W. Limitation to photosynthesis in water-stressed leaves: stomata vs.
metabolism and the role of ATP. Annals of Botany, Oxford, v.89, p.871-885, 2002.
LIETH, J.H., REYNOLDS, J.F. The nonrectangular hyperbola as a photosynthetic light
response model: geometrical interpretation and estimation of the parameter ʘ.
Photosynthetica, Praga, v. 21, p. 363-366, 1987.
LIU, Y.F.; QI, M.F.; LI, T.L. Photosynthesis, photoinhibition, and antioxidant system in
tomato leaves stressed by low night temperature and their subsequent recovery. Plant
Science, London, v.196, p.8-17, 2012.

41
LONG, S.P., BERNACCHI, C.J. Gas exchange measurements, what can they tell us about the
underlying limitations to photosynthesis? Procedures and sources of error. Journal of
Experimental Botany. Oxford, v.54, p.2393-2401, 2003.
LOPES, M.S., ARAUS, J.L.; VAN HEERDEN, P.D.R.; FOYER, C.H. Enhancing drought
tolerance in C4 crops. Journal of Experimental Botany, Oxford, v.62, p.3135-3153, 2011.
MACHADO, R.S.; RIBEIRO, R.V.; MARCHIORI, P.E.R.; MACHADO, D.F.S.P.;
MACHADO, E.C. Respostas biométricas e fisiológicas ao déficit hídrico em cana-de-açúcar
em diferentes fases fenológicas. Pesquisa Agropecuária Brasileira, Brasília, v.44, p.1575-
1582, 2009.
MACHADO, D.F.S.P.; MACHADO, E.C.; MACHADO, R.S.; RIBEIRO, R.V. Efeito da
baixa temperatura noturna e do porta-enxerto na variação diurna das trocas gasosas e na
atividade fotoquímica de laranjeira 'Valência'. Revista Brasileira de Fruticultura,
Jaboticabal, v.32, p.351-359, 2010.
MARKELZ, R.J.C.; STRELLNER, R.S.; LEAKEY, A.D.B. Impairment of C4 photosynthesis
by drought is exacerbated by limiting nitrogen and ameliorated by elevated [CO2] in maize.
Journal of Experimental Botany, Oxford, v.62, p. 3235-3246, 2011.
MAXWELL, K.; JOHNSON, G.N. Chlorophyll fluorescence - a practical guide. Journal of
Experimental Botany, Oxford, v.51, p.659-668, 2000.
RIBEIRO, R.V.; MACHADO, R.S.; MACHADO, E.C.; MACHADO, D.F.S.P.;
MAGALHÃES FILHO, J.R.; LANDELL, M.G.A. Revealing drought-resistance and
productive patterns in sugarcane genotypes by evaluating both physiological responses and
stalk yield. Experimental Agriculture, Cambridge, v.49, p. 212-224, 2013.
RIPLEY, B.S.; GILBERT, M.E.; IBRAIM, D.G.; OSBONE, C.P. Drought constraints on C4
photosynthesis: stomatal and metabolic limitations in C3 and C4 subspecies of Alloteropsis
semialata. Journal of Experimental Botany. Oxford, v.58, p.1351-1363, 2007.
ROLIM, G.S.; CAMARGO, M.B.P.; LANIA, D.G.; MORAES, J.F.L. Classificação climática
de Köppen e de Thornthwaite e sua aplicabilidade na determinação de zonas agroclimáticas
para o Estado de São Paulo. Bragantia, Campinas, v.66, p.711-720, 2007.
SAGE, R.F. The temperature response of C3 and C4 photosynthesis. Plant, Cell and
Environment, Oxford, v.30, p.1086-1106, 2007.
SALES, C.R.G.; RIBEIRO, R.V.; MACHADO, D.F.S.P.; MACHADO, R.S.; DOVIS, V.L.;
LAGÔA, A.M.M.A. Trocas gasosas e balanço de carboidratos em plantas de cana-de-açúcar
sob condições de estresses radiculares. Bragantia, Campinas, v.71, p.319-327, 2012.
SELLIN, A.; KUPPER, P. Temperature, light and leaf hydraulic conductance of little- leaf
linden (Tilia cordata) in a mixed forest canopy. Tree Physiology, Victoria, v. 27, p. 679-688,
2007.
SOARES-CORDEIRO, A.S.; DRISCOLL, S.P.; ARRABAÇA, M.C.; FOYER, C.H.
Dorsoventral variations in dark chilling effects on photosynthesis and stomatal function in

42
Paspalum dilatatum leaves. Journal of Experimental Botany, Oxford, v.62, p.687-699,
2010.
VANDOORNE, B.; MATHIEU, A.S.; VAN DER ENDE, W.; VERGAUWEN, R.;
PÉRILLEUX, C.; JAVAUX, M.; LUTTS, S.Water stress drastically reduces root growth and
inulin yield in Cichorium intybus (var. sativum) independently of photosynthesis. Journal of
Experimental Botany, Oxford, v.63, p.4359–4373, 2012.
VAN HANDEL, E. Direct microdetermination of sucrose. Analytical Biochemistry,
Amsterdam, v. 22, p. 280-283, 1968.
VON CAEMMERER S. Biochemical models of leaf photosynthesis. CSIRO Publishing,
Melbourne, Australia, 2000. 165p.

43
CAPÍTULO III

44
Metabolismo de carboidratos em duas cultivares de cana-de-açúcar sob baixa
temperatura e deficiência hídrica
RESUMO
Para sobreviver às condições adversas, as plantas exibem uma série de respostas aos estresses
ambientais, que frequentemente, ocorrem de forma simultânea. Tais respostas também estão
relacionadas com diferentes tolerâncias ou sensibilidades aos diversos tipos de estresses. O
objetivo deste trabalho é testar a hipótese de que cultivares de cana-de-açúcar mais tolerantes
à deficiência hídrica e/ou baixa temperatura apresentam a fotossíntese e o metabolismo de
carboidratos menos suscetível a estes fatores ambientais. Para tanto, foram utilizadas as
cultivares de cana-de-açúcar IACSP94-2094 e IACSP95-5000 plantadas em potes plásticos de
8,5 L. Aos 87 dias após o plantio, foram submetidas aos tratamentos de baixa temperatura
(22±1/12±1 °C) e deficiência hídrica, por 22 dias, em câmara de crescimento. Após este
período, as plantas foram reidratadas e a temperatura retornou a 32±1/20±1 °C, por 9 dias.
Sob condições ambientais ideais, a IACSP95-5000 tem maior eficiência fotossintética que a
IACSP94-2094. A IACSP95-5000 mostrou ser mais tolerante ao frio, devido a menor redução
da assimilação de CO2 e maior recuperação, superando as plantas controle. Sob frio e
deficiência hídrica, a IACSP94-2094 é mais tolerante por não ter apresentado decréscimo
maior da fotossíntese nos estresses simultâneos. Com a imposição dos tratamentos, foi
observado aumento no teor de açúcares solúveis e amido em ambas cultivares. Na cultivar
IACSP94-2094 sob baixa temperatura e deficiência hídrica o aumento dos açúcares solúveis
totais foi devido ao aumento da sacarose, quando há também aumento da atividade da sintase
de sacarose fosfato.
Palavras-Chave: Saccharum spp., estresses ambientais, trocas gasosas, sintase de sacarose
fosfato, invertases

45
Carbohydrate metabolism in two cultivars of sugarcane under low temperature and
water deficit
ABSTRACT
To survive under adverse environmental conditions, plants show some responses to
environmental stress that often act simultaneously. These responses are also related to
different tolerances or sensitivities to various types of stress. The aim of this study is to test
the hypothesis that sugarcane cultivars more tolerant to water deficit and/or low temperature
have photosynthesis and carbohydrate metabolism less susceptible to these environmental
factors. We used two sugarcane cultivars, IACSP94-2094 and IACSP95-5000 and planted in
plastic pots of 8.5 L. At 87 days after planting, plants were treated with low temperature
(22±1/12±1 °C) and water deficit for 22 days in a growth chamber. After this period, the
plants were rehydrated and the temperature returned to 32±1/20±1 °C for 9 days. Under ideal
environmental conditions IACSP95-5000 has a higher photosynthetic capacity than
IACSP94-2094 cultivar. The IACSP95-5000 cultivar was more tolerant to chilling, due to
lower reduction in CO2 assimilation and greater recovery, overcoming the control plants.
Under low temperature and water deficit, the IACSP94-2094 cultivar was more tolerant for
not having higher decrease of photosynthesis in combined stresses. After treatments, we
observed an increase in soluble sugars and starch in both cultivars. Soluble sugars increase on
IACSP94-2094 cultivar under low temperature and water deficit, was due to sucrose increase,
when there is an activity increase of sucrose phosphate synthase.
Key Words: Saccharum spp., environmental stress, gas exchanges, sucrose phosphate
synthase, invertases

46
1 INTRODUÇÃO
Os carboidratos gerados pela fotossíntese constituem a fonte de energia para produção
e manutenção da biomassa (VANDOORME et al., 2012). Em plantas superiores, a sacarose
além de principal produto da fotossíntese, é uma molécula de transporte para o crescimento,
desenvolvimento, armazenamento, transdução de sinais e aclimatação a estresses ambientais
(SALERNO & CURATTI, 2003).
O acúmulo de sacarose varia de acordo com o genótipo e estádio de desenvolvimento
da planta e do ambiente em que é cultivada. A planta responde ao ambiente através da
transdução de sinais que coordenam o desenvolvimento, além do acúmulo de sacarose (GROF
& CAMPBELL, 2001; MOORE, 2005).
Em plantas C3 a síntese de sacarose pode ser controlada pela regulação da frutose-1,6-
bisfosfatase e sintase de sacarose fosfato (SPS) dependendo da disponibilidade de substrato,
pela regulação alostérica e, em algumas espécies, pela fosforilação proteica (LUNN &
FURBANK, 1999). Esses mecanismos de regulação permitem que a síntese de sacarose seja
coordenada pela fotossíntese e pelas exigências de exportação ou armazenamento temporário
de carboidratos na folha. Entretanto, esse controle é mais complexo em plantas C4, devido à
presença de dois tipos de células fotossintéticas. Assim, os processos de fixação de carbono e
a síntese do produto final são coordenados não só entre cloroplasto e citosol, mas também
entre mesofilo e as células da bainha do feixe vascular (BFV) (LUNN & FURBANK, 1999).
Assim como a síntese de sacarose, a sua quebra é vital para as plantas, não só pela
alocação de carbono, mas também como iniciador de sinais por hexoses, mantendo um
equilíbrio entre ambos. Diferentes mecanismos são ativados por hexoses e outros metabólitos,
além da própria sacarose. Apenas as invertases e a reação reversível da sintase de sacarose
(SuSy) catalisam esta quebra in vivo da sacarose em tecidos vegetais. Entretanto, as invertases
produzem glicose e frutose livres em vez de UDP-glicose e frutose, gerando duas vezes mais
hexoses que a quebra da sacarose pela SuSy (KOCH, 2004).
No campo, as plantas estão expostas a diversos estresses ambientais (YORDANOV et
al., 2000), como temperaturas extremas, deficiência hídrica e salinidade. Frequentemente,
alguns estresses agem de forma simultânea, como a combinação de baixa temperatura e
deficiência hídrica, fatores comuns no inverno, que afetam a fisiologia da cana-de-açúcar.
Entretanto, para sobreviver às condições adversas, as plantas exibem uma série de respostas

47
ao estresse. Tais respostas também estão relacionadas com diferentes tolerâncias ou
sensibilidades aos diversos tipos de estresses.
O metabolismo de carboidratos responde de maneira diferente à baixa temperatura e à
deficiência hídrica, dependendo da espécie e exposição ao estresse (DU et al. 1998, DU &
NOSE, 2002). Em cana-de-açúcar são poucos os trabalhos que relatam estas respostas,
principalmente quando a exposição a estas condições ocorrem de forma simultânea (SALES
et al., 2012).
Em plantas submetidas ao resfriamento, há acúmulo dos principais açúcares como
glicose, frutose e sacarose. Além disso, a atividade da SPS foliar aumenta enquanto a da SuSy
e das invertases não (GUY et al., 1992). Sob baixa temperatura, a sacarose acumulada como
carboidrato de reserva pode ser rapidamente mobilizada conforme as necessidades
metabólicas. Dessa forma, a sacarose é rapidamente translocada para ser utilizada após o
retorno a temperaturas favoráveis, em reações como, por exemplo, a respiração. Além disso,
sob baixa temperatura o crescimento ativo é quase sempre reduzido ou paralisado (GUY et
al., 1992; JAVIER et al., 1997; SALES et al., 2012), resultando em diminuição da demanda
por produtos da fotossíntese podendo, mesmo sob estresse, acumular reservas na forma de
amido.
DU & NOSE (2002) observaram que em cultivares de cana-de-açúcar com três meses
de idade, tolerantes à baixa temperatura, após 52 h de exposição ao frio houve acúmulo de
açúcares solúveis (glicose, frutose e sacarose), semelhante ao que ocorre em plantas C3
tolerantes. Além disso, o conteúdo de amido se manteve alto durante todo o tratamento. Após
exposição ao frio, nestas cultivares tolerantes a atividade da enzima SPS foi semelhante à das
plantas controle, porém houve aumento do estado de ativação da enzima, sugerindo que o frio
não afetou o conteúdo de proteína. Já a cultivar suscetível, apresentou decréscimo da
atividade da SPS após exposição ao frio, provavelmente devido a uma redução desta enzima.
Sob deficiência hídrica moderada, DU et al. (1998) observaram em folha de cana-de-
açúcar, que os processos bioquímicos de síntese de sacarose e amido, do ciclo de Calvin e da
rota C4 não foram seriamente afetados sendo o fechamento estomático a causa do declínio da
fotossíntese. Esses autores sugerem que sob deficiência hídrica severa, a queda significante da
atividade da PPDK (piruvato ortofosfato diquinase) seja responsável pela queda da
fotossíntese. Foi observado ainda aumento da glicose e frutose, possivelmente, devido ao
aumento da atividade de enzimas de quebra do amido e da sacarose, resultando em aumento
da concentração osmótica em folhas de cana-de-açúcar.

48
VANDOORME et al. (2012) observaram em chicória que, sob deficiência hídrica, não
houve impacto sob a concentração de proteína, porém houve aumento da atividade da SPS
foliar, enquanto a atividade da SuSy não foi significativamente afetada. Já a atividade da
invertase ácida foi maior no início do tratamento de deficiência hídrica, enquanto a invertase
neutra teve decréscimo no final do tratamento quando comparada às plantas controle. Além
disso, as plantas sob estresse aumentaram a eficiência do uso da água e a concentração de
açúcares solúveis, houve diminuição na proporção raiz-parte aérea e baixou o potencial
osmótico.
Algumas cultivares de cana-de-açúcar apresentam diferentes respostas de aclimatação
e de recuperação após a ocorrência de deficiência hídrica (LANDELL et al., 2004;
MACHADO et al., 2009; RIBEIRO et al., 2013) e de baixa temperatura (DU & NOSE, 2002;
SALES et al., 2012).
Nossa hipótese é que cultivares de cana-de-açúcar mais tolerantes à deficiência hídrica
e/ou baixa temperatura apresentam metabolismo do carbono (fotossíntese e metabolismo de
carboidratos) menos suscetível a estes fatores ambientais. Baseado nesta hipótese, nosso
objetivo é estudar os efeitos da ocorrência de baixa temperatura e/ou deficiência hídrica sobre
a fotossíntese (trocas gasosas e atividade fotoquímica) e sobre o metabolismo de carboidratos
(acúmulo de carboidratos e atividade de enzimas) em duas cultivares de cana-de-açúcar, com
diferentes características quanto a sua rusticidade.
2 MATERIAL E MÉTODOS
Em bandejas contendo substrato comercial (Carolina Soil®, Vera Cruz, RS) composto
de turfa de esfagno, vermiculita expandida, calcário dolomítico, gesso agrícola e fertilizante
NPK (traços) foram plantados mini-toletes de cana-de-açúcar (Saccharum spp.) cv. IACSP94-
2094 e cv. IACSP95-5000. A IACSP94-2094 apresenta rusticidade sendo indicada para
ambientes desfavoráveis e a IACSP95-5000 é uma cultivar produtiva e indicada para
ambientes favoráveis (LANDELL et al., 2005).
Aos 35 dias após o plantio (DAP), as mudas foram transplantadas para vasos plásticos
contendo 8,5 L de uma mistura de terra, areia e substrato na proporção 1:1:1 (v:v:v). Foram
plantadas uma muda por vaso e conduzidos somente o colmo primário. As plantas foram
mantidas em casa de vegetação onde receberam tanto irrigação diária quanto aplicações de
nutrientes. As aplicações dos nutrientes foram parceladas em três vezes, totalizando, por vaso:

49
18,21 g de Ca(NO3)2; 5,31 g de fosfato monoamônico; 7,29 g de KCl; 2,12 g de MgSO4; 0,17
g de H3BO3; 0,20 g de MnSO4; 0,02 g de CuSO4; 0,02 g de (NH4)6Mo7O24 x 4(H2O); 0,09 g
de ZnSO4; e 0,212 mg de FeEDTA (6% Fe).
Aos 87 DAP, as plantas foram transferidas para câmara de crescimento (Instalafrio,
Brasil) onde permaneceram por um período de 18 dias, recebendo irrigação diária, nas
seguintes condições ambientais: fotoperíodo 14 h/10 h (dia/noite), temperatura do ar
32±1/20±1 °C (dia/noite), umidade relativa de 65% e Q de 1000 μmol m-2
s-1
(14 h). Após o
18º dia, a temperatura da câmara foi diminuída para 22±1/12±1 °C (dia/ noite). Metade das
plantas permaneceu irrigada e a outra metade foi submetida à deficiência hídrica. A restrição
hídrica foi imposta pela suspensão da rega até 30% da capacidade máxima de retenção de
água do substrato, medida por pesagem dos vasos. As plantas permaneceram nestas condições
(22±1/12±1 °C sem ou com restrição hídrica) por 22 dias, após este período, elas foram
reidratadas e a temperatura da câmara de crescimento foi reajustada para 32±1/20±1 °C
(dia/noite) e permaneceram assim por um período de 8 dias.
Durante o período experimental, foram realizadas seis medidas/coletas, nos seguintes
dias, contados após o período de aclimatação das plantas: 1ª medida/coleta feita no 18º dia na
temperatura 32±1/20±1 °C em plantas irrigadas (I) (testemunha); 2ª medida/coleta feita após
34 horas de baixa temperatura com e sem deficiência hídrica; 3ª medida/coleta feita após 13
dias de baixa temperatura e deficiência hídrica (estresse intermediário); 4ª medida/coleta feita
após 20 dias de baixa temperatura e deficiência hídrica (máximo estresse); 5ª medida/coleta
feita após dois dias de retorno à temperatura inicial e reidratação; e a 6ª (medida/coleta) feita
após 8 dias de retorno à temperatura inicial e reidratação.
2.1 Variáveis medidas e calculadas
Assimilação de CO2 e fluorescência da clorofila a
Mediu-se a variação diurna das trocas gasosas e fluorescência da clorofila a por meio
de um analisador de gases por infravermelho integrado com câmara de fluorescência, modelo
Li 6400-40F (Licor, Inc. Nebraska, EUA). As medidas foram realizadas na primeira folha
totalmente expandida e com lígula aparente (folha +1), no terço médio do limbo foliar, em
intervalos de três horas, totalizando cinco medidas, em Q de 1300 μmol m-2
s-1
e déficit de
pressão de vapor entre a folha e o ar ao redor de 1,5 kPa, as temperatura utilizadas foram as
mesmas indicadas nos tratamentos testemunha (32 °C) e baixa temperatura (22 °C). As

50
variáveis medidas em relação às trocas gasosas foram: assimilação de CO2
(A, μmol m-2
s-1
),
condutância estomática (gs, mol m
-2 s
-1), transpiração (E, mmol m
-2 s
-1) e concentração interna
de CO2 (Ci). Calculou-se a eficiência aparente de carboxilação pela razão entre A/Ci (ZHANG
et al., 2001) e a eficiência intrínseca do uso da água (EUAi) pela razão (A/gs).
As variáveis analisadas em relação à fluorescência da clorofila a foram realizadas
como descrito no capítulo II.
Para análise dos dados tanto das trocas gasosas como da fluorescência da clorofila a,
foram utilizadas as médias das 20 medidas (quatro medidas por horário) realizadas em cada
dia do período experimental. Calculou-se a assimilação diurna de CO2 (Ai) a partir da
integração da assimilação instantânea de CO2 ao longo do dia, utilizando a média de 4
repetições.
Potencial da água na folha
Em cada um dos dias de medidas das trocas gasosas também foram realizadas medidas
do potencial da água na folha (Ψw), antes das lâmpadas da câmara de crescimento serem
acesas (pré-manhã) e às 14:00 h, como descrito no capítulo II.
Teor de carboidratos
Nos dias de medidas, às 9:00 h foram coletadas folhas +1 de quatro plantas por
tratamento, as quais foram imediatamente imersas em nitrogênio líquido e mantidas em
freezer (-80 °C) até o momento das análises. Antes da elaboração do extrato para análise do
teor de carboidratos, as folhas foram submetidas à secagem em estufa com circulação forçada
de ar à temperatura de 60 °C, por quatro dias ou até massa constante. Os procedimentos foram
realizados como descrito no capítulo II.
Os extratos para análises de sacarose (SAC) e de açúcares solúveis totais (AST) foram
obtidos pelo método descrito por BIELESK & TURNER (1966).
A determinação do teor de AST foi feita pelo método do fenol-sulfúrico, descrito por
DUBOIS et al. (1956), de SAC pelo método descrito por VAN HANDEL (1968) e de amido
pelo método enzimático descrito por AMARAL et al. (2007).

51
Atividade de enzimas do metabolismo de carboidratos
A atividade das enzimas envolvidas no metabolismo de carboidratos foi quantificada
em folhas +1 que foram coletadas às 9:00 h e imediatamente imersas em nitrogênio líquido e
mantidas em freezer (-80 °C) até o momento das análises.
Para obtenção do extrato para determinação da atividade enzimática foram macerados
com nitrogênio líquido, 300 mg de material vegetal fresco em almofariz com 5% de
polivinilpolipirrolidona (PVPP) e 1,5 mL de tampão fosfato de potássio 100 mM contendo
EDTA 1mM com pH 7,0. Em seguida esse extrato foi centrifugado a 14.000 g por 30 minutos
a 4 °C e o sobrenadante foi utilizado para as análises.
Proteína solúvel total
A dosagem de proteína total no extrato foi feita segundo BRADFORD (1976),
utilizando-se um reagente preparado (Sigma-Aldrich, Brasil). Em tubo de ensaio adicionaram-
se 10 μL de extrato, 90 μL de água e 3 mL do reagente preparado, diluído na proporção 1:4
(reagente: água). Fez-se a leitura da absorbância em espectrofotômetro (Genesys 10UV
Scanning, Thermo Scientific) no comprimento de onda de 595 nm. A concentração de
proteína total foi calculada a partir de uma curva padrão obtida com leituras de soluções
contendo 5, 10, 20, 40 e 60 µg de albumina sérica bovina (BSA). Como branco, colocou-se
água no lugar da amostra.
Atividade da sintase de sacarose fosfato
A determinação da atividade da sintase de sacarose fosfato (SPS, EC 2.4.1.14) foi feita
segundo ZHU et al. (1997) com adaptações. Foram adicionados, em tubo de rosca, 50 μL de
extrato e 50 μL de tampão de reação contendo: tampão Tris-HCl 200 mM em pH 7,5, cloreto
de magnésio (MgCl2) 10 mM, EDTA 2 mM, frutose-6-fosfato (Fru-6-P) 8 mM, glicose-6-
fosfato (Glu-6-P) 40 mM e UDP-glicose (uridina 5'-difosfoglicose) 50 mM. A reação foi
incubada a 37 °C por 0, 30 e 60 minutos. A reação foi interrompida em banho-maria a 100 °C
por três minutos.
A dosagem da sacarose formada na reação foi realizada como descrito por VAN
HANDEL (1968). Foram adicionadas à reação 100 μL de KOH 30% e mantida, por 10

52
minutos, em banho-maria a 100 °C. Em seguida, acrescentou-se 1,5 mL de reagente antrona
preparado da seguinte forma: 76 mL de H2SO4, 30 mL de água e 150 mg de antrona. A reação
foi incubada a 40 °C por 20 minutos e realizada a leitura da absorbância em
espectrofotômetro (Genesys 10UV Scanning - Thermo Scientific) no comprimento de onda de
620 nm. A concentração de sacarose foi calculada a partir de uma curva padrão obtida com
leituras de soluções contendo respectivamente 0,5, 1, 2, 3 e 4 mM de sacarose. Como branco,
colocou-se água no lugar da amostra.
Atividade da sintase de sacarose
A determinação da atividade da sintase de sacarose (SuSy, EC 2.4.1.13) foi feita
segundo ZHU et al. (1997) com adaptações, em tubo de rosca foram adicionados 50 μL de
extrato e 50 μL de tampão de reação contendo: tampão Tris-HCl 200 mM em pH 7,5, MgCl2
15 mM, frutose 25 mM e UDP-glicose 25 mM. A reação foi incubada a 37 °C por 0, 30 e 60
minutos e foi interrompida em banho-maria a 100 °C por três minutos. A dosagem da
sacarose formada foi realizada como descrito anteriormente para a enzima SPS, segundo VAN
HANDEL (1968).
Atividade das invertases ácidas
A atividade da enzima invertase ácida solúvel (IVA, EC 2.4.1.25) foi obtida pelo
método descrito por ZHU et al. (1997). Em microtubo foram adicionados: 50 μL de extrato,
50 μL de tampão de reação acetato de sódio 1 M e pH 4,5 e 100 μL de uma solução de
sacarose 120 mM. A reação foi incubada a 37 °C por 0, 30 e 60 minutos. A reação foi
interrompida acrescentando-se 30 μL de Tris 2,5 M e levada ao banho-maria a 100 °C por três
minutos.
A dosagem de açúcares redutores foi realizada pelo método de Somogyi-Nelson
(NELSON, 1944; SOMOGYI, 1945; 1952). Foram colocados em tubos de ensaio 100 μL de
reação enzimática e 400 μL de água, em seguida adicionou-se 500 μL de solução Somogyi
A+B (misturadas na proporção 4:1), os tubos foram agitados, vedados e levados ao banho-
maria 100 °C por 10 minutos. Ao término do tempo a reação foi colocada em banho de gelo e
em seguida adicionou-se 500 μL de solução de Nelson e 1000 μL de água. Os tubos foram
agitados e foram feitas as leituras de absorbância em espectrofotômetro (Genesys 10UV

53
Scanning - Thermo Scientific) no comprimento de onda de 560 nm. A concentração de
açúcares redutores foi calculada a partir de uma curva padrão obtida com leituras de soluções
contendo respectivamente 0,5, 1, 2, 3 e 4 mM de glicose. Como branco, colocou-se água no
lugar da amostra.
Atividade das invertases neutras
Procedeu-se a atividade da enzima invertase neutra (IVN, EC 2.4.1.26) pelo método
descrito por ZHU et al. (1997). Em microtubo foram adicionados: 50 μL de extrato, 50 μL de
tampão de reação acetato de sódio 1 M e pH 7,5 e 100 μL de uma solução de sacarose 120
mM. A reação foi incubada a 37 °C por 0, 30 e 60 minutos. A reação foi interrompida em
banho-maria a 100 °C por três minutos. A dosagem de açúcares redutores foi realizada pelo
método de Somogyi-Nelson (NELSON, 1944; SOMOGYI, 1945; 1952), como descrito para
IVA.
Delineamento experimental
O delineamento experimental foi inteiramente ao acaso com parcelas subdivididas no
tempo, sendo os fatores de variação as cultivares (IACSP94-2094 e IACSP95-5000), a
temperatura (32/20 °C e 22/12 °C) e o status hídrico (irrigado e deficiência hídrica). Os
resultados foram submetidos à análise de variância (ANOVA) sendo as médias provenientes
de vinte repetições (trocas gasosas e fluorescência da clorofila a) e quatro repetições
(assimilação diária de CO2, potencial hídrico e metabolismo de carboidratos). Quando
encontradas diferenças significativas, as médias foram comparadas pelo teste de Tukey ao
nível de 5% de probabilidade.
3 RESULTADOS
Ambas as cultivares submetidas à DH tiveram decréscimo significativo do potencial
hídrico foliar (Ψw6h) atingindo o valor de -0,69 no período de estresse máximo, nas plantas NI
(Tabela 1), considerado estresse moderado (DU et al., 1996), sendo que somente a baixa
temperatura não afetou Ψw6h. Não houve diferença significativa no Ψw medido às 14:00 h
(dados não apresentados).

54
Tabela 1 - Resposta do potencial hídrico foliar (Ψw6h) de cana-de-açúcar cv. IACSP94-2094 e
cv. IACSP95-5000 submetidas aos tratamentos de baixa temperatura e deficiência hídrica.
Médias de quatro repetições (± desvio padrão).
Ψw6h (MPa)
cv. Controle
(32/20 °C)
Máximo estresse
(22/12°C)
IACSP94-2094 I -0,35 ± 0,02 -0,36 ± 0,02
IACSP94-2094 NI -0,35 ± 0,02 -0,69 ± 0,02
IACSP95-5000 I -0,40 ± 0,02 -0,40 ± 0,015
IACSP95-5000 NI -0,40 ± 0,02 -0,68 ± 0,02
Independente do tratamento (controle, baixa temperatura e baixa temperatura e
deficiência hídrica), a assimilação de CO2 (A) (Figura 1A, B) e a assimilação diária de CO2
(Ai) (Figura 1C, D) da IACSP95-5000 foram significativamente maiores que o da IACSP94-
2094.
Em ambas as cultivares após 34 horas de baixa temperatura houve decréscimo
significativo de A e de Ai (Figura 1C, D). Após a imposição dos tratamentos, o decréscimo de
A na IACSP94-2094 foi de 35% enquanto na IACSP95-5000 foi de 17,5%, permanecendo
baixo durante todo o período de tratamento (Figura 1A, B).
No dia de máxima restrição hídrica (dia 20), A do tratamento não irrigado (NI) da
IACSP95-5000 foi significativamente mais baixo quando comparado às plantas irrigadas (I)
(Figura 1B), enquanto na IACSP94-2094 A nos tratamentos I e NI foi semelhante. Após dois
dias de retorno às temperaturas 32/20 °C (dia/noite) e reidratação das plantas, a IACSP94-
2094 recuperou A e Ai (Figura 1A, C) enquanto que na cv. IACSP95-5000 NI esta
recuperação ocorreu após 8 dias (Figura 1B, D).
Houve decréscimo significativo da condutância estomática (gs) (Figura 2A, B) e
transpiração (E) (Figura 2C, D) após 34 h de resfriamento em ambas as cultivares,
independente do status hídrico, permanecendo assim durante todo o período de estresse.
Ambas cvs. recuperaram gs e E após dois dias de retorno às temperaturas mais altas e
reidratação das plantas. Interessante notar que após 8 dias em recuperação gs e E da
IACSP95-5000 I e NI foram maiores que o controle, ocorrendo um súbito aumento.

55
Figura 1 - (A, B) Resposta da assimilação de CO2 (A) e (C, D) assimilação diária de CO2 (Ai)
de cana-de-açúcar, cultivares IACSP94-2094 e IACSP95-5000, sendo o dia 0 (testemunha)
medida feita após 18 dias de aclimatação a 32/20 °C (dia/ noite) com plantas irrigadas; dia 2
medida feita após 34 horas a 22/12 °C (dia/ noite) com plantas irrigadas (I) e não irrigadas
(NI); dia 13 medida feita após 13 dias de baixa temperatura em plantas irrigadas e não
irrigadas (estresse intermediário); dia 20 medida após 20 dias de baixa temperatura em plantas
irrigadas e não irrigadas (estresse máximo); dia 22 medida após 2 dias de retorno à
temperatura de 32/20 °C e reidratação e dia 28 medida após 8 dias de recuperação das plantas.
Símbolos indicam média de 20 repetições ± erro padrão para A e 4 repetições ± erro padrão
para Ai.
Houve decréscimo significativo da eficiência intrínseca do uso da água (EUAi) após 13
dias de baixa temperatura em ambas as cvs., independente do status hídrico, permanecendo
baixo durante o estresse máximo (Figura 2E, F). Entretanto, EUAi no máximo estresse na cv.
IACSP94-2094 NI foi maior que nas plantas I (Figura 2E).
Foi observado aumento significativo de Ci em ambas as cultivares após 13 dias de
imposição dos tratamentos, mantendo-se alto até o máximo estresse (Figura 3A, B). A
IACSP94-2094 I apresentou Ci mais alto que das plantas NI após 34 h de baixa temperatura
(Figura 3A). Após dois dias de retorno às temperaturas mais altas e reidratação das plantas, Ci
voltou aos valores controle (Figura 3A, B).
5
10
15
20
25
30
0 2 13 20 22 28
200
400
600
800
1000
1200
0 2 13 20 22 28
A (
mol
m-2
s-1
)
IACSP94-2094 I
IACSP94-2094 NI
A B
IACSP95-5000 I
IACSP95-5000 NI
C
Ai (
mm
ol
m-2 d
-1)
Dias de tratamento
D

56
Figura 2 - (A, B) Resposta da condutância estomática (gs), (C, D) transpiração (E) e (E, F)
eficiência intrínseca do uso da água (EUAi) de cana-de-açúcar, cultivares IACSP94-2094 e
IACSP95-5000, sendo o dia 0 (testemunha) medida feita após 18 dias de aclimatação a 32/20
°C (dia/ noite) com plantas irrigadas; dia 2 medida feita após 34 horas a 22/12 °C (dia/ noite)
com plantas irrigadas (I) e não irrigadas (NI); dia 13 medida feita após 13 dias (estresse
intermediário); de baixa temperatura em plantas irrigadas e não irrigadas; dia 20 medida após
20 dias de baixa temperatura em plantas irrigadas e não irrigadas (estresse máximo); dia 22
medida após 2 dias de retorno à temperatura de 32/20 °C e reidratação e dia 28 medida após 8
dias de recuperação das plantas. Símbolos indicam média de 20 repetições ± erro padrão.
O frio e a deficiência hídrica causaram queda na eficiência aparente de carboxilação
(A/Ci) em ambas as cultivares e tratamentos, sendo a queda em IACSP95-5000 foi
relativamente mais acentuada. Porém, comparativamente, os valores de A/Ci foram mais
elevados em IACSP95-5000. A resposta de A/Ci foi oposta a de Ci, ou seja, quando Ci
aumentou, A/Ci diminuiu (Figura 3C e 3D).
A partir de 34 h de baixas temperaturas, a eficiência operacional do FSII (Fq'/Fm') de
ambas as cultivares, tanto das plantas I como nas NI, baixou significativamente
permanecendo baixa durante todo o período de estresse (Figura 4A, B). As duas cultivares
recuperaram Fq'/Fm' logo no primeiro dia de retorno às temperaturas mais altas e reidratação
(Figura 4).
1,5
3,0
4,5
6,0
7,5
0 2 13 2022 28
60
90
120
150
180
0,04
0,08
0,12
0,16
0,20
0,24
0 2 13 2022 28
B
IACSP95-5000 I
IACSP95-5000 NI
CE
(m
mo
l m
-2 s
-1)
D
E
EU
Ai (
mo
l m
ol-1
)
Dias de tratamento
gs (
mo
l m
-2 s
-1)
IACSP94-2094 I
IACSP94-2094 NI
A
F

57
Figura 3 - (A, B) Variação da concentração intercelular de CO2 (Ci) e da (C, D) eficiência
aparente de carboxilação (A/Ci) de cana-de-açúcar, cultivares IACSP94-2094 e IACSP95-
5000, sendo: dia 0 (testemunha) medida feita após 18 dias de aclimatação a 32/20 °C (dia/
noite) com plantas irrigadas; dia 2 medida feita após 34 horas a 22/12 °C (dia/ noite) com
plantas irrigadas e não irrigadas; dia 13 medida feita após 13 dias (estresse intermediário) de
baixa temperatura em plantas irrigadas (I) e não irrigadas (NI); dia 20 medida após 20 dias de
baixa temperatura em plantas irrigadas e não irrigadas (estresse máximo); dia 22 medida após
2 dias de retorno à temperatura de 32/20 °C e reidratação e dia 28 medida após 8 dias de
recuperação das plantas. Símbolos indicam média de 20 repetições ± erro padrão.
Houve aumento significativo do coeficiente de extinção não fotoquímico (NPQ)
durante o período de baixas temperaturas na cv. IACSP94-2094 I e NI, e no dia de máximo
estresse, o NPQ das plantas NI foi significativamente menor que das plantas I (Figura 5A). Na
cv. IACSP95-5000 o NPQ foi semelhante durante todo o período experimental (Figura 5B).
Nas plantas I e NI das duas cultivares houve decréscimo significativo de Fv/Fm após 34
h de baixa temperatura, permanecendo baixo durante todo o período de tratamento (Figura
5C, D) e ambas recuperaram Fv/Fm após o período de retorno às temperaturas mais altas e
reidratação.
Houve decréscimo significativo da eficiência quântica máxima do FSII sob luz
(Fv'/Fm'), durante o período de baixas temperaturas na IACSP94-2094 I e na NI, porém, nas
plantas NI o Fv'/Fm' foi significativamente maior que nas plantas I. A IACSP94-2094 NI
recuperou parcialmente Fv'/Fm' (Figura 5C). A IACSP95-5000 NI apresentou decréscimo
significativo de Fv'/Fm' após 34 h de baixa temperatura e durante o máximo estresse por
100
150
200
250
300
0 2 13 20 22 28
0,5
1,0
1,5
2,0
2,5
3,0
0 2 13 20 22 28
Ci (
mo
l m
ol-1
)
IACSP94-2094 I
IACSP94-2094 NI
A B
IACSP95-5000 I
IACSP95-5000 NI
C
A/C
i (
mo
l m
-2 s
-1 P
a-1)
Dias de tratamento
D

58
temperatura e deficiência hídrica tendo se recuperado totalmente após retorno às temperaturas
mais altas e reidratação (Figura 5D).
Figura 4 - (A, B) Resposta da eficiência operacional do FSII (Fq'/Fm') de cana-de-açúcar,
cultivares IACSP94-2094 e IACSP95-5000, sendo o dia 0 (testemunha) medida feita após 18
dias de aclimatação a 32/20 °C (dia/ noite) com plantas irrigadas; dia 2 medida feita após 34
horas a 22/12 °C (dia/ noite) com plantas irrigadas (I) e não irrigadas (NI); dia 13 medida feita
após 13 dias (estresse intermediário); de baixa temperatura em plantas irrigadas e não
irrigadas; dia 20 medida após 20 dias de baixa temperatura em plantas irrigadas e não
irrigadas (estresse máximo); dia 22 medida após 2 dias de retorno à temperatura de 32/20 °C e
reidratação e dia 28 medida após 8 dias de recuperação das plantas. Símbolos indicam média
de 20 repetições ± erro padrão.
Na IACSP94-2094 I e NI houve decréscimo significativo do fator de eficiência do
fotossistema II (Fq'/Fv') após 34 h de frio, ocorrendo em seguida a recuperação (Figura 6A). Já
na IACSP95-5000, tanto I como NI, Fq'/Fv' decresceu significativamente por todo período de
estresse (Figura 6B), com o retorno às temperaturas maiores e reidratação os valores de Fq'/Fv'
se recuperaram.
Em ambas as cultivares o transporte aparente de elétrons (ETR) decresceu
significativamente após 34 h de baixas temperaturas, permanecendo baixo durante todo o
período de tratamento (Figura 6C, D) e recuperando ETR após o retorno às temperaturas mais
altas e reidratação (Figura 6C, D).
Houve aumento significativo do teor de açúcares solúveis (AS) no período de máximo
estresse (Figura 7A) na IACSP94-2094 I e NI. Após o retorno às temperaturas de 32/20 °C e
reidratação, os valores não retornaram aos do controle, enquanto que nas NI, retornaram
(Figura 7A). Já na IACSP95-5000 I e NI houve aumento significativo de AS após 34 h de
baixa temperatura, permanecendo alto durante todo o período de estresse (Figura 7B) e
0 2 13 20 22 28
0,08
0,12
0,16
0,20
0,24
0,28
0 2 13 20 22 28
F
q'/F
m'
Dias de tratamento
IACSP94-2094 I
IACSP94-2094 NI
A B
IACSP95-5000 I
IACSP95-5000 NI

59
recuperando aos valores do controle após o período de retorno às temperaturas mais altas e
reidratação (Figura 7B).
Figura 5 - (A, B) Variação do coeficiente de extinção não fotoquímico (NPQ) e da (C, D)
eficiência quântica máxima do FSII (Fv/Fm) e eficiência quântica máxima do FSII sob Q
(Fv'/Fm') de cana-de-açúcar, cultivares IACSP94-2094 e IACSP95-5000, sendo o dia 0
(testemunha) medida feita após 18 dias de aclimatação a 32/20 °C (dia/ noite) com plantas
irrigadas; dia 2 medida feita após 34 horas a 22/12 °C (dia/ noite) com plantas irrigadas (I) e
não irrigadas (NI); dia 13 medida feita após 13 dias de baixa temperatura em plantas irrigadas
e não irrigadas; dia 20 medida após 20 dias de baixa temperatura em plantas irrigadas e não
irrigadas (máximo estresse); dia 22 medida após 2 dias de retorno à temperatura de 32/20 °C e
reidratação e dia 28 medida após 8 dias de recuperação das plantas. Símbolos indicam média
de 20 repetições ± erro padrão.
O teor de sacarose (SAC) aumentou significativamente na IACSP94-2094 NI no
período de máximo estresse (Figura 7C), enquanto na IACSP95-5000 I e NI o aumento de
SAC ocorreu logo após 34 h de baixa temperatura, permanecendo alto durante todo o período
de estresse (Figura 7D). SAC tanto da IACSP94-2094 NI como da IACSP95-5000 I e NI
retornaram aos valores do controle após o retorno da temperatura e reidratação (Figura 7C,
D).
0,6
0,9
1,2
1,5
1,8
2,1
0 2 13 20 22 280,30
0,45
0,60
0,75
0 2 13 20 22 28
NP
Q
IACSP94-2094 I
IACSP94-2094 NI
A B
IACSP95-5000 I
IACSP95-5000 NI
C
Fv'/
Fm'
F
v/Fm
Dias de tratamento
D

60
Figura 6 - (A, B) Variação do fator de eficiência do FSII (Fq'/Fv') e do (C, D) transporte
aparente de elétrons (ETR) de cana-de-açúcar, cultivares IACSP94-2094 e IACSP95-5000,
sendo o dia 0 (testemunha) medida feita após 18 dias de aclimatação a 32/20 °C (dia/ noite)
com plantas irrigadas; dia 2 medida feita após 34 horas a 22/12 °C (dia/ noite) com plantas
irrigadas (I) e não irrigadas (NI); dia 13 medida feita após 13 dias de baixa temperatura em
plantas irrigadas e não irrigadas; dia 20 medida após 20 dias de baixa temperatura em plantas
irrigadas e não irrigadas (máximo estresse); dia 22 medida após 2 dias de retorno à
temperatura de 32/20 °C e reidratação e dia 28 medida após 8 dias de recuperação das plantas.
Símbolos indicam média de 20 repetições ± erro padrão.
Em ambas as cultivares, independente do status hídrico, houve um aumento
significativo no teor de amido foliar (AMI), sendo na IACSP94-2094 no período de baixa
temperatura e deficiência hídrica (Figura 7E), enquanto que na IACSP95-5000 o aumento
ocorreu logo após 34 h de baixa temperatura (Figura 7F). Após o período de retorno da
temperatura e reidratação na IACSP94-2094 (Figura 7E), os teores de AMI não atingiram os
valores do controle, enquanto na IACSP95-5000 houve recuperação parcial dos teores de AMI
(Figura 7F).
A atividade da sintase de sacarose (SuSy) aumentou na IACSP94-2094 I e NI com as
baixas temperaturas (Figura 8A). Nas plantas I esse aumento foi observado somente no
período de máximo estresse, enquanto nas plantas NI esse aumento ocorreu no período de
estresse intermediário (Figura 8A).
0 2
13
20
22
28
40
60
80
100
120
0,18
0,27
0,36
0,45
0,54
0 2
13
20
22
28
C
ET
R (
mol
m-2 s
-1)
Dias de tratamento
Fq'/F
v'
IACSP94-2094 I
IACSP94-2094 NI
A B
IACSP95-5000 I
IACSP95-5000 NI
D

61
Figura 7 - (A, B) Variação no teor dos açúcares solúveis (AS), da (C, D) sacarose (SAC) e do
amido (AMI) em folhas de cana-de-açúcar, cultivares IACSP94-2094 e IACSP95-5000, sendo
o dia 0 (testemunha) medida feita após 18 dias de aclimatação a 32/20 °C (dia/ noite) com
plantas irrigadas; dia 2 medida feita após 34 horas a 22/12 °C (dia/ noite) com plantas
irrigadas (I) e não irrigadas (NI); dia 13 medida feita após 13 dias de baixa temperatura em
plantas irrigadas e não irrigadas; dia 20 medida após 20 dias de baixa temperatura em plantas
irrigadas e não irrigadas (máximo estresse); dia 22 medida após 2 dias de retorno à
temperatura de 32/20 °C e reidratação e dia 28 medida após 8 dias de recuperação das plantas.
Símbolos indicam média de quatro repetições ± erro padrão.
Durante o máximo estresse observou-se ainda que a atividade da SuSy na IACSP94-
2094 I foi significativamente maior que das plantas NI (Figura 8A). A atividade da SuSy na
IACSP94-2094 retornou aos valores do controle no período de recuperação (Figura 8A). Foi
observado aumento significativo da atividade da SuSy na IACSP95-5000 NI no estresse
intermediário (Figura 8B), retornando aos valores do controle já no máximo estresse.
Houve aumento significativo na atividade da sintase de sacarose fosfato (SPS) na
IACSP94-2094 I e NI durante o período de baixas temperaturas (Figura 8C). No período de
máximo estresse, a atividade da SPS foi maior nas plantas NI (Figura 8C). Na IACSP95-5000
a atividade da SPS foi semelhante durante todo o período experimental (Figura 8D).
240
320
400
480
560
50
100
150
200
250
0 2 13 20 22 28
0
70
140
210
280
350
420
0 2 13 20 22 28
AS
(
mo
l g
-1 M
S)
IACSP94-2094 I
IACSP94-2094 NI
A
B
IACSP95-5000 I
IACSP95-5000 NI
C
SA
C (
mo
l g
-1 M
S)
D
E
AM
I (
mo
l g
-1 M
S)
Dias de tratamento
F

62
Figura 8 - Variação da atividade das enzimas (A, B) sintase de sacarose (SuSy) e da (C, D)
sintase de sacarose fosfato (SPS) em folhas de cana-de-açúcar, cultivares IACSP94-2094 e
IACSP95-5000, sendo o dia 0 (testemunha) medida feita após 18 dias de aclimatação a 32/20
°C (dia/ noite) com plantas irrigadas; dia 2 medida feita após 34 horas a 22/12 °C (dia/ noite)
com plantas irrigadas e não irrigadas; dia 13 medida feita após 13 dias de baixa temperatura
em plantas irrigadas e não irrigadas; dia 20 medida após 20 dias de baixa temperatura em
plantas irrigadas e não irrigadas (máximo estresse); dia 22 medida após 2 dias de retorno à
temperatura de 32/20 °C e reidratação e dia 28 medida após 8 dias de recuperação das plantas.
Símbolos indicam média de quatro repetições ± erro padrão.
Foi observado decréscimo significativo da atividade das invertases ácidas (IVA) na
IACSP94-2094 I e NI durante o período de estresse (Figura 9A) e houve recuperação dos
valores após o retorno às temperaturas de 32/20 °C e reidratação (Figura 9A). Nas IACSP95-
5000 I e NI houve decréscimo, apesar de não significativo, na atividade das IVA somente após
34 h de baixa temperatura, recuperando os valores mesmo com a continuidade do estresse
(Figura 9B). Em IACSP95-5000 I, no 8º dia de recuperação, a atividade da IVA foi
significativamente maior que a da testemunha (Figura 9B).
Houve aumento significativo na atividade das invertases neutras (IVN) nas cultivares
IACSP94-2094 I e IACSP95-5000 I no máximo estresse (Figura 9C, D), enquanto neste
mesmo período houve decréscimo significativo das atividades em ambas as cultivares NI
(Figura 9C, D). As cultivares NI recuperaram a atividade das IVN após dois dias de retorno às
temperaturas mais altas e reidratação das plantas (Figura 9C, D).
0,00
0,15
0,30
0,45
0,60
0 2 13 20 22 28
0,00
0,15
0,30
0,45
0,60
0,75
0 2 13 20 22 28
Su
Sy
(m
ol
gM
F m
in-1
)
IACSP94-2094 I
IACSP94-2094 NI
A
B
IACSP95-5000 I
IACSP95-5000 NI
C
SP
S
(m
ol
gM
F m
in-1
)
Dias de tratamento
D

63
Figura 9 - Variação da atividade das (A, B) invertases ácidas (IVA) e das (C, D) invertases
neutras (IVN) em folhas de cana-de-açúcar, cultivares IACSP94-2094 e IACSP95-5000,
sendo o dia 0 (testemunha) medida feita após 18 dias de aclimatação a 32/20 °C (dia/ noite)
com plantas irrigadas; dia 2 medida feita após 34 horas a 22/12 °C (dia/ noite) com plantas
irrigadas e não irrigadas; dia 13 medida feita após 13 dias de baixa temperatura em plantas
irrigadas e não irrigadas; dia 20 medida após 20 dias de baixa temperatura em plantas
irrigadas e não irrigadas (máximo estresse); dia 22 medida após 2 dias de retorno à
temperatura de 32/20 °C e reidratação e dia 28 medida após 8 dias de recuperação das plantas.
Símbolos indicam média de quatro repetições ± erro padrão.
4 DISCUSSÃO
Período de baixa temperatura e deficiência hídrica
Diversos fatores ambientais, como por exemplo a seca, temperaturas extremas e a
salinidade, afetam negativamente o crescimento e desenvolvimento das plantas, além do
rendimento médio de uma cultura (ASHRAF & FOOLAD, 2007), devido a uma série de
distúrbios morfológicos, fisiológicos, bioquímicos e moleculares (WANG et al., 2003), o que
leva ao interesse em elucidá-los e relacioná-los à tolerância das plantas a estes fatores
ambientais.
A assimilação de CO2 (A) da IACSP95-5000 na testemunha (32/20 °C e irrigada) foi
significativamente maior que a da IACSP94-2094 (Figura 1A, B). Dois fatores determinam
0,0
0,9
1,8
2,7
3,6
4,5
5,4
0 2 13 20 22 280,0
0,9
1,8
2,7
3,6
4,5
0 2 13 20 22 28
IVA
(m
ol
gM
F m
in-1
)
IACSP94-2094 I
IACSP94-2094 NI
A
B
IACSP95-5000 I
IACSP95-5000 NI
C
IVN
(m
ol
gM
F m
in-1
)
Dias de tratamento
D

64
esta resposta, ou seja, os maiores valores de gs (Figura 2A, B) permitindo maior fluxo de
difusão do CO2 através das aberturas estomáticas, combinados com os maiores valores da
razão A/Ci (Figura 3C), que indica maior eficiência de carboxilação. Outras características se
destacam na IACSP95-5000, como a maior eficiência operacional do fotossistema II (Fq'/Fm',
Figura 4A, B) e consequentemente, maior ETR em relação a IACSP94-2094 (Figura 6C, D).
A IACSP95-5000 destaca-se em relação à IACSP94-2094 como sendo uma cultivar menos
rústica e mais produtiva em ambientes favoráveis (LANDELL et al., 2005), e neste trabalho
destacou-se também como uma cultivar com maior capacidade fotossintética.
Sob estresse, independente do tratamento, baixa temperatura com e sem deficiência
hídrica, A e Ai da IACSP95-5000 tiveram valores significativamente maiores que o da
IACSP94-2094 (Figura 1). Entretanto, nas duas cultivares ocorreu decréscimo significativo
destes parâmetros devido ao estresse. A queda relativa de Ai na IACSP94-2094 sob estresse
máximo de baixa temperatura (48%) e baixa temperatura e deficiência hídrica (38%) foram
estatisticamente semelhantes, não apresentando efeito cumulativo importante. No entanto, na
IACSP95-5000 ocorreu efeito cumulativo dos dois estresses, já que sob baixa temperatura Ai
decaiu 16%, enquanto em baixa temperatura e deficiência hídrica decaiu 35%, ou seja, mais
que o dobro. Outro aspecto a considerar é que houve um aumento significativo de NPQ
durante o período de baixa temperatura e restrição hídrica na IACSP94-2094 I e NI (Figura
5A). Na IACSP95-5000, o NPQ foi semelhante durante todo o período experimental (Figura
5B). Segundo LAWLOR & TEZARA (2009), o NPQ é uma forma de dissipação de energia
muito frequente quando há excesso de energia não utilizada. Estes resultados sugerem que a
fotossíntese de ambas as cultivares foi sensível à baixa temperatura, porém a IACSP95-5000
com menor intensidade que a IACSP94-2094. Por outro lado, com a ocorrência simultânea de
baixa temperatura e deficiência hídrica, a IACSP95-5000 foi, possivelmente, mais sensível ao
efeito cumulativo de frio e seca. Interessante notar que RIBEIRO et al. (2013) observaram
que sob deficiência hídrica mais severa (ΨW6h = -1,8 MPa) a IACSP94-2094 apresentou as
menores quedas em A, quando comparada a outras cultivares, SP87-365 e IACSP96-2042.
Comparativamente, a cv. IACSP95-5000 apresentaram queda maior da razão A/Ci do que a
IACSP94-2094 (Figura 3C e D). MARTINS (2012) também sugeriu que a maior tolerância à
deficiência hídrica da IACSP94-2094 em relação a IACSP95-5000 estaria relacionada com a
maior fotoproteção indicada pelo NPQ e maior atividade e expressão de PEPcase.
A queda de A após 34 h de imposição dos tratamentos pode estar relacionada a fatores
difusivos, metabólicos e fotoquímicos (ALLEN & ORT, 2001; DU et al., 1996;
GHANNOUM et al., 2003; GHANNOUM, 2009; MACHADO et al., 2009, 2010). De fato,

65
no presente trabalho a queda em A foi devida tanto a fatores difusivos, relacionados à queda
de gs (Figura 2A e B), como metabólicos, queda na razão A/Ci (Figura 3C e D) e também
fotoquímico, queda em Fq'/Fm', (Figura 4) com consequente queda em ETR (Figura 6C e D).
DU et al. (1996) observaram em cana-de-açúcar sob deficiência hídrica moderada (ΨW6h = -
0,85 MPa), que o declínio da fotossíntese ocorreu devido, principalmente, a fatores
estomáticos. Sob deficiência hídrica mais severa (ΨW6h < -0,85 MPa), o declínio de A foi
devido, em parte, à queda de gs, acrescido por componentes metabólicos, sendo o fator
limitante a enzima PPDK. LOBO (2012) também relatou que a deficiência hídrica em cana-
de-açúcar promoveu decréscimos em gs e da atividade e expressão de Rubisco e PEPcase.
O efeito máximo da baixa temperatura sobre A ocorreu de forma rápida, ou seja, já nas
34 horas iniciais, visto que durante o resto do período experimental, até o 20º dia, o
incremento na queda de A foi negligível em ambas as cultivares. Como já foi descrito, na
IACSP94-2094 não ocorreu maior queda de A, mesmo com a adição do estresse hídrico
(Figura 1A).
Após o resfriamento, com o declínio de A, foi observado o fechamento estomático, que
pode ter ocorrido devido a um efeito direto do frio sobre as células-guarda ou ainda, uma
resposta indireta ao aumento de Ci, induzido pela diminuição da atividade de carboxilação
(ALLEN & ORT, 2001). De fato, Ci aumentou progressivamente enquanto A/Ci diminuiu em
ambas as cultivares (Figura 3). Além disso, pode ocorrer sinalização química causada pelo
frio e também pela deficiência hídrica o que poderia ainda causar o fechamento estomático
(LIANG & ZHANG, 1999; VESELOVA et al., 2005; ZHOU et al., 2007). No tratamento com
baixa temperatura, as respostas em ambas as cultivares foram semelhantes, porém mais
acentuadas na IACSP94-2094. Em relação ao efeito conjunto da baixa temperatura e
deficiência hídrica, os mesmos efeitos podem ter ocorrido acrescidos da queda do Ψw6h.
Entretanto, em nenhuma das cultivares ocorreu aumento da fotorrespiração devido aos
estresses, como pode ser verificado pela relação linear entre eficiência operacional (Fq'/Fm') e
eficiência quântica (CO2), dada por CO2 = -0,00312 + 0,09783*Fq’/Fm’ (R2=0,96, p<0,01)
(dados não apresentados). Esta relação indica a utilização de 10,2 fótons/CO2 fixado,
independente do tratamento.
Quando ambos os estresses ocorreram conjuntamente, com a queda de A também
ocorreu queda em gs evitando assim a desidratação. O aumento de Ci só ocorreu no período de
seca intermediária e máxima (respectivamente no 13o e 20º dias) (Figura 3A e B). O aumento
de Ci (Figura 3A e B) na IACSP94-2094 NI e na IACSP95-5000 NI coincide com o
decréscimo do Ψw6h (Tabela 1), sugerindo que o declínio de A pode também ter ocorrido

66
devido a fatores não estomáticos (DU et al., 1996; LOBO 2012), como foi sugerido pela
queda de A/Ci (Figura 3C e D).
Quando as plantas são expostas a estresses bióticos e abióticos, são frequentemente
observados decréscimos na eficiência quântica máxima do FSII (Fv/Fm) (BAKER, 2008).
Fv/Fm representa a eficiência máxima com que a luz absorvida pelo FSII é usada para a
redução da QA (BAKER, 2008). Neste experimento, ambas as cultivares apresentaram
decréscimo significativo de Fv/Fm após o resfriamento (Figura 5C e D), permanecendo baixo
durante todo o período de tratamento, porém somente a IACSP94-2094 I e NI apresentaram
valores abaixo de 0,725 caracterizando fotoinibição (CRITCHLEY, 1998). A alteração do
Fv/Fm pode ter ocorrido devido a mudança na eficiência da dissipação não-fotoquímica
(MAXWELL & JOHNSON, 2000). De fato, na IACSP94-2094 I e NI houve aumento de
NPQ acompanhado do decréscimo de Fv'/Fm' durante o período de tratamento (Figura 5A e
C).
A taxa de consumo de ATP e NADPH é um dos principais fatores que determinam a
eficiência operacional FSII (Fq'/Fm') em muitas situações. Alterações na eficiência de
carboxilação, na taxa de regeneração da ribulose 1,5-bisfosfato (RuBP), no fornecimento de
CO2 para os sítios de carboxilação via estômatos e na taxa de transporte de carboidratos para
fora da célula podem influenciar a taxa de utilização de ATP e NADPH e, consequentemente,
Fq'/Fm'. Muitos estresses ambientais alteram a assimilação de CO2, embora os locais da
limitação da fotossíntese possam ser muito variados. O estresse induz a redução da
condutância estomática, do metabolismo de carbono e do transporte, podendo diminuir a
eficiência do FSII. Aumentos de NADPH e ATP diminuem o fluxo linear de elétrons e a taxa
de oxidação de QA, que podem ser monitorados por diminuições no fator de eficiência do FSII
(Fq'/Fv'). No entanto, a acidificação do lúmen, bem como o aumento dos teores de ATP
também resultam num aumento do NPQ (Figura 5A, B) e uma diminuição do Fv'/Fm' (Figura
5C, D) (BAKER, 2008).
A assimilação de CO2 pelas folhas resulta em triose-P, da qual é sintetizada sacarose e
amido como produtos finais de duas rotas gliconeogênicas: a sacarose no citosol das células
do mesofilo e o amido nos cloroplastos da BFV em cana-de-açúcar (GROF & CAMPBELL,
2001; LUNN & FURBANK 1999). Durante o dia, a sacarose é continuamente exportada para
tecidos não fotossintetizantes da planta, enquanto o amido é acumulado nos cloroplastos. Os
teores de amido do cloroplasto são máximos durante o dia e mínimos a noite, quando é
degradado para síntese de sacarose, mantendo assim, sua exportação durante a noite. Em
condições adequadas, baixos teores de açúcar estimulam a fotossíntese (McCORMICK et al.,

67
2006; LOBO, 2012), a mobilização de reservas e a exportação, enquanto a alta concentração
de açúcar promove o crescimento e o armazenamento de carboidratos (SMITH & STITT,
2007; SOUZA, 2011; TAIZ & ZEIGER, 2009).
Em folhas de cana-de-açúcar, sob condições normais de crescimento, a glicose e a
frutose apresentam a maior concentração às 10 h, enquanto o conteúdo de sacarose começa a
aumentar às 10h, atingindo valores máximos entre 13 e 16 h e o declínio da sacarose ocorre
após as 19 h. A concentração de amido começa a aumentar a partir das 10 h e tem um pico
máximo às 16 h. A partir das 19 h, 90% do amido produzido na folha são então consumidos
no período noturno (SOUZA, 2011).
Neste experimento, durante o período de estresse, as folhas para análises bioquímicas
foram coletadas às 9 h e foi observado aumento no teor de AS (composto principalmente por
glicose + frutose + sacarose) em ambas as cultivares (Figura 7A, B, C e D). Na IACSP95-
5000 I e NI este aumento ocorreu após 34 h de frio, enquanto na IACSP94-2094 I e NI o
aumento de AS ocorreu no período de máximo estresse. Houve acúmulo de SAC nas folhas na
IACSP94-2094 NI no período de estresse máximo. Este aumento provavelmente está
relacionado com a alta atividade da SPS (Figura 7C e 8C). No trabalho apresentado no
capítulo II, também foi observado aumento da concentração de SAC nas plantas expostas à
baixa temperatura noturna e deficiência hídrica (Tabela 2, Capítulo II).
Em ambas as cultivares, independente do status hídrico, foi observado aumento da
concentração de AMI foliar, porém este aumento foi bem maior na IACSP94-2094,
independente do regime hídrico, em relação à testemunha. MACHADO (2009) também
observou em citros, após o tratamento com baixa temperatura noturna, que houve aumento na
concentração de AMI, provavelmente devido à inibição de enzimas de mobilização do amido,
ou ainda, a queda no crescimento, diminuindo assim a demanda (ALLEN & ORT, 2001). O
acúmulo de carboidratos nas folhas após a imposição dos tratamentos, também observado por
LOBO (2012), pode ser devido à baixa demanda de carboidratos. Ou seja, é possível que a
queda no crescimento das plantas, que tem temperatura ideal em 35 °C (EBRAHIM et al.,
1998; SALES et al., 2012), tenha sido mais afetada do que a queda em A, e portanto,
decorrente disto, ocorreu acúmulo de reservas. Esta formação de reserva pode ser
remobilizada para suprir o substrato necessário ao crescimento rápido, quando o ambiente se
tornar favorável (PEARCE, 1999; POLLOCK & JONES, 1979).
Na rota de síntese de sacarose, a enzima chave é a SPS, exercendo alto controle em
altas taxas fotossintéticas e, portanto, também sobre o fluxo máximo de síntese (HUBER &
HUBER, 1996). Foi observado que em plantas sob baixas temperaturas houve aumento da

68
atividade da SPS e da SuSy em folhas de espinafre (GUY et al., 1992), ou ainda, aumento no
estado de ativação da enzima em folhas de cana-de-açúcar de cultivar tolerante (DU & NOSE,
2002). Entretanto, sob deficiência hídrica severa, DU et al. (1998) observaram que a atividade
enzimática relacionada com a síntese de sacarose e amido diminuíram, porém em menor
proporção que as trocas gasosas, indicando baixa possibilidade dos componentes da rota da
sacarose e amido como fatores limitantes das trocas gasosas.
No presente experimento houve respostas diferenciadas entre cultivares (Figura 8).
Houve aumento da atividade da SPS em IACSP94-2094 I e NI durante o período de
tratamento, sendo que no período de máximo estresse a atividade da SPS foi maior nas plantas
NI. O aumento da SPS indica mudança nas propriedades regulatórias da enzima
(BASCUÑÁN-GODOY et al., 2006). Além disso, sob baixas temperaturas, o aumento da
atividade da SPS associado ao acúmulo de SAC sugerem que a resposta não é simplesmente
de ajuste deste processo metabólico para superar a cinética enzimática lenta em baixas
temperaturas, mas provavelmente, um processo adaptativo para maximizar a síntese do
composto com propriedades osmóticas importantes na tolerância a esse estresse (GUY, et al.,
1992).
A utilização da sacarose como fonte de energia depende de sua quebra, gerando
hexoses, e nas plantas duas enzimas catalisam esta reação: a SuSy, gerando FRU + UDP-
glicose, ou as invertases gerando GLU + FRU, que regulam a entrada da sacarose em
diferentes rotas de utilização (STURM, 1999), incluindo o carregamento de carboidratos no
complexo cc-ec para exportação da sacarose (LALONDE et al., 2003: RAE et al., 2005;
SMITH & STITT, 2007). Em plantas de cana-de-açúcar, mudanças na atividade do dreno
podem promover ajustes nas taxas de descarregamento pelo floema (LALONDE et al., 2003)
promovendo a manutenção de um gradiente de exportação de sacarose.
A atividade da SuSy (Figura 8A e B) aumentou na IACSP94-2094 com a baixa
temperatura (no máximo estresse) e com a deficiência hídrica (no estresse intermediário). Na
IACSP95-5000 NI houve aumento significativo da atividade da SuSy no estresse
intermediário. VANDOORME et al. (2012) observaram em plantas de chicória, que a
deficiência hídrica não influenciou significativamente a atividade da SuSy, indicando a
utilização de seus produtos em processos anabólicos.
Durante o período de estresse, a atividade da IVA decresceu na IACSP94-2094 I e NI,
enquanto em ambas as cultivares nas plantas I houve aumento da IVN e nas plantas NI
decréscimo, indicando sensibilidade da IVN aos estresses impostos de forma simultânea
(Figura 9). Em decorrência do aumento da atividade das invertases, houve um aumento do

69
teor de AS (Figura 7A, B). Decréscimo de IVA foi observado por FU et al. (2010) em uma
espécie de gramínea sob deficiência hídrica, sugerindo que a alta concentração de sacarose
seja uma consequência do aumento da atividades das enzimas SPS e SuSy e declínio da IVA.
Na IACSP95-5000 o aumento da atividade da IVN nas plantas I pode ter contribuído
para a menor queda de A em relação às plantas NI, devido ao aumento no teor de hexoses, que
pode incrementar o potencial osmótico (Figura 1B, 7B e 9D).
Período de recuperação
Após o estresse máximo, as plantas foram reidratadas e retornaram à temperatura de
32/20 °C. Dois dias depois ocorreu aumento súbito de A e Ai em ambas as cultivares,
atingindo valores semelhantes aos da testemunha (Figura 1). Esta recuperação no 2º dia está
relacionada com a recuperação de gs, Ci, A/Ci, Fq'/Fm' e ETR, a valores semelhantes à
testemunha, antes do estresse (Figuras 1, 2, 3, 4 e 6).
É interessante notar que A e Ai em IACSP95-5000 que foi submetida à baixa
temperatura continuou a aumentar até o 8º dia de recuperação e superaram em 45% e 30%,
respectivamente, aos valores de A e Ai da testemunha (Figura 1B, D). Esta resposta está
relacionada com o aumento de 79% em gs (Figura 2B), o que deve proporcionar aumento do
fluxo de CO2 aumentando o Ci em 40% (Figura 3B). Também pode estar relacionado com o
aumento de 15 e 25%, respectivamente, em Fq'/Fm' e ETR, em relação ao 2º dia de
recuperação (Figuras 4B e 6D). No tratamento de baixa temperatura combinado com a
deficiência hídrica, o aumento de A e Ai maior do que a testemunha não ocorreu, apesar de ter
ocorrido em gs e Ci. Porém, A/Ci permaneceu menor que a testemunha (Figura 3D), sugerindo
efeito residual da deficiência hídrica sobre o metabolismo fotossintético, como também foi
observado por DU et al. (1996).
As plantas quando retornaram às condições ideais durante a recuperação,
possivelmente tiveram aumento no crescimento, demandando mais fotoassimilados. A taxa
máxima de crescimento da cana-de-açúcar ocorre entre 25 e 35 °C e quando expostas à
temperatura de 15 °C já se observa inibição do crescimento vegetativo (EBRAHIM et al.,
1998; SALES et al., 2012). Concomitantemente ao aumento de A, ocorreu queda significativa
no teor dos demais carboidratos no tecido foliar (Figura 7), principalmente na IACSP95-5000.
Assim, sugere-se que o aumento súbito de A em relação à testemunha durante a recuperação
da IACSP95-5000 I seja causado pela ação combinada dos aumentos em gs, A/Ci, Fq'/Fm' e da
queda acentuada nos teores de carboidratos, possivelmente causado pelo fluxo de sacarose ao

70
floema (McCORMICK et al., 2008; LOBO, 2012). LOBO (2012) observou que a maior
concentração de sacarose, frutose ou glicose causa queda acentuada na assimilação de CO2 e
no ETR. Os processos de inibição ou estímulo da fotossíntese estão relacionados com o
consumo de intermediários nos drenos (McCORMICK et al., 2006; 2008; 2009) prevenindo a
falta ou o acúmulo de metabólitos. Na recuperação também houve mudança geral nas
atividades de enzimas relacionadas ao metabolismo de carboidratos, bem como de seus teores
nas folhas. Os teores de carboidratos (AS, SAC e AMI) em todos os tratamentos, exceto na
IACSP94-2094 I, decresceram significativamente durante a recuperação em relação ao
máximo estresse. Este tipo de resposta sugere que ocorreu grande exportação da fonte em
direção aos drenos em crescimento ativo. Ao mesmo tempo, as atividades de SPS e SuSy
decresceram, enquanto as atividades das invertases aumentaram do 2º para 8º dia de
recuperação. Alta atividade de invertases indica alta taxa de catabolismo.
5 CONCLUSÕES
1. Sob condições ideais, a cv. IACSP95-5000 tem maior fotossíntese que a cv. IACSP94-2094
devido à maior condutância estomática e à eficiência aparente de carboxilação.
2. A cv. IACSP95-5000 é mais tolerante à baixa temperatura e apresenta maior capacidade de
recuperação da fotossíntese após a sua ocorrência.
4. Sob a ocorrência conjunta de frio e deficiência hídrica, a cv. IACSP94-2094 é mais
tolerante do que a cv. IACSP95-5000.
5. O declínio da assimilação de CO2 em ambas as cultivares, em consequência da ocorrência
de frio e/ou deficiência hídrica é devido a fatores difusivos, metabólicos e fotoquímicos.
6. O alto teor de açúcares solúveis totais nas folhas da cv. IACSP94-2094 NI no período de
estresse máximo é devido, principalmente, ao aumento no teor de sacarose, quando há
também aumento da atividade da sintase de sacarose fosfato.
7. O alto teor de açúcares solúveis totais nas folhas da cv. IACSP94-2094 I no período de
estresse é devido, principalmente, à hidrólise do amido. Neste mesmo período ocorre também
aumento da atividade das invertases neutras.

71
6 REFERÊNCIAS BIBLIOGRÁFICAS
ALLEN, D.J.; ORT, D.R. Impacts of chilling temperatures on photosynthesis in warm-
climate plants. Trends in Plant Science, London, v. 6, p. 36-42, 2001.
AMARAL, L.I.V.; GASPAR, M.; COSTA, P.M.F.; AIDAR, M.P.M.; BUCKERIDGE, M.S.
Novo método enzimático rápido e sensível de extração e dosagem de amido em materiais
vegetais. Hoehnea, São Paulo, v. 34, p. 425-431, 2007.
ASHRAF, M.; FOOLAD, M.R. Roles of glycine betaine and proline in improving plant
abiotic stress resistance. Environmental and Experimental Botany, Oxford, v. 59, p. 206-
216, 2007.
BAKER, N.R. A probe of photosynthesis: in vivo. Annual Review of Plant Biology, Palo
Alto, v. 59, p.89–113, 2008.
BIELESKI, R.L.; TURNER, A. Separation and estimation of amino acids in crude plant
extracts by thin-layer electrophoresis and chromatography. Analytical biochemistry,
Amsterdam, v. 17, p. 278-293, 1966.
BASCUÑÁN-GODOY, L.; URIBE, E.; ZÚÑIGA-FEEST, A.; CORCUERA, L.J.; BRAVO,
L.A. Low temperature regulates sucrose-phosphate activity in Colobanthus quitensis (Kunth)
Bartl. by decreasing its sensitivity to Pi and increased activation by glucose-6-phosphate.
Polar Biology, New York, v. 29, p. 1011-1017, 2006.
BRADFORD, M.N. A rapid and sensitive method for the quantitation of microgram
quantities of protein utilizing the principle of protein-dye binding. Analytical Biochemistry,
Amsterdan, v. 72, p. 248-254, 1976.
CRITCHLEY, C. Photoinhibition. In: RAGHAVENDRA, A.S. Photosynthesis: a
comprehensive treatise. Cambridge: Cambridge University Press. 1998. chap. 20, p. 264-
272.
DU, Y.C.; KAWAMITSU, Y.; NOSE, A. ; HIYANE, S.; MURAYAMA, S.; WASANO, K.;
UCHIDA, Y. Effects of water stress on carbon exchange rate and activities of photosynthetic
enzymes in leaves of sugarcane (Saccharum sp.). Functional Plant Biology, Victoria, v.23,
p.719-726, 1996.
DU, Y.C.; NOSE, A.; WASANO, K.; UCHIDA, Y. Responses to water stress of enzyme
activities and metabolite levels in relation to sucrose and starch synthesis, the Calvin cycle
and the C4 pathways in sugarcane (Saccharum sp.) leaves. Australian Journal of Plant
Physiology, Melbourne, v. 25, p. 253-260, 1998.
DU, Y.C.; NOSE, A. Effects of chilling temperature on the activity of enzimes of sucrose
synthesis and the accumulation of saccharides in leaves of three sugarcane cultivars differing
in cold sensitivity. Photosynthetica, Praga, v.40, p. 389-395, 2002.

72
DUBOIS, M.; GILLES, K.A.; HAMILTON, J.K.; REBERS, P.A.; SMITH, F. Colorimetric
method for determination of sugars and related substances. Analytical Chemistry,
Washington, v. 28, n.30, p. 350-356, 1956.
EBRAHIM, M.K.H.; VOGG, G.; OSMAN, M.N.E.H; KOMOR, E. Photosynthetic
performance and adaptation of sugarcane at suboptimal temperatures. Journal of Plant
Physiology, Melbourne, v.153, p.587-592, 1998.
FU, J.; HUANG, B.; FRY, J. Osmotic potencial, sucrose level, and activity of sucrose
metabolic enzymes in tall fescue in response to deficit irrigation. Journal of American
Society for Horticultural Science, Alexandria, v. 135, p. 506-510, 2010.
GHANNOUM, O.; CONROY, J.P.; DRISCOLL, S.P.; PAUL, M.J.; FOYER, C.H.;
LAWLOR, D.W. Nonstomatal limitations are responsible for drought-induced photosynthetic
inhibition in four C4 grasses. New Phytologist, Oxford, v.159, p.599-608, 2003.
GHANNOUM, O. C4 photosynthesis and water stress. Annals of Botany, Oxford, v.103,
p.635-644, 2009.
GROF, C.P.L.; CAMPBELL, J.A. Sugarcane sucrose metabolism: scope for molecular
manipulation. Australian Journal of Plant Physiology, Melbourne, v. 28, p. 1-12, 2001.
GUY, C.L.; HUBER, J.L.A.; HUBER, S.C. Sucrose phosphate synthase and sucrose
accumulation at low temperature. Plant Physiology, Rockville, v. 100, p. 502-508, 1992.
HUBER, S.C.; HUBER, J.L. Role and regulation of sucrose-phosohate synthase in higher
plants. Annual Review of Plant Physiology and Plant Molecular Biology, Palo Alto, v. 47,
p. 431-444, 1996.
JAVIER, P.J.; JOSÉ, I.J.; MANUEL, S.D. Chilling of drought-hardened and non-hardened
plants of different chilling-sensitive maize lines. Changes in water relations and ABA
contents . Plant Science, Hoboken, v.112, p. 71- 79, 1997.
KOCH, K. Sucrose metabolism: regulatory mechanisms and pivotal roles in sugar sensing and
plant development. Current Opinion in Plant Biology, London, v. 7, p. 235-246, 2004.
LALONDE, L.; TEGEDER, M.; THRONE-HOLST, M.; FROMMER, W. B. PATRICK, J.
W.. Phloem loading and unloading of sugars and amino acids. Plant, Cell and Environment,
Oxford, 26, 37–56, 2003.
LANDELL, M.G.A.; CAMPANA, M.P.; FIGUEIREDO, P.; VASCONCELOS, A.C.M;
XAVIER, M.A.; BIDOIA, M.A.P.; PRADO, H.; SILVA, M.A.; DINARDO-MIRANDA,
L.L.; SANTOS, A.S.; PERECIN, D.; ROSSETTO, R.; SILVA, D.N.; MARTINS, A.L.M;
GALLO, P.B.; KANTACK, R.A.D.; AZANIA, C.A.A.M.; PINTO, L.R.; SOUZA, S.A.C.D.
Variedades de cana-de-açúcar para o Centro-Sul do Brasil. Campinas: IAC, 2004. 32p.
(Boletim técnico IAC 195 – 14ª Liberação do Programa Cana IAC).
LANDELL, M.G.A.; CAMPANA, M.P.; FIGUEIREDO, P.; VASCONCELOS, A.C.M;
XAVIER, M.A.; BIDOIA, M.A.P.; PRADO, H.; SILVA, M.A.; DINARDO-MIRANDA,

73
L.L.; SANTOS, A.S.; PERECIN, D.; ROSSETTO, R.; SILVA, D.N.; MARTINS, A.L.M;
GALLO, P.B.; KANTACK, R.A.D.; CAVICHIOLI, J.C.; VEIGA FILHO, A.A.; ANJOS,
I.A; AZANIA, C.A.M.; PINTO, L.R.; SOUZA, S.A.C.D. Variedades de cana-de-açúcar
para o Centro-Sul do Brasil. Campinas, IAC, 2005, 33p. [15° liberação do Programa Cana
IAC (1959-2005)].
LAWLOR, D. W.; TEZARA, W. Causes of decreased photosynthetic rate and metabolic
capacity in water-deficient leaf cells: a critical evaluation of mechanisms and integration of
processes. Annals of Botany, Oxford, v. 103, p.561–579, 2009.
LIANG, J.; ZHANG, J. The relations of stomatal closure and reopening to xylem ABA
concentration and leaf water potential during soil drying and rewatering. Plant Growth
Regulation, Dordrecht, v. 29, p. 77-86, 1999.
LOBO, A.K.M. Modulação da fotossíntese por açúcares e deficiência hídrica em plantas
de cana-de-açúcar. 2012. 106p. Dissertação (Mestrado em Bioquímica) - Universidade
Federal do Ceará, Fortaleza.
LUNN, J.E.; FURBANK, R.T. Sucrose biosynthesis in C4 plants. New Phytologist, Oxford,
v. 143, p. 221-237, 1999.
MACHADO, D.F.S.P.; MACHADO, E.C.; MACHADO, R.S.; RIBEIRO, R.V. Efeito da
baixa temperatura noturna e do porta-enxerto na variação diurna das trocas gasosas e na
atividade fotoquímica de laranjeira 'Valência'. Revista Brasileira de Fruticultura,
Jaboticabal, v. 32, p. 351-359, 2010.
MACHADO, R. S. Respostas fisiológicas de genótipos de cana-de-açúcar ao déficit
hídrico imposto na fase inicial de desenvolvimento. 2009. 64p. Dissertação (Mestrado em
Agricultura Tropical e Subtropical) – Pós-Graduação – IAC.
MACHADO, R.S.; RIBEIRO, R.V.; MARCHIORI, P.E.R.; MACHADO, D.F.S.P.;
MACHADO, E.C.; LANDELL, M.G.A. Respostas biométricas e fisiológicas ao déficit
hídrico em cana-de-açúcar em diferentes fases fenológicas. Pesquisa Agropecuária
Brasileira, Brasília, v. 44, p. 1575-1582, 2009.
MARTINS, M.O. Regulação da fotossíntese por deficiência hídrica, nitrogênio e CO2
elevado em cana-de-açúcar. 2012. 96p. Tese (Doutorado em Bioquímica) - Universidade
Federal do Ceára, Fortaleza.
MAXWELL, K.; JOHNSON, G.N. Chlorophyll fluorescence - a practical guide. Journal of
Experimental Botany, Oxford, v. 51, p. 659-668, 2000.
McCORMICK, A.J.; CRAMER, M.D.; WATT, D.A. Sink strength regulates photosynthesis
in sugarcane. New Phytologist, Oxford, v. 171, p. 759-770, 2006.
McCORMICK, A.J.; CRAMER, M.D.; WATT, D.A. Changes in photosynthetic rates and
gene expression of leaves during a source-sink perturbation in sugarcane. Annals of Botany,
Oxford, v. 101, p. 89-102, 2008.

74
McCORNINCK, A.J.; WATT, D.A.; CRAMER, M.D. Supply demand: sink regulation of
sugar accumulation in sugarcane. Journal of Experimental Botany, Oxford, v. 60, p. 357-
364, 2009.
MOORE, P.H. Integration of sucrose accumulation processes across hierarchical scales:
towards developing an understanding of the gene-to-crop continuum. Fields Crops Research,
Amsterdan, v.92, p. 119-135, 2005.
NELSON, N. A photometric adaptation of the Somogyi method for the determination of
glucose. Journal of Biological Chemistry, Bethesda, v. 153, p. 375-380, 1944.
PEARCE, R. Molecular analysis of acclimation to cold. Plant Growth Regulation,
Dordrecht, v. 29, p. 47-76, 1999.
POLLOCK, C.J.; JONES, T. Seasonal patterns of fructan metabolism in forage grasses. New
Phytologist, Oxford, v. 83, p. 8-15, 1979.
RAE, A.L.; GROF, C.P.L.; CASU, R.E.; BONNETT, G.D. Sucrose accumulation in the
sugarcane stem: pathways and control points for transport and compartmentation. Field
Crops Research, Amsterdam, v. 92, p. 159-168, 2005
RIBEIRO, R.V.; MACHADO, R.S.; MACHADO, E.C.; MACHADO, D.F.S.P.;
MAGALHÃES FILHO, J.R.; LANDELL, M.G.A. Revealing drought-resistance and
productive patterns in sugarcane genotypes by evaluating both physiological responses and
stalk yield. Experimental Agriculture, Cambridge, v.49, p. 212-224, 2013.
SALERNO, G.L.; CURATTI, L. Origin of sucrose metabolism in higher plants: when, how
and why? Trends in Plant Science, London, v. 8, p. 63-69, 2003.
SALES, C.R.G.; RIBEIRO, R.V.; MACHADO, D.F.S.P.; MACHADO, R.S.; DOVIS, V.L.;
LAGÔA, A.M.M.A. Trocas gasosas e balanço de carboidratos em plantas de cana-de-açúcar
sob condições de estresses radiculares. Bragantia, Campinas, v.71, p.319-327, 2012.
SMITH, A.M.; STITT, M. Coordination of carbon supply and plant growth. Plant, Cell and
Environmental, Oxford, v. 30, p. 1126-1149, 2007.
SOMOGYI, M. A new reagent for the determination of sugars. Journal of Biological
Chemistry, Bethesda, v. 160, p. 61-68, 1945.
SOMOGYI, M. Notes on sugar determination. Journal of Biological Chemistry, Bethesda,
v. 195, p. 19-23, 1952.
SOUZA, A.P. Mecanismos fotossintéticos e relação fonte-dreno em cana-de-açúcar
cultivada em atmosfera enriquecida em CO2. 208p. 2011. Tese (Doutorado em Ciências) -
Instituto de Biociências - Universidade de São Paulo - São Paulo.
STURM, A. TANG, G.Q. The sucrose-cleaving enzymes of plants are crucial for
development, growth and carbon partitioning. Trends in Plant Science, London, v. 4, p. 401-
407, 1999.

75
TAIZ, L.; ZEIGER, E. Fisiologia vegetal. 4 ed. Porto Alegre: Artmed. 2009. 819 p.
VANDOORME, B.; MATHIEU, A.-S.; VAN DEN ENDE, W; VERGAUWEN, R.;
PÉRILLEUX, C.; JAVAUX, M.; LUTTS, S. Water stress drastically reduces root growth and
inulin yield in Chichorium intybus (var. sativum) independently of photosynthesis. Journal of
Experimental Botany, Oxford, v.63, p.4359-4373, 2012.
VAN HANDEL, E. Direct microdetermination of sucrose. Analytical Biochemistry,
Amsterdam, v. 22, p. 280-283, 1968.
VESELOVA, S.V.; FARHUTDINOV, R.G.; VESELOV, S.Y.; KUDOYAROVA, G.R.;
VESELOV, D.S.; HARTUNG, W. The effect of root cooling on hormone content, leaf
conductance and root hydraulic conductivity of durum wheat seedlings (Triticum durum L.).
Journal of Plant Physiology, Londrina, v.162, p.21-16, 2005.
WANG, W.; VINOCUR, B.; ALTMAN, A. Plant responses to drought, salinity and extreme
temperatures: towards genetic engineering for stress tolerance. Planta, Berlin, v. 218, p. 1-14,
2003.
YORDANOV, I.; VELIKOVA, V.; TSONEV, T. Plant responses to drought, acclimation, and
stress tolerance. Photosynthetica, Praga, v. 38, p. 171-186, 2000.
ZHANG, S.; LI, Q.; MA, K.; CHEN, L. Temperature-dependent gas exchange and
stomatal/non-stomatal limitation to CO2 assimilation of Quercus liaotungensis under midday
high irradiance. Photosynthetica, Praga, v.39, p.383-388, 2001.
ZHOU, Y.; HUANG, L.; ZHANG, Y, SHI, K.; YU, J.; NOGUÉS, S. Chill-induced decrease
in capacity of RuBP carboxylation and associated H2O2 accumulation in cucumber leaves are
alleviated by grafting onto figleaf gourd. Annals of Botany, Oxford, v. 100, p. 839-848,
2007.
ZHU, Y.J.; KOMOR, E.; MOORE, P.H. Sucrose accumulation in the sugarcane stem is
regulated by the difference between the activities of soluble acid invertase and sucrose
phosphate synthase. Plant Physiology, Rockville, v. 115, p. 609-616, 1997.