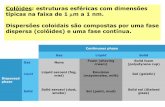
Colóides
description
Transcript of Colóides

Tecnologia em Miniatura
A nanotecnologia pode colocar milhares de
rádios em um único fio de cabelo

• Inventado no fim do século XIX, o rádio populariza-se depois da Primeira Guerra Mundial;

• O desenvolvimento dos transistor aposenta as válvulas e permite o surgimento do “radinho de pilha” portátil.

• Chips receptores e transmissores de rádio fazem funcionar telefones celulares, brinquedos e outros eletrônicos sem fio.

• O nanorrádio. Pesquisadores da Universidade de Berkeley ( Estados Unidos) construíram um rádio com um tubo de carbono com 1 micrometro de comprimento e 10 nanômetros de espessura. ( 10 mil vezes mais fino que uma folha de papel).


As soluções coloidais, são, em geral,turvas e frequentemente esbranquiçadas.

• O Leite ( 85% de água)
• A maionese( gotículas de óleo no vinagre)
• A gelatina ( rica em proteínas)

• O látex ( produção de luvas e acessórios hospitalares)
• O plasma sanguíneo ( recuperação de paciente debilitados)
• A goma-arábica ( cola, na industria farmacêutica, de alimentos, entre outros.)


• Manteiga
• Creme chantili
• Água de coco
• Creme dental
• Creme de barbear

• Sabonete
• Xampus
• Filmes fotográficos
• Cosméticos
• Tintas
• Vernizes, etc.

1860 Thomas Graham Observou:
• Difundem-se na água muito lentamente;• Quando em solução aquosa, não
atravessam certas membranas;• Não apresentam tendência de se
cristalizar;
A partir dessas observações, essas substâncias foram chamadas de Colóides.

Sistema Coloidal

• Solução coloidal é uma dispersão na qual as partículas dispersas têm um tamanho médio entre 1 e 1000 nanômetros ( nm)

Dispersibilidade das Partículas Coloidais
• A) Colóide reversível, liófilo ou liofílico
( quando o dispersante é a água)
Se dispersa espontaneamente no dispersante
Gelatina
Detergente

• Gelatina sólida ( gel)
• Gelatina líquida ( sol)

• B) colóide irreversível, liófobo ou liofóbico
Não se dispersa espontaneamente no dispersante.
Metais, bases, sais etc.
( partículas fragmentadas até atingir o tamanho coloidal)
Depósito de enxofre – Vulcão Tacorá

Preparo dos Colóides
• Fragmentação( partículas maiores são fragmentadas)
Moinho coloidal
Arco elétrico ( Método de Bredig)
Ultrassom

• Aglomeração ( ou condensação)
Partículas menores são aglomeradas até atingir o tamanho coloidal
Mudança de Solvente = creolina
Reações químicas = formação de precipitado

Propriedades dos Coloides
Tamanho das Partículas
• Sedimentação as partículas não se sedimentam
espontaneamente);
separação muito lenta;
Ultracentrífugas

Separação dos componentes do sangue.

• FiltraçãoAtravessam filtros comuns de laboratório;
Retidos em ultrafiltros;

• Movimento browniano ( Robert Brown)Movimento constante, perpétuo e em
ziguezague

Farol em noite com neblina;
Luz se dispersa em todas as direções quando encontra as gotículas de água;

A purificação dos coloides e a hemodiálise
• O processo de purificação dos colóides é a chamada diálise.
1. A solução é colocada dentro de uma membrana permeável;

2. Como as partículas coloidais não saem através da membrana, elas são lavadas de suas impurezas;

3. O fluxo contínuo do líquido carrega as impurezas para fora da membrana permeável.

Por que a Hemodiálise?


• Diálise Peritoneal


Algumas Propriedades• O material na forma de pó muito fino tem
propriedades diferentes das propriedades do mesmo material em pedaços ou blocos.
Alumínio em pó

Um objeto de ouro e uma solução de ouro coloidal

• Carvão ativado ( filtros de água para reter impurezas);
• Argilas (plástico, papel = mais resistência)
• Metais, óxidos metálicos ( catalizadores)

Ação do Catalisador

Fenômenos de Superfície
• O material finamente dividido = grande área superficial
• Na superfície das partículas surgem forças especiais que não podem ser notadas no bloco.

a) Área superficial das partículasCubo de ferro 1cm de aresta = 7,8g
Cortado ao meio = 2cm2 = 8cm2
Um novo corte = 4 novas faces = 10cm2
Após 1 bilhão de cortes, os 7,8g de ferro terão uma área aproximada de 50 campos de futebol.

b) Forças de superfícieUm átomo no interior tem suas
forças de coesão e repulsão equilibradas;
Um átomo que está na superfície do reticulado interage com o meio externo.

• Absorção:
Retenção de um material no interior dos poros;
Ex. uma esponja absorve o volume de água = o seu volume;
• Adsorção:
Retenção de um material na superfície de outro material;
Ex. Hidrogênio na platina em pó.

• Absorção

• Adsorção seletiva de íons:
Adsorve íons positivos ou negativos;
Diminui a tendência de aglomeração;
Colóide é mais estável;

Adsorção do dispersante:Formação de uma película de moléculas em torno da partícula coloidal ( camada de solvatação), evita aglomeração e precipitação.

Lavar roupa ( gotículas de gordura se dispersam na água;
A bile, no intestino, solubilizam gorduras
( digestão e absorção pelo organismo)

A maionese, gotículas de óleo se dispersam no vinagre

Precipitação dos Colóides
• Neutralização das cargas elétricas das partículas; ( suco de laranja no leite)
Partículas coloidais positivas e eletrólitos com íons negativos

• Eliminação da camada de solvatação
Mudança do solvente
Verniz ( goma arábica + álcool) despejado na água = turvação;

Muitas argilas, ao serem carregadas pelos rios, coagulam-se e precipitam quando a água doce encontra o sal do mar; nos deltas dos rios, muitas ilhas se formam ( demora milênios)
Ilha de MarajóIlhas do Delta do rio
Nilo

O ar de cidades grandes e industrializadas fica frequentemente poluído ( fumaça coloidal)
São Paulo , Capital