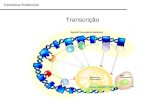
Polaridade das Ligações, Geometria Molecular e Força Molecular
Apresentação das principais estratégias de biologia molecular...
Transcript of Apresentação das principais estratégias de biologia molecular...
-
Principais estratégias de biologia molecular para viabilizar o emprego de biomoléculas oriundas de
micro-organismos extremófilos como biofármacos, bem como para o aprimoramento dessas
biomoléculas
Profa Dra Gisele Monteiro
FBT/FCF/USP
UNIVERSIDADE DE SÃO PAULO
Faculdade de Ciências Farmacêuticas
-
Quando usar organismo geneticamente modificado?
• MO patogênicos
• Fonte rara ou perigosa
• Rendimento baixo no MO original
• Difícil condição de crescimento e produção
• Produto tóxico para o MO original quando em altas concentrações
• Plantas de produção já estabelecidas
• Potencial de criar moléculas que não existiriam na natureza –
biobetters.
-
Expressão de proteínas antigênicas do vírus da
hepatite B – produção de vacina em levedura
U$10/dose
U$0,23/dose
Esquema: Watson et al., 1998. Recombinant DNA, 2nd edition, Scientific American Books
-
Quando usar organismo geneticamente modificado?
•MO patogênicos
•Fonte rara ou perigosa
•Rendimento baixo no MO original
•Difícil condição de crescimento e produção
•Produto tóxico para o MO original quando em altas concentrações
•Plantas de produção já estabelecidas
•Potencial de criar moléculas que não existiriam na natureza –
biobetters.
-
Enzimas e medicamentos
-
Quando usar organismo geneticamente modificado?
•MO patogênicos
•Fonte rara ou perigosa
•Rendimento baixo no MO original
•Difícil condição de crescimento e produção
•Produto tóxico para o MO original quando em altas concentrações
•Plantas de produção já estabelecidas
•Potencial de criar moléculas que não existiriam na natureza –
biobetters.
-
Preciso usar OGMs - estratégias
• Escolher a fonte do material genético
• Escolher a célula hospedeira
• Escolher o tipo de transformação
– Seleção x estabilidade x quantidade
-
Figure 8-43 Molecular Biology of the Cell (© Garland Science 2008)
Transcriptase reversa
-
Ligação de fatores de transcrição
3 5
5 3
Fita codificadora
Fita molde
Ligação da RNA polimerase
Início da transcrição
5 3
+1 = sítio de início da transcrição
Região 5 não traduzida
ATG = início da ORF
Fim da ORF = códon de
terminação
Região 3 não traduzida, sítio do término da
transcrição
5 3
3 5
3 5
-
Preciso usar OGMs - estratégias
• Escolher a fonte do material genético
• Escolher a célula hospedeira
• Escolher o tipo de transformação
– Seleção x estabilidade x quantidade
-
Produção de insulina humana em E. coli
-
Eritropoietina (EPO)
-
Leveduras geneticamente modificadas para produzir padrão de glicosilação humanizado.
-
Preciso usar OGMs - estratégias
• Escolher a fonte do material genético
• Escolher a célula hospedeira
• Escolher o tipo de transformação
– Seleção x estabilidade x quantidade
-
Transformação
• Plasmídeo epissomal – Muitas cópias por célula
– Exige seleção constante
– Marcas de seleção – antibióticos (aspectos regulatórios)
• Integrativo no DNA genômico – Estável
– Uma ou poucas cópias
– Seleção apenas 1 vez
– Integrar em locais que diminuem a produtividade
-
Principais estratégias de biologia molecular para o desenvolvimento de biobetters
-
Qual objetivo de bioprospecções?
-
Figure 7-1 Molecular Biology of the Cell (© Garland Science 2008)
-
Ex. Asparaginases
-
Ex. Asparaginases: asnA x asnB
-
Asparaginases tipo II
-
Mutação racional
Patel et al, 2009. J. Clin. Invest. 119:1964–1973 (2009). doi:10.1172/JCI37977
-
N24*
Patel et al, 2009. J. Clin. Invest. 119:1964–1973 (2009). doi:10.1172/JCI37977
Maggi ey al., 2017. SREP7: 14479 | DOI:10.1038/s41598-017-15075-4
-
Mutações randômicas - epPCR
-
Atividade no soro - teste in vivo
Mutante A mutante B Mutante A mutante B
-
Formação de anticorpos anti-ASNase
*
* * *
-
Obrigada!!!