5. MOLÉCULAS NA TROPOSFERA 5.1. LIGAÇÃO COVALENTE EM MOLÉCULAS DIATÓMICAS Escola Secundária...
Transcript of 5. MOLÉCULAS NA TROPOSFERA 5.1. LIGAÇÃO COVALENTE EM MOLÉCULAS DIATÓMICAS Escola Secundária...

5. MOLÉCULAS NA TROPOSFERA
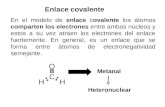
5.1. LIGAÇÃO COVALENTE EM MOLÉCULAS DIATÓMICAS
Escola Secundária Maria Lamas – Torres NovasFísica e Química A – 10º AnoNelson Alves Correia
UNIDADE 2 – NA ATMOSFERA DA TERRA: RADIAÇÃO, MATÉRIA E ESTRUTURA

OBJECTIVOS
• Indicar o significado da sigla CFC, identificando os respectivos compostos pelo nome e fórmula, como derivados do metano e do etano.
• Aplicar a nomenclatura IUPAC a alguns alcanos e seus derivados halogenados.

FORMAÇÃO E DECOMPOSIÇÃO DO OZONO
Cerca de 90% do ozono está na Estratosfera.
Formação do ozono:
1º - Fotodissociação das moléculas de O2 por acção das radiações UV
2º - Os radicais livres de oxigénio (O•) reagem com moléculas de oxigénio

FORMAÇÃO E DECOMPOSIÇÃO DO OZONO
Decomposição do ozono:
1º - Fotodissociação das moléculas de ozono
2º - Os radicais livres de oxigénio (O•) reagem commoléculas de ozono

FORMAÇÃO E DECOMPOSIÇÃO DO OZONO

FORMAÇÃO E DECOMPOSIÇÃO DO OZONO
A velocidade de formação de ozono é igual à sua velocidadede decomposição.
Existe um equilíbrio entre a formação e a decomposição naturais de ozono, pelo que a concentração de ozono na Estratosfera fica constante.
Este equilíbrio é importante para os seres vivos, pois é responsável pela existência da camada de ozono, queprotege a Terra da radiação ultravioleta.

FILTROS SOLARES
As radiações ultravioleta são classificadas em UVA, UVB e UVC, por ordem crescente da sua energia.
As radiações UVC são as mais energéticas e mais perigosas,mas não chegam à Terra. São absorvidas na parte superior da atmosfera (na Termosfera e, em menor grau, na Mesosfera).
As radiações UVB são absorvidas pela camada de ozono,mas algumas chegam à Terra, provocando queimaduras,cancros de pele (melanoma), doenças dos olhos, mutações genéticas, destruição de espécies vegetais e deterioração de alguns materiais.

FILTROS SOLARES
As radiações UVA, são as menos energéticas e menos perigosas, mas provocam o envelhecimento da pele, a síntese da melanina (pigmento natural que protege a pele absorvendo a radiação) e queimaduras.
Apesar da atmosfera, nomeadamente a camada de ozono,funcionar como um filtro solar, absorvendo os ultravioletas,parte desta radiação não é absorvida e atinge os seres vivos.
Assim, é importante proteger a pele, que está mais exposta à radiação solar, usando protectores solares (cremes solares).

FILTROS SOLARES
Os protectores solares têm filtros solares que absorvem ou reflectem a radiação solar:
o Filtros químicos - Formados por moléculas orgânicas que absorvem as radiações UVA e UVB;
o Filtros físicos (ecrãs minerais) - Formados por compostos inorgânicos (óxidos de zinco e de titânio) que reflectem a maior parte da radiação solar. São mais eficazes do que os filtros químicos.

FILTROS SOLARES
Índice de protecção solar ou factor de protecção solar (FPS) – Indica o número de minutos que uma pele pode estar exposta ao sol sem sofrer danos. Depende do tipo e da concentração das substâncias protectoras.
Um factor de protecção 30 indica que uma pele com esse protector suporta 30 × 10* = 300 minutos (5 horas) de exposição ao sol sem sofrer danos.
* 10 minutos de exposição ao sol sem sofrer danos e sem protector

CAMADA DE OZONO
Camada de ozono - Quantidade de ozono que existe na Estratosfera, disperso entre 15 km e 50 km de altitude.
A camada de ozono absorve as radiações ultravioleta com energia entre 6,6 x 10-19 J e 9,9 x 10-19 J, funcionando comoum filtro solar natural.
Durante a absorção da radiação ocorre efeito químico da radiação (quebra das ligações químicas) e efeito térmico (aumento da energia cinética das partículas, responsávelpelo aumento da temperatura na Estratosfera).

CAMADA DE OZONO
O ozono na Estratosfera protege os seres vivos, mas na Troposfera é uma substância nociva que irrita os olhos,o nariz e a garganta.

ALTERAÇÃO DO EQUILÍBRIO DE FORMAÇÃOE DECOMPOSIÇÃO DO OZONO
A concentração do ozono na Estratosfera manteve-se constante durante muito tempo, porque existe um equilíbrio entre a formação e a decomposição naturais do ozono .
Mas, a concentração do ozono começoua diminuir quando substâncias,libertadas pelo Homem para atmosfera(óxidos de azoto e radicais de cloro Cl•),aumentaram a velocidade dedecomposição do ozono.

ALTERAÇÃO DO EQUILÍBRIO DE FORMAÇÃOE DECOMPOSIÇÃO DO OZONO
Os óxidos de azoto formam-se a partir do oxigénio e do azoto atmosféricos, a temperaturas elevadas, com os efluentes dos aviões supersónicos.
Os radicais Cl• formam-se principalmente a partir dos CFC (clorofluorcarbonetos ou freons).
Os CFC são derivados do metano (CH4) e do etano (C2H6),onde os átomos de hidrogénio são substituídos por átomosde cloro e de flúor (derivados halogenados):CFCl3 (triclorofluormetano) e CF2Cl2 (diclorodifluormetano).

ALTERAÇÃO DO EQUILÍBRIO DE FORMAÇÃOE DECOMPOSIÇÃO DO OZONO
Os CFC têm sido usados no arrefecimento dos frigoríficos e aparelhos de ar condicionado, em espumas de isolamento térmico, em latas de spray (lacas, desodorizantes e perfumes), diluentes, etc.
A maioria dos CFC acabam por ser lançados na atmosfera e, como são praticamente inertes (reagem pouco), atingem a Estratosfera e provocam a destruição do ozono.

DESTRUIÇÃO DO OZONO
Na Estratosfera, os CFC são decompostos pelas radiações UV, formando os radicais cloro:
O radical cloro reage com o ozono, formando monóxido de cloro e oxigénio (reacção A). O monóxido de cloro reage com o radical oxigénio e forma radical cloro (reacção B):

DESTRUIÇÃO DO OZONO
A reacção global resultante das reacções A e B pode ser representada pela seguinte equação:
O radical cloro não aparece na reacção global porque é consumido na 1ª reacção e forma-se de novo na 2ª reacção, ficando disponível para reagir novamente com o ozono.
Significa que funciona como um catalisador(aumenta a velocidade da reacção sem se transformar).Outros catalisadores da decomposição do ozono são as que produzem os radicais livres:

DESTRUIÇÃO DO OZONO
Para além dos agentes antropogénicos (CFC e óxidos de azoto), também existem agentes naturais que podem provocar a destruição do ozono.
Os principais agentes naturais são os vulcões, cujas erupções libertam grandes quantidades de gases para a Estratosfera.As partículas finas e o ácido sulfúrico contidos nestes gases também podem funcionar como catalisadores da decomposição do ozono.

BURACO DE OZONO
A diminuição da camada de ozono não é uniforme emtoda a atmosfera, sendo muito acentuada na Antárctida(foi detectada em 1987, sobre o Pólo Sul).
Buraco de ozono - Zona sobre a Antárctida onde o ozonoquase desapareceu.
Desde 1987 (Protocolo de Montreal) que alguns países têm estabelecido normas e prazos para a redução dos CFC.

BURACO DE OZONO

BURACO DE OZONO
Os ventos polares empurramos CFC para o Pólo Sul.
Durante 6 meses, o Pólo Sul ficasem luz solar e com temperaturasaté -80 ºC.
Formam-se pequenos cristais de geloque actuam como catalisadores natransformação dos CFC em radicaiscloro, o que aumenta ainda maiscom as radiações UV do Sol, duranteos restantes 6 meses.

BURACO DE OZONO
Nas latitudes médias, a radiação ultravioleta tem sido constante na última década.
Em 2010, a quantidade de ozono não estava a diminuirnem a aumentar.
A camada de ozono, fora das regiões polares, deve recuperaraté 2050, para os níveis antes de 1980, mas o buraco de ozono sobre a Antártida deve recuperar muito mais tarde.
O buraco de ozono já está a influenciar o clima da Terra, alterando a temperatura e o movimento do vento.
Fonte: Earth Observatory (NASA)



BIBLIOGRAFIA
Dantas, M., & Ramalho, M. (2008). Jogo de Partículas A – Físicae Química A - Química - Bloco 1 - 10º/11º Ano. Lisboa: Texto Editores.